Clear Sky Science · ru
Эндокринная терапия перепрограммирует рак молочной железы, способствуя метастатическому побегу за счёт повышения сигнальной активности P-Rex1/Rac1
Почему это исследование важно для пациентов
Множество опухолей молочной железы питаются гормоном эстрогеном и в течение многих лет после операции лечатся препаратами, блокирующими этот сигнал. Тем не менее значительная доля таких опухолей может тихо возвращаться спустя долгое время после окончания терапии. В этом исследовании показано, как гормон-блокирующая терапия может переводить часть клеток в медленно растущее, но готовое к миграции состояние, и что блокада определённого пути клеточного движения может помочь предотвратить эти поздние, опасные рецидивы. 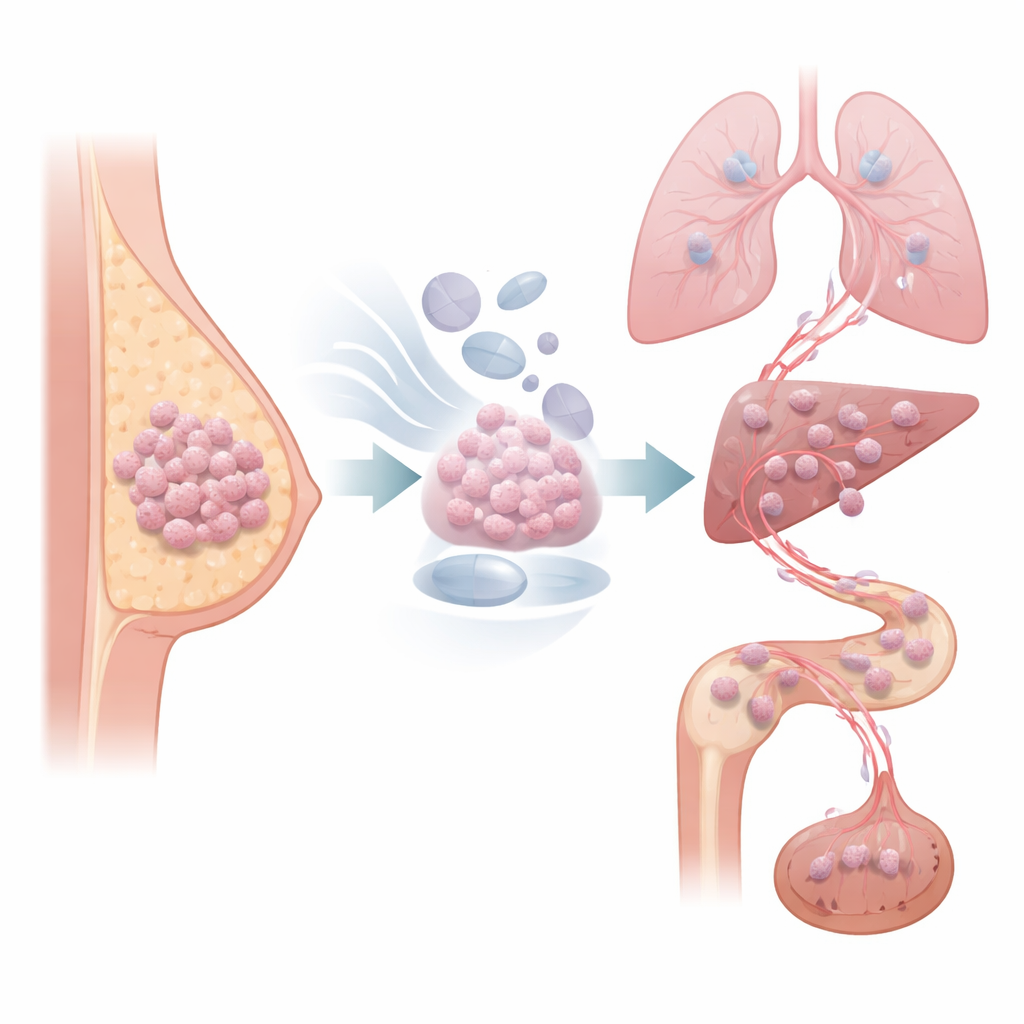
Медленные, но опасные клетки рака
Врачи давно наблюдают, что некоторые опухоли с положительными эстрогеновыми рецепторами возвращаются через десять и более лет после первоначального лечения. Эти поздние рецидивы часто растут медленно, но их трудно излечить после распространения. При исследовании тканей пациентов учёные обнаружили, что метастазы из эстроген-зависимых опухолей часто содержали меньше активно делящихся клеток, чем исходные опухоли в груди. Это указывало на то, что медленно растущие клетки, а не только быстро делящиеся, могут играть ключевую роль в позднем распространении.
Создание модели тихого побега
Чтобы изучить этих «тихих побегунов», команда лечила чувствительные к эстрогену клетки рака молочной железы обычными гормон-блокирующими препаратами в лаборатории. Со временем возникли два типа выживших: быстрорастущие резистентные клетки и вторая группа, которая делилась медленно, но отказывалась умирать. Когда медленные клетки имплантировали мышам, они формировали меньшие первичные опухоли молочной железы с признаками, напоминающими стареющие или подвергшиеся стрессу клетки, включая крупные деформированные ядра и плотный коллаген вокруг них. Несмотря на такое вялое ростовое поведение в исходном очаге, эти клетки распространялись в лёгкие и кости так же эффективно, как и быстрорастущие клетки, что демонстрирует: скорость роста и способность к распространению — разные вещи. 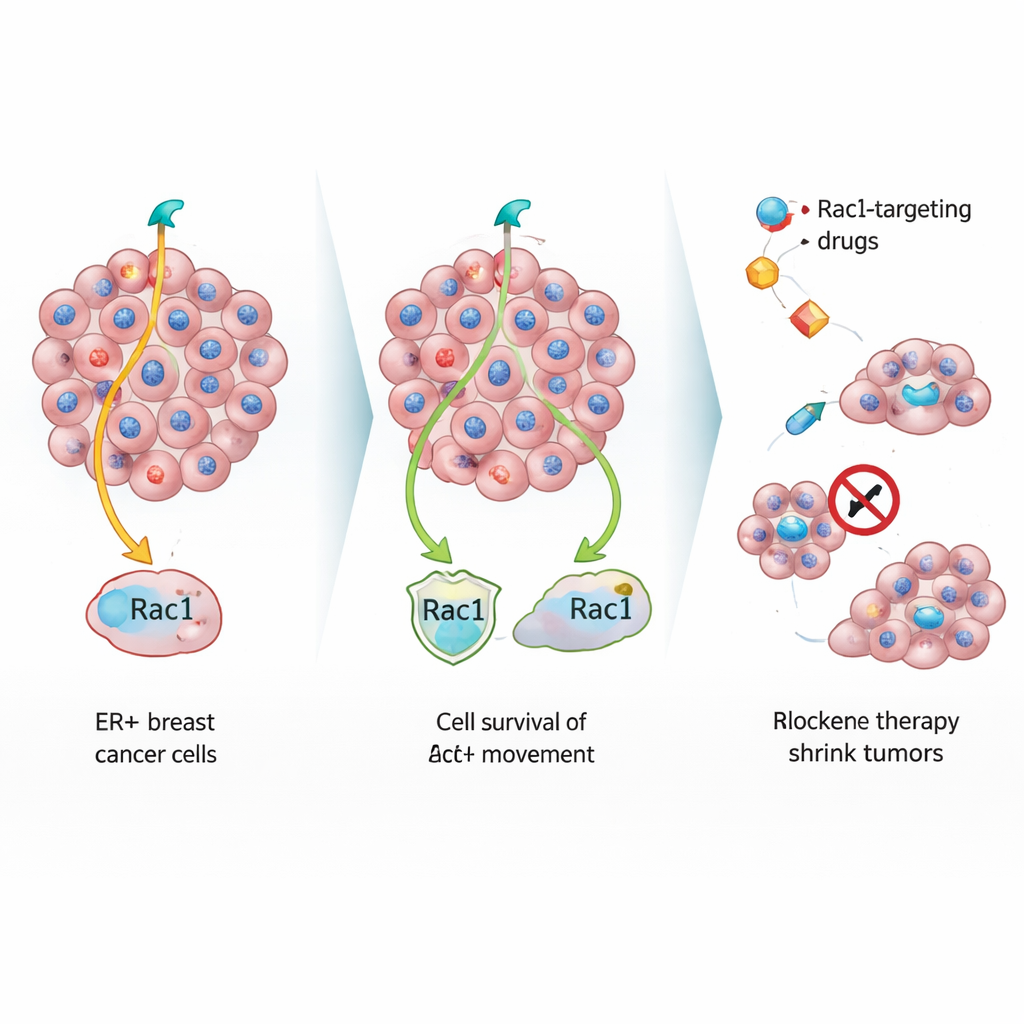
Переключатель движения, срабатывающий при лечении
Затем команда использовала секвенирование РНК одиночных клеток, метод, позволяющий прочитать активность тысяч генов в отдельной клетке, чтобы увидеть, как гормональная терапия перенастраивает этих выживших. Они обнаружили, что эндокринная терапия переводит часть клеток в состояние, похожее на сенесценцию, при котором деление замедляется, но пути выживания остаются активными. В этих клетках сильно усиливался сигнальный маршрут, сосредоточенный вокруг белков P-Rex1 и Rac1. Rac1 контролирует форму и движение клетки, а P-Rex1 — один из его ключевых активаторов. Медленные резистентные клетки зависели от этой оси для своей миграционной способности, а анализ образцов пациентов показал повышенный уровень P-Rex1 в опухолях с положительным эстрогеновым рецептором и их метастазах, особенно в случаях поздних рецидивов.
Тестирование новых комбинаций лекарств
Поскольку путь P-Rex1/Rac1 выглядел как двигатель движения и выживания для этих толерантных клеток, исследователи протестировали препараты, ослабляющие активность Rac1. В культуре эти ингибиторы снижали образование колоний и замедляли закрытие раневых имитаций у медленных резистентных клеток сильнее, чем у быстрых. В моделях на мышах с встроенными флуоресцентными датчиками активности Rac1 два препарата, нацеленных на Rac1, явно снижали Rac1-сигнал внутри опухолей, леченных тамоксифеном. В модели опухоли, полученной от пациентки, чья болезнь уже устояла перед несколькими гормональными терапиями, ингибиторы Rac1 в одиночку умеренно замедляли рост опухоли и увеличивали выживаемость. При комбинации с тамоксифеном они, однако, вызывали регрессию опухолей и существенно уменьшали итоговый вес опухолей.
Подсказки от распространённых обезболивающих
Один из агентoв-блокаторов Rac1, R-кеторолак, является зеркальным изомером препарата, уже применяемого для обезболивания после операций. Команда провела метаанализ предыдущих клинических исследований, в которых отслеживали исходы рака молочной железы у пациенток, получавших кеторолак в периоперационный период. В этих исследованиях применение кеторолaка связывалось с меньшим риском рецидива рака, тогда как другие обезболивающие без активности против Rac1 такой связи не показывали. Хотя это само по себе не доказательство, сигнал на уровне популяции поддерживает идею, что временная блокада Rac1 в ключевые периоды лечения может снизить вероятность того, что толерантные клетки посеют будущие метастазы.
Что это значит для будущего
Для неспециалиста главный вывод таков: гормональная терапия может непреднамеренно преобразовать часть клеток рака молочной железы в медленно делящиеся, но весьма способные к миграции. Эта работа выделяет путь P-Rex1/Rac1 как «ручку управления» для такого поведения и показывает на животных, что её ослабление, особенно в сочетании со стандартными гормональными препаратами, может уменьшать резистентные опухоли. Эти результаты ещё не стали основанием для нового стандартного лечения, но они предполагают, что добавление безопасных стратегий таргетирования Rac1, возможно даже заимствованных из существующих обезболивающих, однажды поможет предотвратить поздние, угрожающие жизни рецидивы эстроген-зависимого рака молочной железы.
Цитирование: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Ключевые слова: рак молочной железы с положительным эстрогеновым рецептором, резистентность к эндокринной терапии, метастазирование, сигналинг Rac1, P-Rex1