Clear Sky Science · nl
Hormonale therapie herprogrammeert borstkanker en vergemakkelijkt metastatische ontsnapping via opregulatie van P-Rex1/Rac1-signaalgeving
Waarom dit onderzoek belangrijk is voor patiënten
Veel borstkankers worden aangedreven door het hormoon oestrogeen en worden jarenlang behandeld met middelen die dit signaal blokkeren na de operatie. Toch kan een groot deel van deze kankers stilletjes terugkeren lang nadat de behandeling lijkt te zijn afgerond. Deze studie onthult hoe hormoonblokkerende therapie sommige kankercellen in een langzaam groeiende maar reisklare toestand kan duwen, en laat zien dat het blokkeren van een specifiek celdelings- en bewegingspad kan helpen deze late, dodelijke terugkeer te voorkomen. 
Langzame maar gevaarlijke kankercellen
Artsen zien al lange tijd dat sommige oestrogeenreceptor-positieve borstkankers tien jaar of langer na de oorspronkelijke behandeling terugkomen. Deze late recidieven groeien vaak langzaam maar zijn moeilijk te genezen zodra ze zich hebben verspreid. Door weefsel van patiënten te onderzoeken, vonden de onderzoekers dat uitzaaiingen van oestrogeengedreven tumoren vaak minder actief delende cellen bevatten dan de oorspronkelijke borsttumoren. Dit suggereert dat langzaam groeiende cellen, niet alleen snel delende exemplaren, belangrijke drijvende krachten kunnen zijn achter late verspreiding.
Een model bouwen van stille ontsnapping
Om deze stille ontsnappers te bestuderen, behandelde het team in het laboratorium oestrogeen-gevoelige borstkankercellen met standaard hormoonblokkerende middelen. Na verloop van tijd ontstonden twee soorten overlevenden: snel groeiende resistente cellen en een tweede groep die langzaam deelde maar niet wilde afsterven. Toen de langzamere cellen in muizen werden geïmplanteerd, vormden ze kleinere primaire borsttumoren met kenmerken die leken op verouderde of gestreste cellen, waaronder grote, vervormde kernen en dichte collageenophoping rondom hen. Ondanks deze trage groei op de oorspronkelijke plaats, verspreidden deze cellen zich naar de longen en botten even efficiënt als de snel groeiende cellen, wat aantoont dat groeisnelheid en verspreiding niet hetzelfde zijn. 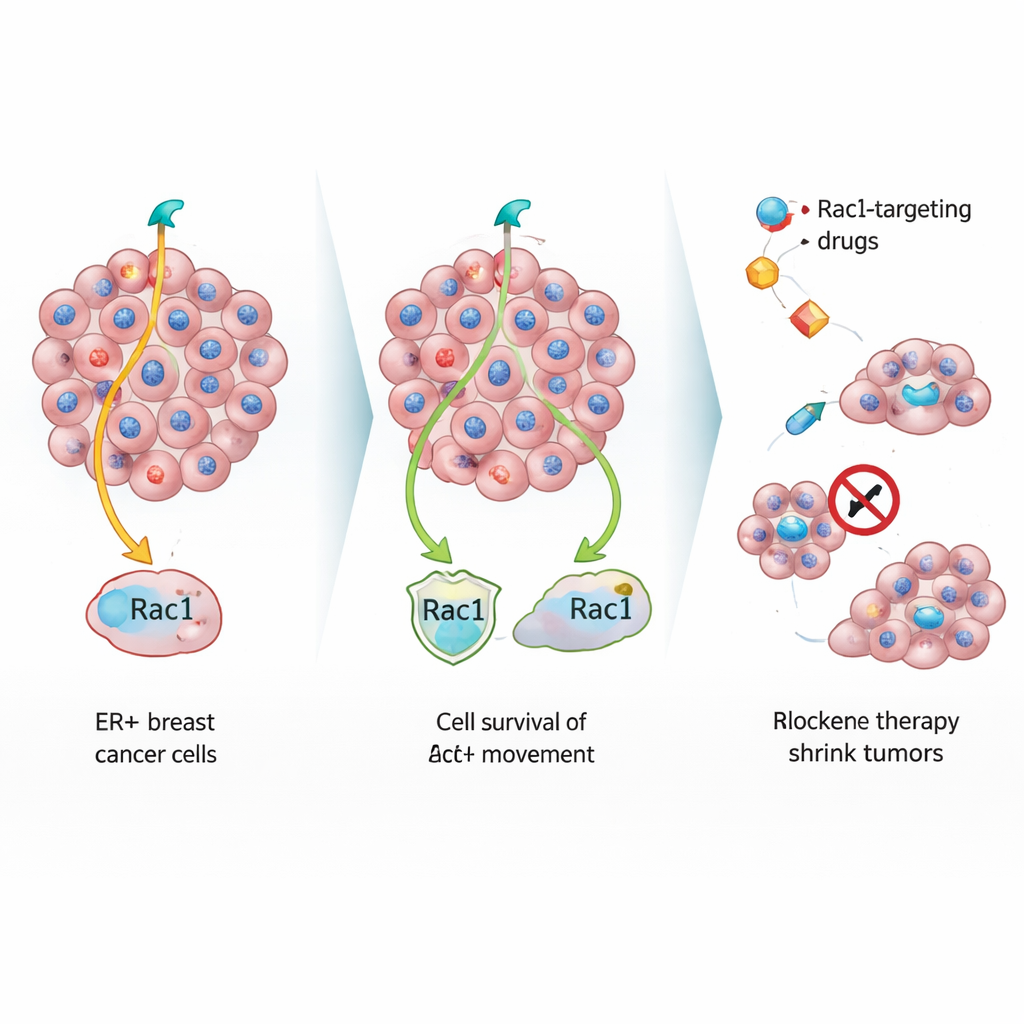
Een bewegingsschakelaar omgeklapt door behandeling
Vervolgens gebruikten de onderzoekers single cell RNA-sequencing, een techniek die de activiteit van duizenden genen in individuele cellen uitleest, om te zien hoe hormonale therapie deze overlevenden herbedraadde. Ze vonden dat endocriene behandeling een subset cellen in een senescent-achtige toestand dreef, waarin deling vertraagt maar overlevingsroutes actief blijven. In deze cellen was een signaalroute rond de eiwitten P-Rex1 en Rac1 sterk opgereguleerd. Rac1 helpt de celvorm en beweging te regelen, en P-Rex1 is een van zijn belangrijke activatoren. De langzaam resistente cellen waren afhankelijk van deze as voor hun migratievermogen, en patiëntmonsters toonden dat P-Rex1-niveaus hoog waren in oestrogeenreceptor-positieve tumoren en hun uitzaaiingen, vooral bij gevallen die laat terugkeerden.
Nieuwe medicijncombinaties testen
Aangezien de P-Rex1/Rac1-route leek te fungeren als motor voor beweging en overleving van deze tolerante cellen, testten de onderzoekers middelen die Rac1-activiteit dempen. In kweek verminderten deze remmers de kolonievorming en vertraagden ze wondachtige sluiting door de langzaam resistente cellen meer dan bij de snelle cellen. In muismodellen met ingebouwde fluorescerende sensoren voor Rac1-activiteit verlaagden twee Rac1-gerichte verbindingen zichtbaar de Rac1-signaalgeving binnen tamoxifeenbehandelde tumoren. In een patiënt-afgeleid tumormodel afkomstig van een vrouw wiens kanker al tegen meerdere hormoontherapieën had geresisteerd, vertraagden Rac1-remmers alleen de tumorgroei bescheiden en verlengden ze de overleving. In combinatie met tamoxifeen veroorzaakten ze echter tumorkrimp en verminderden ze het uiteindelijke tumorgewicht significant.
Aanwijzingen uit bestaande pijnstillers
Een van de Rac1-blokkerende middelen, R-ketorolac, is het spiegelbeeld van een geneesmiddel dat al wordt gebruikt voor pijnbestrijding na een operatie. Het team voerde een meta-analyse uit van eerdere klinische studies die uitkomsten bij borstkankerpatiënten volgden die ketorolac rond de operatietijd kregen. In deze studies werd gebruik van ketorolac gekoppeld aan een lager risico op kankerrecidief, terwijl andere pijnstillers zonder Rac1-remmende activiteit dit patroon niet lieten zien. Hoewel dit op zichzelf geen bewijs is, ondersteunt deze aanwijzing op populatieniveau het idee dat tijdelijke blokkade van Rac1 tijdens cruciale behandelingsvensters de kans kan verkleinen dat tolerante cellen toekomstige uitzaaiingen zaaien.
Wat dit betekent voor de toekomst
Voor niet-specialisten is de kernboodschap dat hormoontherapie onbedoeld sommige borstkankercellen kan herschikken in langzaam delende maar zeer capabele reizigers. Dit werk identificeert het P-Rex1/Rac1-pad als een regelknop voor dat gedrag en laat in diermodellen zien dat het terugdraaien van die knop, vooral in combinatie met standaard hormoonmiddelen, resistente tumoren kan doen krimpen. De bevindingen vertalen zich nog niet direct naar een nieuwe standaardbehandeling, maar ze suggereren dat het toevoegen van veilige Rac1-richtende strategieën, mogelijk zelfs aangepast uit bestaande pijnmiddelen, op termijn kan helpen late, levensbedreigende terugkeer van oestrogeengedreven borstkanker te voorkomen.
Bronvermelding: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Trefwoorden: oestrogeenreceptor-positieve borstkanker, resistentie tegen endocriene therapie, metastase, Rac1-signaalgeving, P-Rex1