Clear Sky Science · sv
Endokrin terapi omprogrammerar bröstcancer och underlättar metastatisk flykt via uppreglering av P-Rex1/Rac1‑signalering
Varför denna forskning är viktig för patienter
Många bröstcancerformer drivs av hormonet östrogen och behandlas med läkemedel som blockerar denna signal i åratal efter operation. Trots det kan en stor andel av dessa cancerformer tyst återkomma långt efter att behandlingen verkar avslutad. Denna studie avslöjar hur hormonblockerande behandling kan pressa vissa cancerceller in i ett långsamt växande men reseklart tillstånd, och visar att blockering av en specifik cellrörelseväg kan hjälpa till att stoppa dessa sena, dödliga återfall. 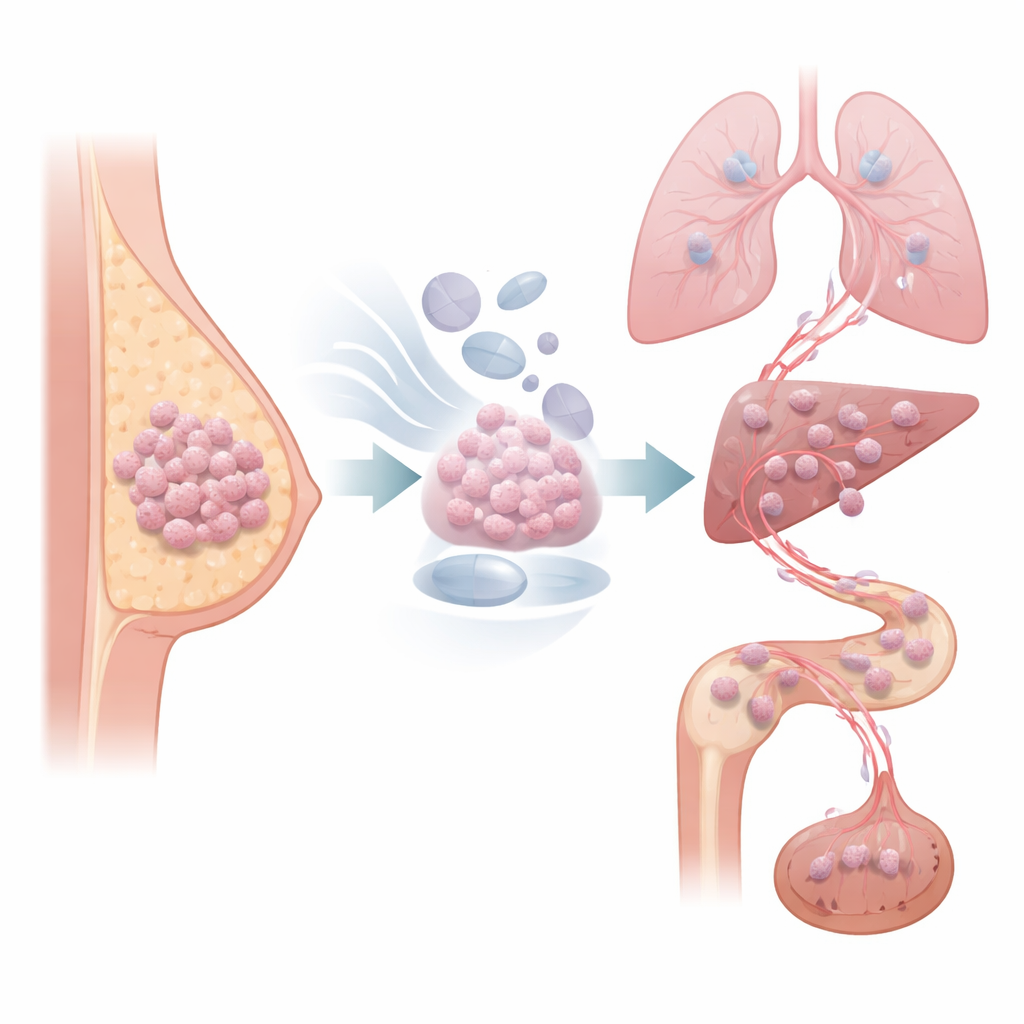
Långsamma men farliga cancerceller
Läkare har länge sett att vissa östrogenreceptorpositiva bröstcancer kommer tillbaka ett decennium eller mer efter första behandlingen. Dessa sena återfall växer ofta långsamt men är svåra att bota när de väl har spridit sig. Genom att undersöka patientvävnad fann forskarna att metastaser från östrogenstyrda tumörer ofta innehöll färre aktivt delande celler än de ursprungliga brösttumörerna. Detta tyder på att långsamt växande celler, inte bara snabbt delande, kan vara nyckeldrivkrafter bakom sen spridning.
Bygga en modell för tyst flykt
För att studera dessa tysta flyktkonstnärer behandlade teamet östrogenkänsliga bröstcancerceller med standardiserade hormonblockerande läkemedel i laboratoriet. Med tiden uppstod två typer av överlevare: snabbväxande resistenta celler och en andra grupp som delade sig långsamt men vägrade dö. När de långsammare cellerna implanterades i möss bildade de mindre primära brösttumörer med egenskaper som liknade åldrade eller stressade celler, inklusive stora, förvrängda cellkärnor och tät kollagen omkring dem. Trots denna långsamma tillväxt på ursprungsplatsen spred sig dessa celler till lungor och ben lika effektivt som de snabbväxande cellerna, vilket visar att tillväxthastighet och spridning inte är samma sak. 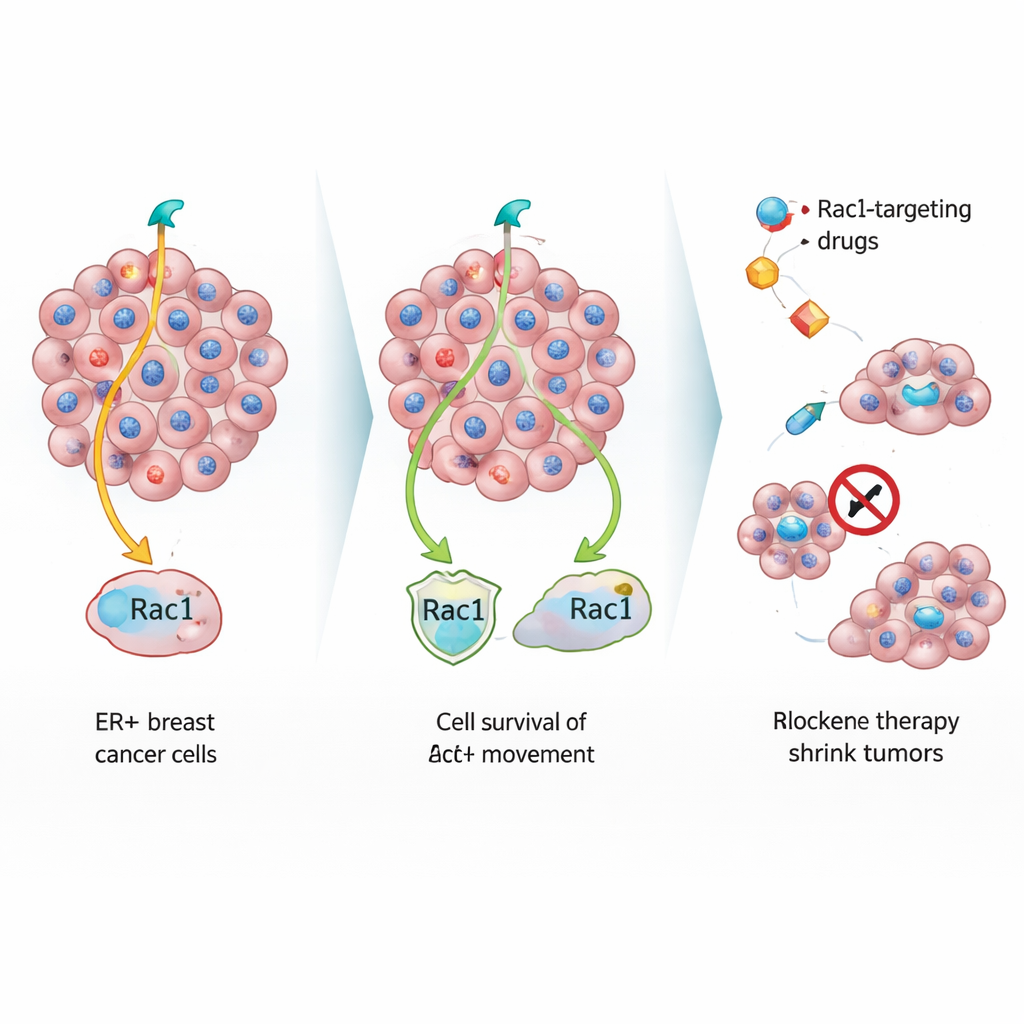
En rörelsereglerare som växlas om av behandlingen
Teamet använde sedan single cell RNA‑sekvensering, en teknik som läser aktiviteten hos tusentals gener i enskilda celler, för att se hur hormonbehandling omkopplade dessa överlevare. De fann att endokrin behandling pressade en undergrupp celler mot ett senescent‑liknande tillstånd, där delning avstannar men överlevnads‑vägar förblir aktiva. I dessa celler var en signalväg centrerad kring proteinerna P‑Rex1 och Rac1 starkt uppreglerad. Rac1 hjälper till att kontrollera cellform och rörelse, och P‑Rex1 är en av dess nyckelaktivatorer. De långsamma resistenta cellerna var beroende av denna axel för sin förmåga att migrera, och patientprov visade att P‑Rex1‑nivåerna var höga i östrogenreceptorpositiva tumörer och deras metastaser, särskilt i fall som återkom sent.
Test av nya läkemedelskombinationer
Där P‑Rex1/Rac1‑vägen såg ut att vara en rörelse‑ och överlevnadsmotor för dessa toleranta celler testade forskarna läkemedel som dämpar Rac1‑aktivitet. I odlingar minskade dessa hämmare koloni‑bildning och bromsade sårliknande slutförande hos de långsamma resistenta cellerna mer än hos de snabba. I musmodeller med inbyggda fluorescerande sensorer för Rac1‑aktivitet sänkte två Rac1‑riktade föreningar tydligt Rac1‑signaleringen i tamoxifenbehandlade tumörer. I en patient‑härledd tumörmodell tagen från en kvinna vars cancer redan resistent mot flera hormonbehandlingar hade Rac1‑hämmare ensamma en måttlig effekt på att sakta tumörtillväxt och förlänga överlevnad. När de kombinerades med tamoxifen fick de tumörerna att krympa och minskade avsevärt slutlig tumörvikt.
Ledtrådar från verkliga smärtstillande
En av Rac1‑blockerande substanserna, R‑ketorolak, är spegelbilden av ett läkemedel som redan används för smärtlindring efter operation. Teamet genomförde en metaanalys av tidigare kliniska studier som följt bröstcancerutfall hos patienter som fick ketorolak i samband med operation. I dessa studier kopplades användning av ketorolak till en lägre risk för canceråterfall, medan andra smärtstillande utan Rac1‑riktad aktivitet inte visade samma mönster. Även om detta inte är bevis i sig, stöder denna populationsnivå‑signal idén att tillfällig blockering av Rac1 under avgörande behandlingsfönster kan minska chansen att toleranta celler sår framtida metastaser.
Vad detta betyder för framtiden
För en icke‑specialist är huvudbudskapet att hormonbehandling oavsiktligt kan omforma vissa bröstcancerceller till långsamt delande men mycket kapabla resenärer. Detta arbete identifierar P‑Rex1/Rac1‑vägen som en kontrollknapp för det beteendet och visar i djurmodeller att man kan vrida ned denna knapp, särskilt i kombination med standard hormonläkemedel, för att krympa resistenta tumörer. Resultaten översätts ännu inte till en ny standardbehandling, men de antyder att tillägg av säkra strategier för att rikta Rac1, möjligen även anpassade från befintliga smärtmedel, en dag kan hjälpa till att förhindra sena, livshotande återfall av östrogenstyrd bröstcancer.
Citering: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Nyckelord: östrogenreceptorpositiv bröstcancer, resistens mot endokrin terapi, metastas, Rac1‑signalering, P-Rex1