Clear Sky Science · ar
إعادة برمجة العلاج الهرموني لسرطان الثدي تُسهل الهروب النقيلي عبر زيادة إشارات P-Rex1/Rac1
لماذا يهم هذا البحث المرضى
العديد من سرطانات الثدي تغذيها هرمونات الاستروجين ويُعالجها الأطباء بأدوية تحجب هذا الإشارة لسنوات بعد الجراحة. ومع ذلك، فإن جزءًا كبيرًا من هذه الأورام قد يعود بهدوء بعد وقت طويل من انتهاء العلاج الظاهر. تكشف هذه الدراسة كيف يمكن أن يدفع العلاج المانع للهرمونات بعض الخلايا السرطانية إلى حالة بطيئة النمو لكنها جاهزة للانتقال، وتبيّن أن حجب مسار محدد لحركة الخلايا قد يساعد في وقف هذه العودة المتأخرة والقاتلة. 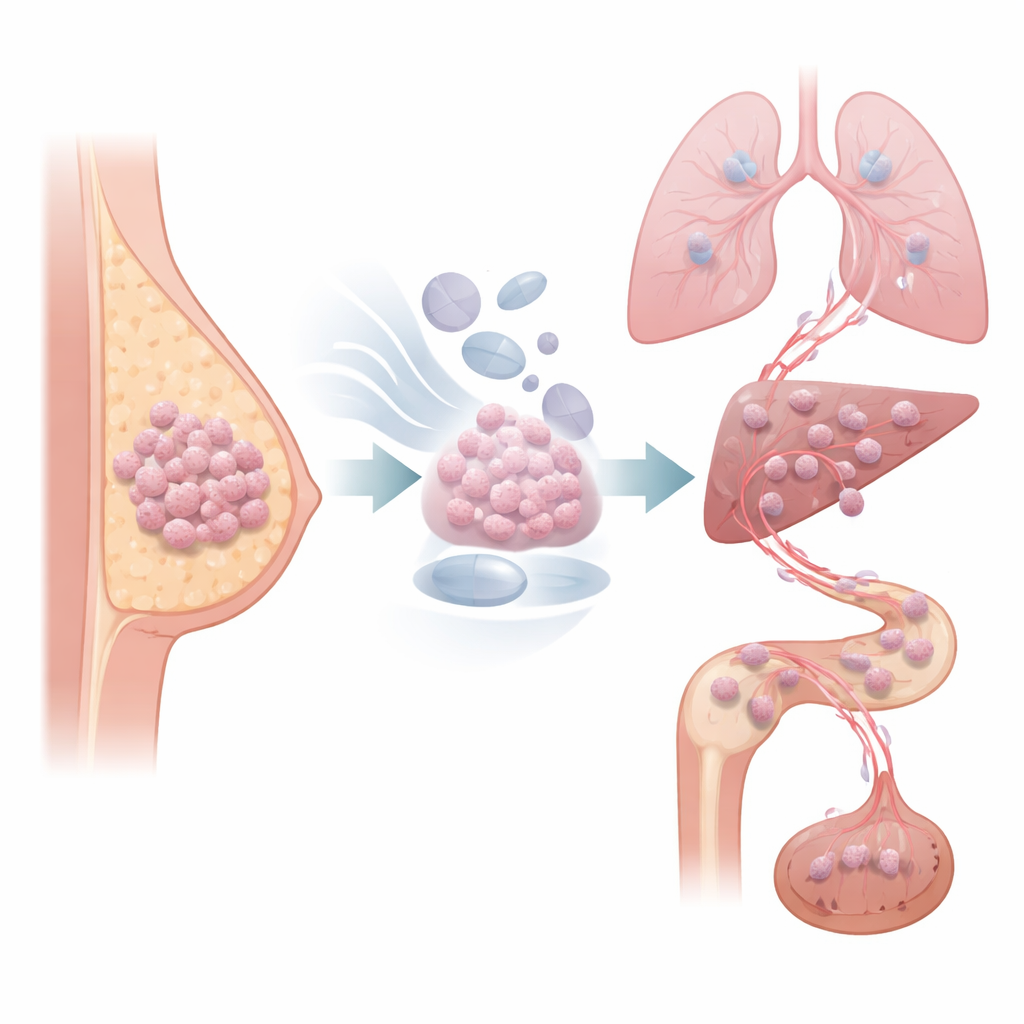
خلايا بطيئة لكنها خطيرة
لاحظ الأطباء منذ زمن أن بعض سرطانات الثدي موجبة مستقبل الاستروجين تعود بعد مرور عقد أو أكثر من المعالجة الأولية. هذه الانتكاسات المتأخرة غالبًا ما تنمو ببطء لكنها تصعب معالجتها بمجرد انتشارها. من خلال فحص أنسجة المرضى، وجد الباحثون أن النقائل من الأورام المحركة بالهرمونات احتوت في كثير من الأحيان على خلايا أقل انقسامًا مقارنة بالأورام الأصلية في الثدي. وهذا يوحي بأن الخلايا البطيئة النمو، وليس فقط السريعة الانقسام، قد تكون المحرك الرئيس للانتشار المتأخر.
بناء نموذج للهروب الصامت
لدراسة هؤلاء الهاربين الصامتين، عالج الفريق خلايا سرطان ثدي الحساسة للاستروجين بأدوية منع الهرمونات القياسية في المختبر. مع مرور الوقت، ظهر نوعان من الناجين: خلايا مقاومة سريعة النمو ومجموعة ثانية انقسمت ببطء لكنها رفضت الموت. عندما زُرعت الخلايا الأبطأ في فئران، كوّنت أورامًا أولية أصغر بسمات تشبه الخلايا المسنة أو المتوترة، بما في ذلك أنوية كبيرة مشوهة وكثافة عالية من الكولاجين حولها. وعلى الرغم من هذا النمو البطيء في الموقع الأصلي، انتشرت هذه الخلايا إلى الرئتين والعظام بكفاءة مماثلة للخلايا سريعة النمو، مما يكشف أن سرعة النمو وانتشار الخلايا ليسا الشيء نفسه. 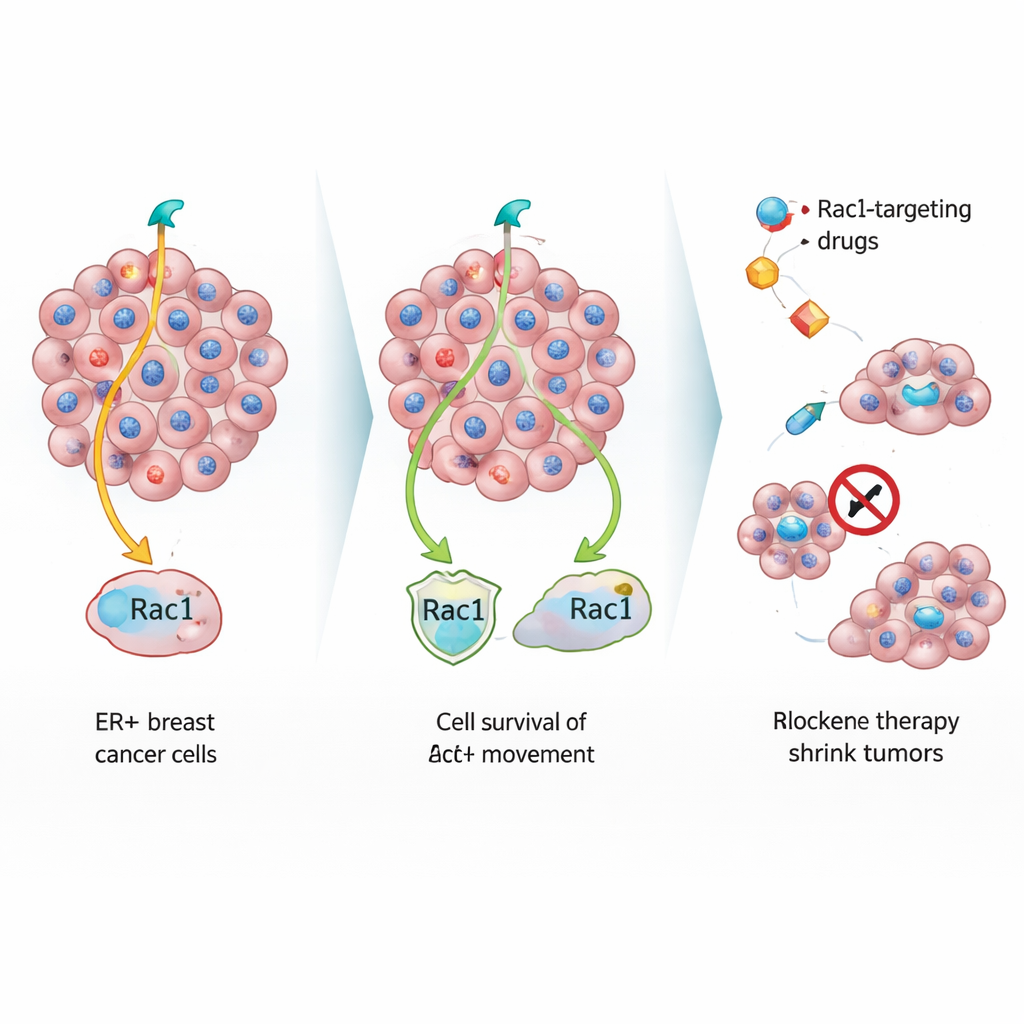
مفتاح حركة تقلبه المعالجة
ثم استخدم الفريق تسلسل الحمض النووي الريبي للخلايا المفردة، وهي تقنية تقرأ نشاط آلاف الجينات في كل خلية على حدة، ليرى كيف يعيد العلاج الهرموني توصيل هذه الخلايا الناجية. وجدوا أن المعالجة الهرمونية دفعت مجموعة فرعية من الخلايا إلى حالة شبيهة بالهرم، حيث يتباطأ الانقسام لكن تبقى مسارات البقاء نشطة. في هذه الخلايا، ارتفع نشاط مسار إشاري يتركز حول بروتينات تُدعى P-Rex1 وRac1. يساعد Rac1 في التحكم بشكل الخلية وحركتها، وP-Rex1 هو أحد منشطاته الرئيسية. اعتمدت الخلايا البطيئة المقاومة على هذا المحور لقدرتها على الهجرة، وأظهرت عينات المرضى أن مستويات P-Rex1 كانت مرتفعة في الأورام موجبة مستقبل الاستروجين ونقائلها، لا سيما في الحالات التي عادت متأخرًا.
اختبار تركيبات دوائية جديدة
لأن محور P-Rex1/Rac1 بدا كمحرك للحركة والبقاء لتلك الخلايا المتحملة، اختبر الباحثون أدوية تُضعف نشاط Rac1. في الأطباق المخبرية، خفّضت هذه المثبطات تكوين المستعمرات وأبطأت إغلاق تشبه الجروح لدى الخلايا البطيئة المقاومة أكثر من الخلايا السريعة. في نماذج فئران مزودة بمستشعرات فلورية لنشاط Rac1، خفضت مركبان مستهدفا Rac1 بشكل مرئي إشارات Rac1 داخل أورام معالجة بالتاموكسيفين. في نموذج ورم مشتق من مريضات أخذ من امرأة كانت سرطاناتها قد صمدت أمام علاجات هرمونية متعددة، أبطأت مثبطات Rac1 نمو الورم مؤقتًا وطالَت البقاء. ولكن عند الجمع مع التاموكسيفين، تراجعت الأورام وانخفض وزن الورم النهائي بشكل ملحوظ.
دلالات من مسكنات الألم المستخدمة فعليًا
أحد العوامل المانعة لـRac1، R-ketorolac، هو الصورة المرآتية لدواء يُستخدم بالفعل لتسكين الألم بعد الجراحة. أجرى الفريق تحليلًا تلويًا لدراسات سريرية سابقة راقبت نتائج سرطان الثدي لدى مرضى تلقوا كيتورولاك حول وقت الجراحة. عبر هذه الدراسات، ارتبط استخدام كيتورولاك بخطر أقل لعودة السرطان، بينما لم تظهر مسكنات أخرى تفتقر إلى نشاط استهداف Rac1 نفس النمط. وعلى الرغم من أن هذا ليس دليلًا قاطعًا بمفرده، فإن هذه الإشارة على مستوى السكان تدعم الفكرة القائلة بأن حجب Rac1 مؤقتًا خلال فترات علاجية حرجة قد يقلل من احتمال أن تؤسس الخلايا المتحملة نقائل مستقبلية.
ماذا يعني هذا للمستقبل
للغير مختص، الرسالة المركزية هي أن العلاج الهرموني قد يعيد تشكيل بعض خلايا سرطان الثدي بشكل غير مقصود إلى خلايا بطيئة الانقسام لكنها مسافرة بكفاءة عالية. تحدد هذه الدراسة محور P-Rex1/Rac1 كزر تحكم لهذا السلوك وتُظهر في الحيوانات أن خفض نشاط هذا المحور، خصوصًا بالمزامنة مع أدوية الهرمون القياسية، يمكن أن يقلص الأورام المقاومة. النتائج لم تُترجم بعد إلى بروتوكول علاجي جديد، لكنها تقترح أن إضافة استراتيجيات آمنة لاستهداف Rac1، وربما مستعارة من أدوية مسكنة موجودة، قد تساعد يومًا ما في الوقاية من عودات متأخرة ومهددة للحياة لأورام الثدي المحركة بالاستروجين.
الاستشهاد: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
الكلمات المفتاحية: سرطان الثدي موجِب لمستقبل الاستروجين, مقاومة العلاج الهرموني, النقائل, إشارات Rac1, P-Rex1