Clear Sky Science · pt
Terapia endócrina reprograma o câncer de mama facilitando a fuga metastática via aumento da sinalização P-Rex1/Rac1
Por que esta pesquisa importa para pacientes
Muitos cânceres de mama são alimentados pelo hormônio estrogênio e são tratados com drogas que bloqueiam esse sinal por anos após a cirurgia. Ainda assim, uma grande parcela desses tumores pode retornar silenciosamente muito depois de o tratamento parecer encerrado. Este estudo revela como a terapia de bloqueio hormonal pode empurrar algumas células cancerígenas para um estado de crescimento lento, porém pronto para viajar, e mostra que bloquear uma via específica de movimentação celular pode ajudar a impedir esses retornos tardios e letais. 
Células cancerígenas lentas, mas perigosas
Médicos há muito observam que alguns cânceres de mama positivos para receptor de estrogênio reaparecem uma década ou mais após o tratamento inicial. Essas recorrências tardias frequentemente crescem lentamente, mas são difíceis de curar quando já se espalharam. Ao examinar tecidos de pacientes, os pesquisadores descobriram que as metástases de tumores dirigidos por estrogênio frequentemente continham menos células em divisão ativa do que os tumores mamários originais. Isso sugere que células de crescimento lento, e não apenas as de divisão rápida, podem ser os principais motores da disseminação tardia.
Construindo um modelo da fuga silenciosa
Para estudar esses artistas da fuga silenciosa, a equipe tratou células de câncer de mama sensíveis ao estrogênio com drogas bloqueadoras hormonais padrão em laboratório. Com o tempo, emergiram dois tipos de sobreviventes: células resistentes de crescimento rápido e um segundo grupo que se dividia lentamente, mas se recusava a morrer. Quando as células mais lentas foram implantadas em camundongos, formaram tumores mamários primários menores com características semelhantes a células envelhecidas ou estressadas, incluindo núcleos grandes e distorcidos e colágeno denso ao redor. Apesar desse crescimento lento no local primário, essas células se espalharam para pulmões e ossos com a mesma eficiência das células de crescimento rápido, revelando que velocidade de crescimento e capacidade de disseminação não são a mesma coisa. 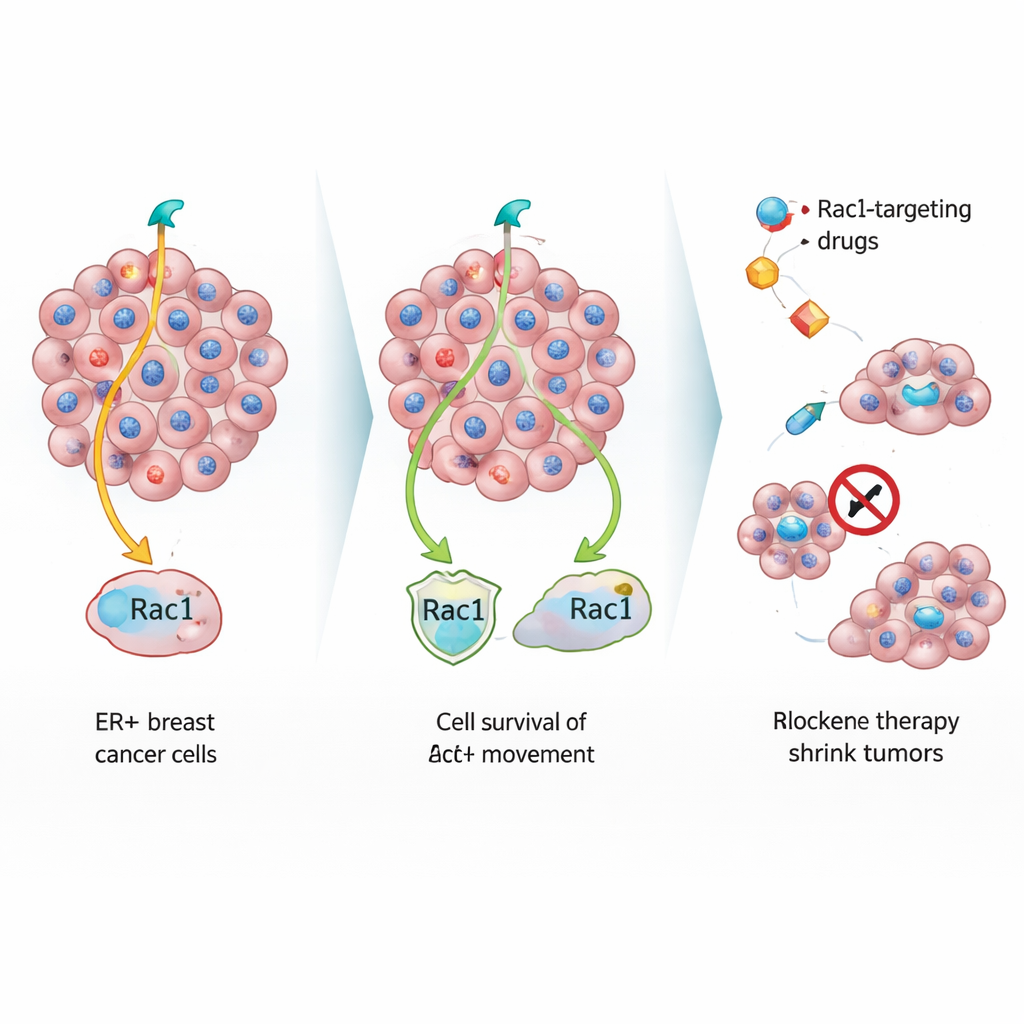
Um interruptor de movimento acionado pelo tratamento
A equipe então usou sequenciamento de RNA de célula única, uma técnica que lê a atividade de milhares de genes em células individuais, para ver como a terapia hormonal estava reconfigurando esses sobreviventes. Eles descobriram que o tratamento endócrino empurrou um subconjunto de células para um estado semelhante à senescência, em que a divisão desacelera, mas vias de sobrevivência permanecem ativas. Nestas células, uma via de sinalização centrada nas proteínas chamadas P-Rex1 e Rac1 foi fortemente ativada. Rac1 ajuda a controlar a forma e o movimento celular, e P-Rex1 é um de seus ativadores-chave. As células lentas e resistentes dependiam desse eixo para sua capacidade de migrar, e amostras de pacientes mostraram que os níveis de P-Rex1 eram altos em tumores positivos para receptor de estrogênio e em suas metástases, especialmente nos casos que recidivaram tardiamente.
Testando novas combinações de drogas
Como a via P-Rex1/Rac1 parecia um motor de movimentação e sobrevivência para essas células tolerantes, os pesquisadores testaram drogas que reduzem a atividade de Rac1. Em cultura, esses inibidores reduziram a formação de colônias e retardaram o fechamento tipo ferida pelas células resistentes lentas mais do que pelas rápidas. Em modelos de camundongo com sensores fluorescentes embutidos para a atividade de Rac1, dois compostos direcionados a Rac1 diminuíram visivelmente a sinalização de Rac1 dentro de tumores tratados com tamoxifeno. Em um modelo tumoral derivado de paciente, obtido de uma mulher cujo câncer já havia resistido a múltiplas terapias hormonais, os inibidores de Rac1 isoladamente desaceleraram modestamente o crescimento tumoral e prolongaram a sobrevivência. Quando combinados com tamoxifeno, no entanto, causaram encolhimento dos tumores e reduziram significativamente o peso tumoral final.
Pistas vindas de analgésicos do mundo real
Um dos agentes bloqueadores de Rac1, R-ketorolaco, é a imagem especular de um fármaco já usado para alívio da dor após cirurgia. A equipe realizou uma meta-análise de estudos clínicos anteriores que acompanharam desfechos do câncer de mama em pacientes que receberam ketorolaco ao redor do período cirúrgico. Nesses estudos, o uso de ketorolaco foi associado a um menor risco de recorrência do câncer, enquanto outros analgésicos sem atividade de bloqueio de Rac1 não mostraram esse padrão. Embora não constitua prova por si só, essa indicação em nível populacional apoia a ideia de que bloquear temporariamente Rac1 durante janelas de tratamento críticas pode reduzir a chance de que células tolerantes gerem metástases futuras.
O que isso significa para o futuro
Para um não especialista, a mensagem central é que a terapia hormonal pode, involuntariamente, remodelar algumas células de câncer de mama em viajantes de lenta divisão, porém altamente capazes. Este trabalho aponta a via P-Rex1/Rac1 como um botão de controle desse comportamento e mostra em animais que girar esse botão para baixo, especialmente em combinação com drogas hormonais padrão, pode encolher tumores resistentes. As descobertas ainda não se traduzem em um novo tratamento padrão, mas sugerem que acrescentar estratégias seguras de direcionamento de Rac1, possivelmente até adaptadas de analgésicos já existentes, poderia um dia ajudar a prevenir retornos tardios e ameaçadores à vida do câncer de mama dirigido por estrogênio.
Citação: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Palavras-chave: câncer de mama com receptor de estrogênio positivo, resistência à terapia endócrina, metástase, sinalização Rac1, P-Rex1