Clear Sky Science · tr
Hormonal tedaviyle yeniden programlanan meme kanseri, P-Rex1/Rac1 sinyallemesinin yukarı düzenlenmesiyle metastatik kaçışı kolaylaştırıyor
Bu araştırma hastalar için neden önemli
Meme kanserlerinin çoğu hormon östrojenle beslendiği için ameliyat sonrası yıllarca bu sinyali engelleyen ilaçlarla tedavi edilir. Buna rağmen, bu kanserlerin büyük bir kısmı tedavi bitmiş gibi görünse bile sessizce geri dönebilir. Bu çalışma, hormon bloke edici tedavinin bazı kanser hücrelerini yavaş büyüyen ama seyahat etmeye hazır bir duruma itebileceğini ortaya koyuyor ve belirli bir hücre hareket yolunu engellemenin bu geç ve ölümcül nüksleri önlemeye yardımcı olabileceğini gösteriyor. 
Yavaş ama tehlikeli kanser hücreleri
Hekimler, östrojen reseptörü pozitif bazı meme kanserlerinin ilk tedaviden on yıl veya daha uzun süre sonra geri döndüğünü uzun zamandır gözlemliyor. Bu geç nüksler genellikle yavaş büyür ancak yayıldıklarında tedavisi zordur. Hastalardan alınan dokuları inceleyerek araştırmacılar, östrojen kaynaklı tümörlerin metastazlarında genellikle orijinal meme tümörlerinden daha az aktif bölünen hücre bulunduğunu saptadı. Bu, geç yayılmanın ana iticilerinin sadece hızlı bölünen hücreler değil, yavaş büyüyen hücreler de olabileceğini düşündürdü.
Sessiz kaçışı modelleme
Bu sessiz kaçışçıları incelemek için ekip, laboratuvarda östrojene duyarlı meme kanseri hücrelerini standart hormon bloke edici ilaçlarla tedavi etti. Zamanla iki tür sağ kalan hücre ortaya çıktı: hızlı büyüyen dirençli hücreler ve yavaş bölünen ama ölmek istemeyen ikinci bir grup. Yavaş hücreler farelere implante edildiğinde, büyük, bozulmuş çekirdekler ve çevresinde yoğun kollajen gibi yaşlanmış veya strese girmiş hücreleri anımsatan özelliklerle daha küçük primer meme tümörleri oluşturdu. Orijinal bölgede yavaş büyümeye rağmen, bu hücreler akciğer ve kemiklere hızlı büyüyen hücreler kadar verimli şekilde yayıldı; bu da büyüme hızı ile yayılma kapasitesinin aynı şey olmadığını ortaya koydu. 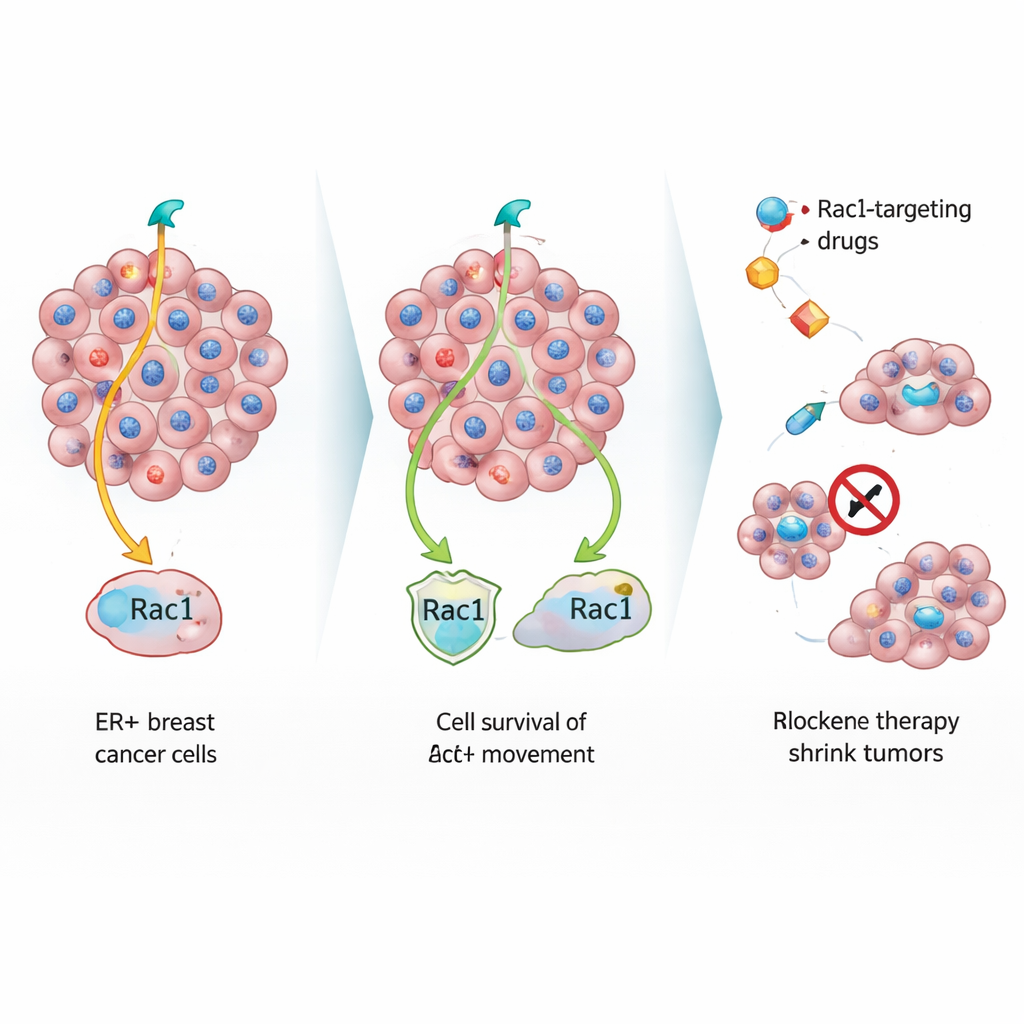
Tedaviyle açılan bir hareket anahtarı
Ekip daha sonra tek hücre RNA dizileme yöntemini kullanarak hormon tedavisinin bu sağ kalanları nasıl yeniden kabloladığını inceledi. Endokrin tedavisinin bir hücre alt kümesini senesans-benzeri bir duruma ittiğini; bu durumda bölünme yavaşlarken hayatta kalma yollarının aktif kaldığını buldular. Bu hücrelerde P-Rex1 ve Rac1 adlı proteinler merkezli bir sinyal yolunun güçlü şekilde artırıldığı görüldü. Rac1 hücre şekli ve hareketini kontrollemeye yardımcı olurken, P-Rex1 onun kilit aktivatörlerinden biridir. Yavaş dirençli hücreler bu eksene, göç kabiliyetleri için bağımlıydı ve hasta örnekleri P-Rex1 düzeylerinin östrojen reseptörü pozitif tümörlerde ve özellikle geç nüks gösteren olgulardaki metastazlarda yüksek olduğunu gösterdi.
Yeni ilaç kombinasyonlarını test etmek
P-Rex1/Rac1 yolu bu toleran hücreler için bir hareket ve hayatta kalma motoru gibi görününce, araştırmacılar Rac1 aktivitesini azaltan ilaçları test etti. Deney düzeneğinde bu inhibitörler, yavaş dirençli hücrelerin koloni oluşumunu azalttı ve yara kapama benzeri hareketleri hızlı hücrelere göre daha çok yavaşlattı. Rac1 aktivitesi için yerleşik floresan sensörlere sahip fare modellerinde, iki Rac1 hedefli bileşik tamoksifenle tedavi edilen tümörlerin içinde Rac1 sinyallemesini belirgin şekilde düşürdü. Bir kadından alınmış ve birden fazla hormon tedavisine direnç geliştirmiş hasta kaynaklı tümör modelinde, tek başına Rac1 inhibitörleri tümör büyümesini ılımlı olarak yavaşlattı ve sağkalımı uzattı. Ancak tamoksifen ile kombinasyon halinde, tümörlerin küçülmesine ve nihai tümör ağırlığında belirgin azalmaya yol açtılar.
Gerçek dünyadan ağrı kesicilerden ipuçları
Rac1’i engelleyen ajanlardan biri olan R-ketorolak, ameliyat sonrası ağrı giderimi için hâlihazırda kullanılan bir ilacın ayna görüntüsüdür. Ekip, cerrahi sırasında ketorolak alan hastalarda meme kanseri sonuçlarını izleyen önceki klinik çalışmaları meta-analizle değerlendirdi. Bu çalışmalarda ketorolak kullanımı kanser nüks riskinin daha düşük olmasıyla ilişkilendirildi; Rac1 hedeflemesi olmayan diğer ağrı kesiciler bu deseni göstermedi. Tek başına kesin kanıt olmasa da bu popülasyon düzeyindeki ipucu, kritik tedavi pencerelerinde geçici olarak Rac1’i bloke etmenin toleran hücrelerin gelecekte metastaz tohumu atma olasılığını azaltabileceği fikrini destekliyor.
Gelecek için anlamı
Bir uzman olmayan için merkezi mesaj şudur: hormon terapisi bazı meme kanseri hücrelerini istemeden yavaş bölünen ama yüksek derecede seyahat yeteneğine sahip hücrelere dönüştürebilir. Bu çalışma bu davranışın kontrol düğmesini P-Rex1/Rac1 yolunda işaretliyor ve hayvan çalışmalarında bu düğmeyi kısmak —özellikle standart hormon ilaçlarıyla birlikte— dirençli tümörleri küçültebiliyor. Bulgular henüz yeni bir standart tedaviye dönüşmüş değil, ama güvenli Rac1 hedefleme stratejilerinin, hatta mevcut bazı ağrı kesicilerden uyarlanabileceklerin, bir gün östrojen kaynaklı meme kanserinin geç ve yaşamı tehdit eden nükslerini önlemeye yardımcı olabileceğini öne sürüyor.
Atıf: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Anahtar kelimeler: östrojen reseptörü pozitif meme kanseri, endokrin terapi direnci, metastaz, Rac1 sinyallemesi, P-Rex1