Clear Sky Science · de
Endokrine Therapie führt bei Brustkrebs zu Reprogrammierung, die metastatische Flucht durch Hochregulierung der P-Rex1/Rac1‑Signalgebung erleichtert
Warum diese Forschung für Patientinnen wichtig ist
Viele Brustkrebserkrankungen werden vom Hormon Östrogen angetrieben und über Jahre nach der Operation mit Medikamenten behandelt, die dieses Signal blockieren. Trotzdem kann ein großer Teil dieser Tumoren lange nach scheinbarem Abschluss der Behandlung still zurückkehren. Diese Studie zeigt, wie hormonblockierende Therapien einige Krebszellen in einen langsam wachsenden, aber reisefähigen Zustand drängen können, und dass die Blockade eines bestimmten Zellbewegungswegs helfen könnte, diese späten, lebensgefährlichen Rückfälle zu verhindern. 
Langsame, aber gefährliche Krebszellen
Ärztinnen und Ärzte beobachten seit Langem, dass einige östrogenrezeptorpositive Brustkrebserkrankungen ein Jahrzehnt oder länger nach der Erstbehandlung wieder auftreten. Diese späten Rezidive wachsen oft langsam, sind aber schwer heilbar, sobald sie gestreut haben. Beim Vergleich von Patientenproben fanden die Forschenden, dass Metastasen von östrogengetriebenen Tumoren häufig weniger aktiv teilende Zellen enthielten als die ursprünglichen Brusttumoren. Das deutet darauf hin, dass langsam wachsende Zellen, nicht nur schnell teilende, entscheidende Treiber der späten Ausbreitung sein können.
Ein Modell für leise Fluchtmechanismen
Um diese stillen Fluchtkünstler zu untersuchen, behandelte das Team im Labor östrogensensible Brustkrebszellen mit üblichen hormonblockierenden Medikamenten. Mit der Zeit tauchten zwei Arten von Überlebenden auf: schnell wachsende, resistente Zellen und eine zweite Gruppe, die langsam teilte, aber nicht zugrunde ging. Wurden die langsameren Zellen in Mäuse implantiert, bildeten sie kleinere primäre Brusttumoren mit Merkmalen, die gealterten oder gestressten Zellen ähneln, darunter große, verzerrte Zellkerne und dichte Kollagenablagerungen. Trotz dieses trägen Wachstums am Ursprungsort verbreiteten sich diese Zellen in Lunge und Knochen genauso effizient wie die schnell wachsenden Zellen, was zeigt, dass Wachstumsgeschwindigkeit und Ausbreitung nicht dasselbe sind. 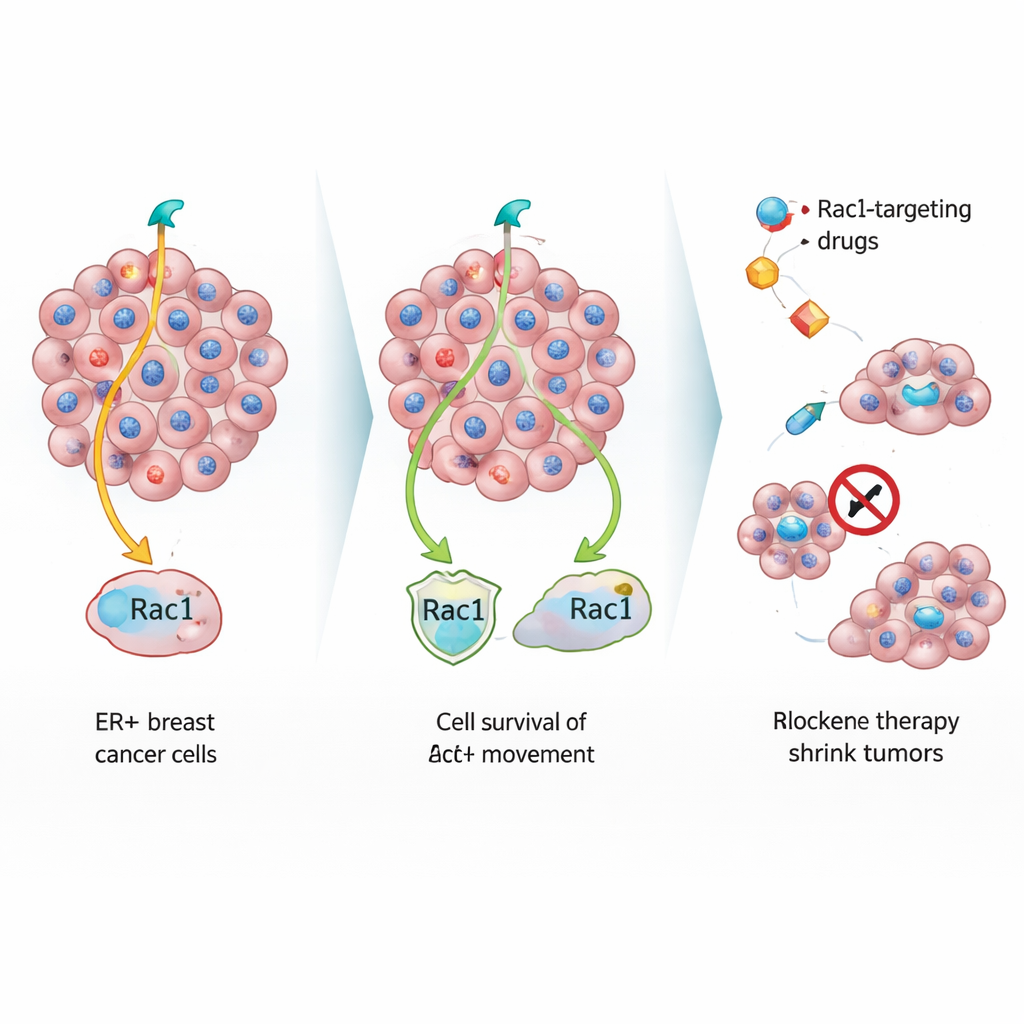
Ein durch Behandlung umgeschalteter Bewegungsmechanismus
Das Team nutzte dann Einzelzell‑RNA‑Sequenzierung, eine Methode, die die Aktivität tausender Gene in einzelnen Zellen erfasst, um zu sehen, wie die Hormontherapie diese Überlebenden umprogrammiert. Sie stellten fest, dass die endokrine Behandlung eine Untergruppe von Zellen in einen seneszenzähnlichen Zustand drängte, in dem die Teilung verlangsamt ist, Überlebenswege jedoch aktiv bleiben. In diesen Zellen war ein Signalweg um die Proteine P‑Rex1 und Rac1 stark hochreguliert. Rac1 steuert Zellform und Bewegung, und P‑Rex1 ist einer seiner zentralen Aktivatoren. Die langsam resistenten Zellen waren auf diese Achse angewiesen, um zu migrieren, und Patientenproben zeigten erhöhte P‑Rex1‑Spiegel in östrogenrezeptorpositiven Tumoren und ihren Metastasen, insbesondere bei Fällen mit später Wiederkehr.
Testen neuer Medikamentenkombinationen
Da die P‑Rex1/Rac1‑Achse wie ein Motor für Bewegung und Überleben dieser toleranten Zellen wirkte, prüften die Forschenden Wirkstoffe, die Rac1‑Aktivität dämpfen. In Zellkulturen reduzierten diese Inhibitoren die Koloniebildung und verlangsamten die Wundverschluss‑ähnliche Migration der langsamen resistenten Zellen stärker als bei den schnellen Zellen. In Mausmodellen mit eingebauten Fluoreszenzsensoren für Rac1‑Aktivität senkten zwei Rac1‑gerichtete Verbindungen sichtbar das Rac1‑Signal in tamoxifenbehandelten Tumoren. In einem patientenabgeleiteten Tumormodell, gewonnen von einer Frau, deren Krebs bereits gegenüber mehreren Hormontherapien resistent war, verlangsamten Rac1‑Inhibitoren allein das Tumorwachstum nur mäßig und verlängerten das Überleben. In Kombination mit Tamoxifen jedoch schrumpften die Tumoren und das Endtumorgewicht wurde deutlich reduziert.
Anhaltspunkte aus realen Schmerzmitteln
Einer der Rac1‑blockierenden Wirkstoffe, R‑Ketorolac, ist das Spiegelbild eines Medikaments, das bereits zur Schmerzlinderung nach Operationen eingesetzt wird. Das Team führte eine Metaanalyse früherer klinischer Studien durch, die Brustkrebs‑Ergebnisse bei Patientinnen verfolgten, die perioperativ Ketorolac erhielten. In diesen Studien war die Anwendung von Ketorolac mit einem geringeren Risiko für Krebsrückfälle verbunden, während andere Schmerzmittel ohne Rac1‑hemmende Aktivität dieses Muster nicht zeigten. Obwohl das kein schlüssiger Beweis für sich ist, stützt dieser bevölkerungsbezogene Hinweis die Idee, dass eine vorübergehende Blockade von Rac1 in wichtigen Behandlungsphasen die Wahrscheinlichkeit verringern könnte, dass tolerante Zellen zukünftige Metastasen aussäen.
Was das für die Zukunft bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Hormontherapie kann unbeabsichtigt einige Brustkrebszellen in langsam teilende, aber ausgesprochen reisefähige Zustände umformen. Diese Arbeit identifiziert die P‑Rex1/Rac1‑Achse als Stellschraube für dieses Verhalten und zeigt in Tiermodellen, dass das Absenken dieser Stellschraube, vor allem in Kombination mit Standardhormonmedikamenten, resistente Tumoren verkleinern kann. Die Ergebnisse führen noch nicht zu einem neuen Standardbehandlungsprotokoll, deuten aber darauf hin, dass das Hinzufügen sicherer Rac1‑gezielter Strategien, möglicherweise sogar adaptiert aus existierenden Schmerzmitteln, eines Tages helfen könnte, späte, lebensbedrohliche Rückfälle von östrogengetriebenem Brustkrebs zu verhindern.
Zitation: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Schlüsselwörter: östrogenrezeptorpositiver Brustkrebs, Resistenz gegen endokrine Therapie, Metastasen, Rac1‑Signalgebung, P-Rex1