Clear Sky Science · fr
La thérapie endocrinienne reprogramme le cancer du sein et facilite l’évasion métastatique via l’augmentation du signal P-Rex1/Rac1
Pourquoi cette recherche est importante pour les patients
De nombreux cancers du sein sont alimentés par l’hormone œstrogène et sont traités par des médicaments qui bloquent ce signal pendant des années après la chirurgie. Pourtant, une grande proportion de ces cancers peut réapparaître discrètement longtemps après la fin apparente du traitement. Cette étude révèle comment la thérapie anti-hormonale peut pousser certaines cellules cancéreuses dans un état à croissance lente mais prêtes à migrer, et montre que bloquer une voie cellulaire spécifique de mobilité pourrait aider à prévenir ces récidives tardives et mortelles. 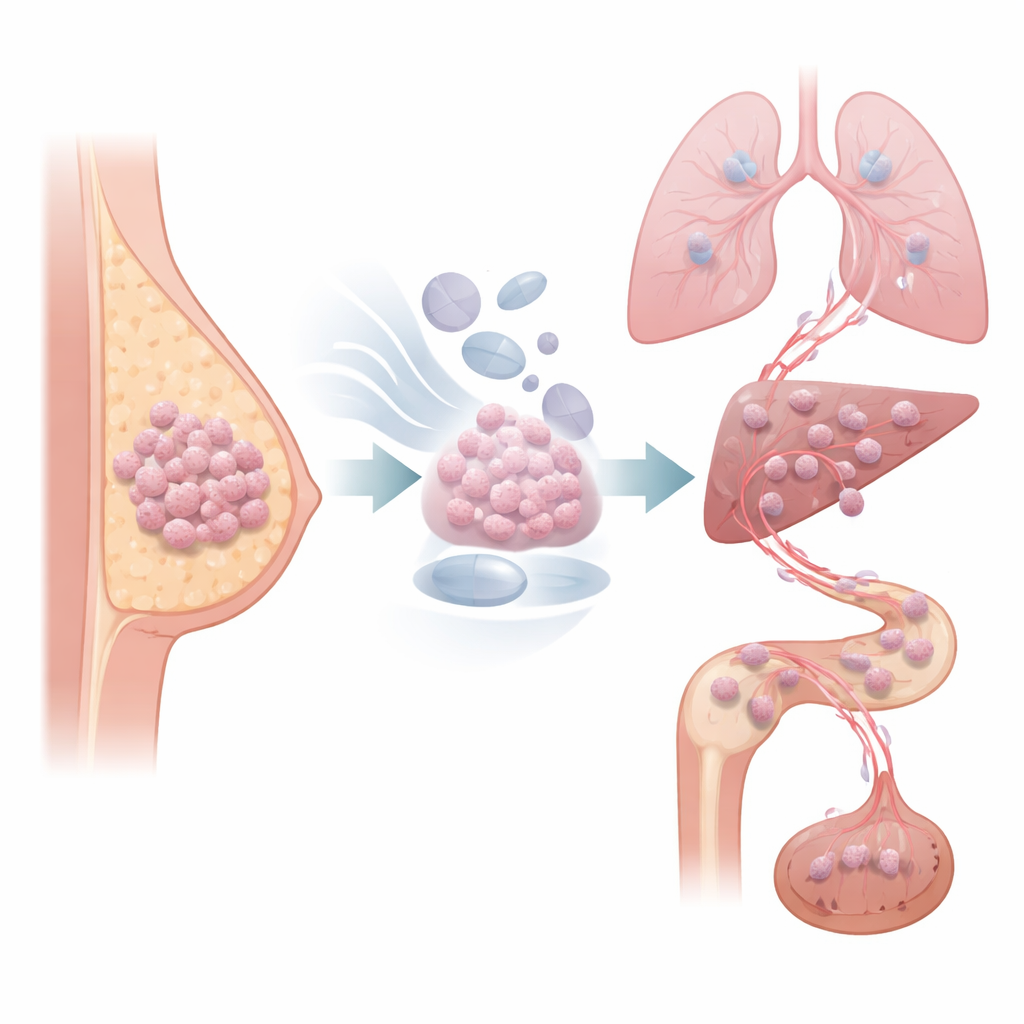
Des cellules lentes mais dangereuses
Les cliniciens observent depuis longtemps que certains cancers du sein récepteurs d’œstrogène positifs réapparaissent dix ans ou plus après le traitement initial. Ces récidives tardives croissent souvent lentement mais sont difficiles à guérir une fois disséminées. En examinant des tissus de patientes, les chercheurs ont constaté que les métastases issues de tumeurs dépendantes des œstrogènes contenaient fréquemment moins de cellules en division active que la tumeur mammaire d’origine. Cela suggère que des cellules à croissance lente, et pas seulement celles qui divisent rapidement, peuvent être des moteurs clés de la dissémination tardive.
Construire un modèle d’évasion silencieuse
Pour étudier ces artistess de l’évasion silencieuse, l’équipe a exposé en laboratoire des cellules de cancer du sein sensibles aux œstrogènes aux traitements anti-hormonaux standards. Avec le temps, deux types de survivantes sont apparues : des cellules résistantes à croissance rapide et un second groupe qui se divisait lentement mais refusait de mourir. Quand les cellules plus lentes furent implantées chez la souris, elles ont formé des tumeurs mammaires primaires plus petites présentant des caractéristiques rappelant des cellules âgées ou stressées, y compris de gros noyaux déformés et un collagène dense autour d’elles. Malgré cette croissance lente sur le site d’origine, ces cellules ont colonisé les poumons et les os aussi efficacement que les cellules à croissance rapide, révélant que vitesse de croissance et capacité de dissémination sont distinctes. 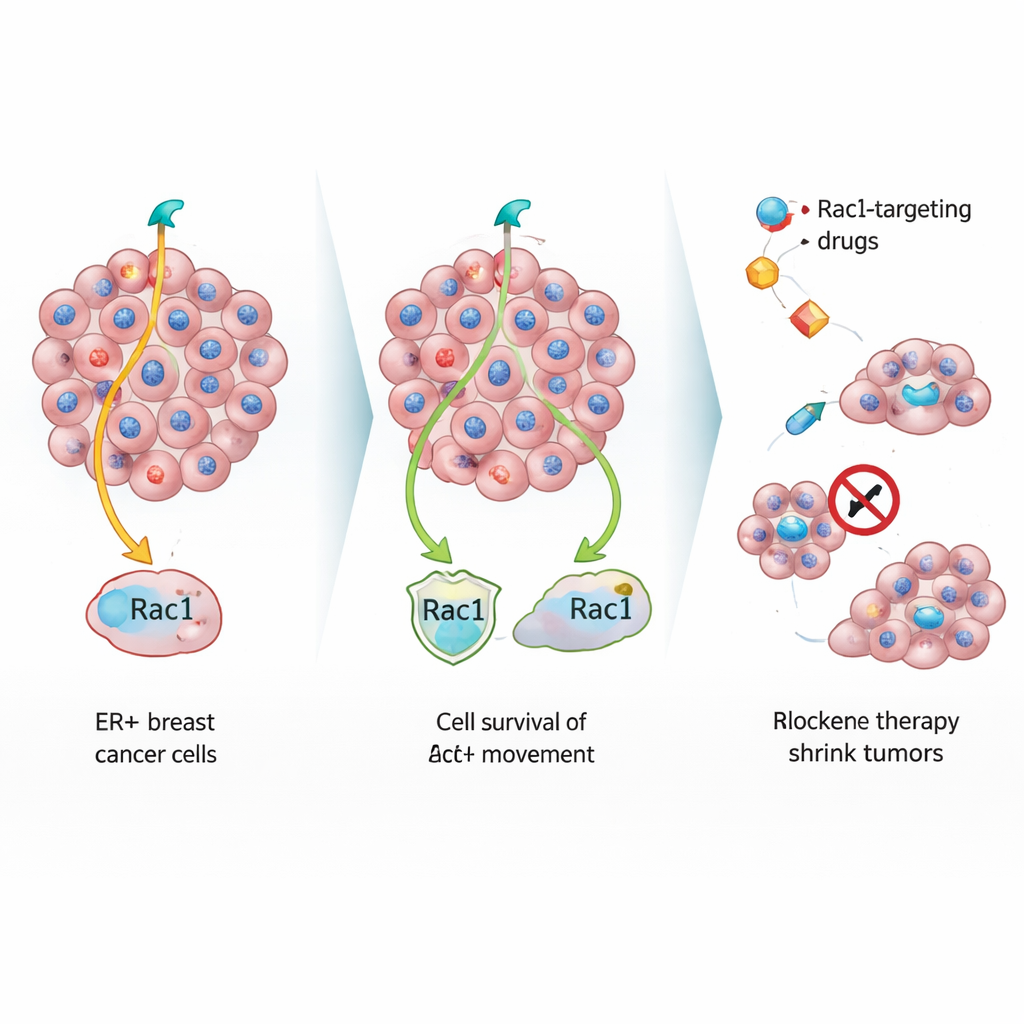
Un interrupteur de mobilité actionné par le traitement
L’équipe a ensuite utilisé le séquençage ARN unicellulaire, une technique qui lit l’activité de milliers de gènes dans des cellules individuelles, pour voir comment la thérapie hormonale reprogramm(ait) ces survivantes. Ils ont découvert que le traitement endocrinien poussait un sous-ensemble de cellules vers un état ressemblant à la sénescence, où la division ralentit mais les voies de survie restent actives. Dans ces cellules, une voie de signalisation centrée sur les protéines P-Rex1 et Rac1 était fortement activée. Rac1 aide à contrôler la forme et le mouvement cellulaire, et P-Rex1 en est un des activateurs clés. Les cellules lentes et résistantes dépendaient de cet axe pour leur capacité à migrer, et des échantillons de patientes montraient des niveaux élevés de P-Rex1 dans les tumeurs ER+ et leurs métastases, en particulier dans les cas de récidive tardive.
Tester de nouvelles combinaisons médicamenteuses
Parce que la voie P-Rex1/Rac1 ressemblait à un moteur de mobilité et de survie pour ces cellules tolérantes, les chercheurs ont testé des médicaments qui atténuent l’activité de Rac1. In vitro, ces inhibiteurs ont réduit la formation de colonies et ralenti la fermeture de lésions simulées par les cellules lentes résistantes plus que par les cellules rapides. Dans des modèles murins équipés de capteurs fluorescents de l’activité de Rac1, deux composés ciblant Rac1 ont visiblement réduit la signalisation Rac1 au sein de tumeurs traitées par tamoxifène. Dans un modèle tumoral dérivé d’une patiente dont le cancer avait déjà résisté à plusieurs thérapies hormonales, les inhibiteurs de Rac1 seuls ont modestement ralenti la progression tumorale et prolongé la survie. En combinaison avec le tamoxifène, toutefois, ils ont provoqué une régression tumorale et réduit significativement le poids final des tumeurs.
Indices venant d’analgésiques du monde réel
Un des agents bloquant Rac1, le R-kétorolac, est l’image miroir d’un médicament déjà utilisé pour le soulagement de la douleur après chirurgie. L’équipe a réalisé une méta-analyse d’études cliniques antérieures suivant l’issue des cancers du sein chez des patientes ayant reçu du kétorolac autour du moment de la chirurgie. Dans ces études, l’utilisation du kétorolac était associée à un risque plus faible de récidive, tandis que d’autres analgésiques sans activité ciblant Rac1 ne montraient pas ce schéma. Bien que cela ne constitue pas une preuve à lui seul, ce signal au niveau de la population soutient l’idée que bloquer temporairement Rac1 pendant des fenêtres thérapeutiques clés pourrait réduire la probabilité que des cellules tolérantes engendrent des métastases futures.
Ce que cela signifie pour l’avenir
Pour un non-spécialiste, le message central est que la thérapie hormonale peut involontairement remodeler certaines cellules du cancer du sein en cellules à division lente mais fortement capables de voyager. Ce travail identifie la voie P-Rex1/Rac1 comme un bouton de contrôle de ce comportement et montre chez l’animal que tourner ce bouton vers le bas, en particulier en association avec les traitements hormonaux standards, peut réduire des tumeurs résistantes. Ces résultats ne constituent pas encore un nouveau traitement standard, mais ils suggèrent que l’ajout de stratégies sûres ciblant Rac1, éventuellement adaptées à partir d’analgésiques existants, pourrait un jour aider à prévenir les récidives tardives et mortelles des cancers du sein dépendants des œstrogènes.
Citation: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Mots-clés: cancer du sein à récepteur d’œstrogène positif, résistance à la thérapie endocrinienne, métastase, signalisation Rac1, P-Rex1