Clear Sky Science · pl
Reprogramowanie raka piersi przez terapię hormonalną ułatwia ucieczkę do przerzutów poprzez nasilanie sygnalizacji P-Rex1/Rac1
Dlaczego to badanie ma znaczenie dla pacjentów
Wiele raków piersi jest napędzanych przez hormon estrogen i leczonych lekami blokującymi ten sygnał przez wiele lat po operacji. Mimo to duża część tych nowotworów może cicho powracać długo po zakończeniu leczenia. Badanie to ujawnia, w jaki sposób terapia blokująca hormony może przekształcić niektóre komórki nowotworowe w stan wolnego wzrostu, ale gotowości do rozprzestrzeniania, i pokazuje, że zablokowanie określonej ścieżki kontrolującej ruch komórek może pomóc zatrzymać te późne, śmiertelne nawroty. 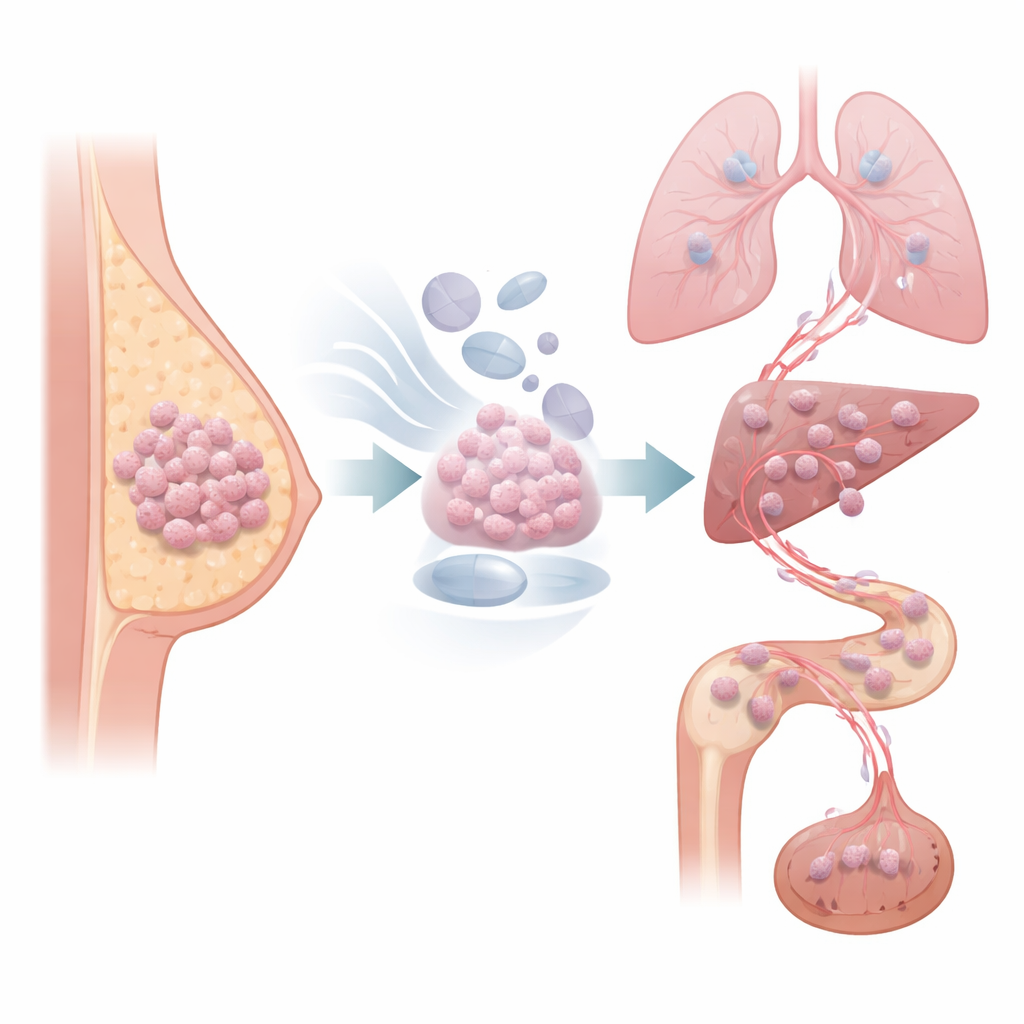
Wolne, lecz niebezpieczne komórki nowotworowe
Lekarze od dawna obserwują, że niektóre nowotwory piersi z receptorem estrogenowym wracają po dekadzie lub więcej od początkowego leczenia. Te późne nawroty często rosną powoli, ale są trudne do wyleczenia po rozsianiu. Analiza tkanki od pacjentów wykazała, że przerzuty z guzów napędzanych estrogenem często zawierały mniej komórek aktywnie dzielących się niż pierwotne guzy piersi. Sugeruje to, że kluczową rolę w późnym rozsiewie mogą odgrywać komórki wolno rosnące, a nie tylko szybko dzielące się.
Budowa modelu cichej ucieczki
Aby zbadać tych „cichych” uciekinierów, zespół poddał wrażliwe na estrogen komórki raka piersi standardowym lekom blokującym hormony w warunkach laboratoryjnych. Z czasem pojawiły się dwie grupy ocalałych: szybko rosnące, oporne komórki oraz druga grupa dzieląca się wolno, lecz niepoddająca się śmierci. Gdy wolniejsze komórki wszczepiono myszom, tworzyły mniejsze pierwotne guzy piersi z cechami przypominającymi komórki stare lub zestresowane, w tym dużymi, zniekształconymi jądrami i gęstym kolagenem wokół nich. Pomimo ospałego wzrostu w miejscu pierwotnym, komórki te rozprzestrzeniały się do płuc i kości równie skutecznie jak komórki szybko rosnące, co ujawnia, że tempo wzrostu i zdolność do rozsiewu to odrębne właściwości.
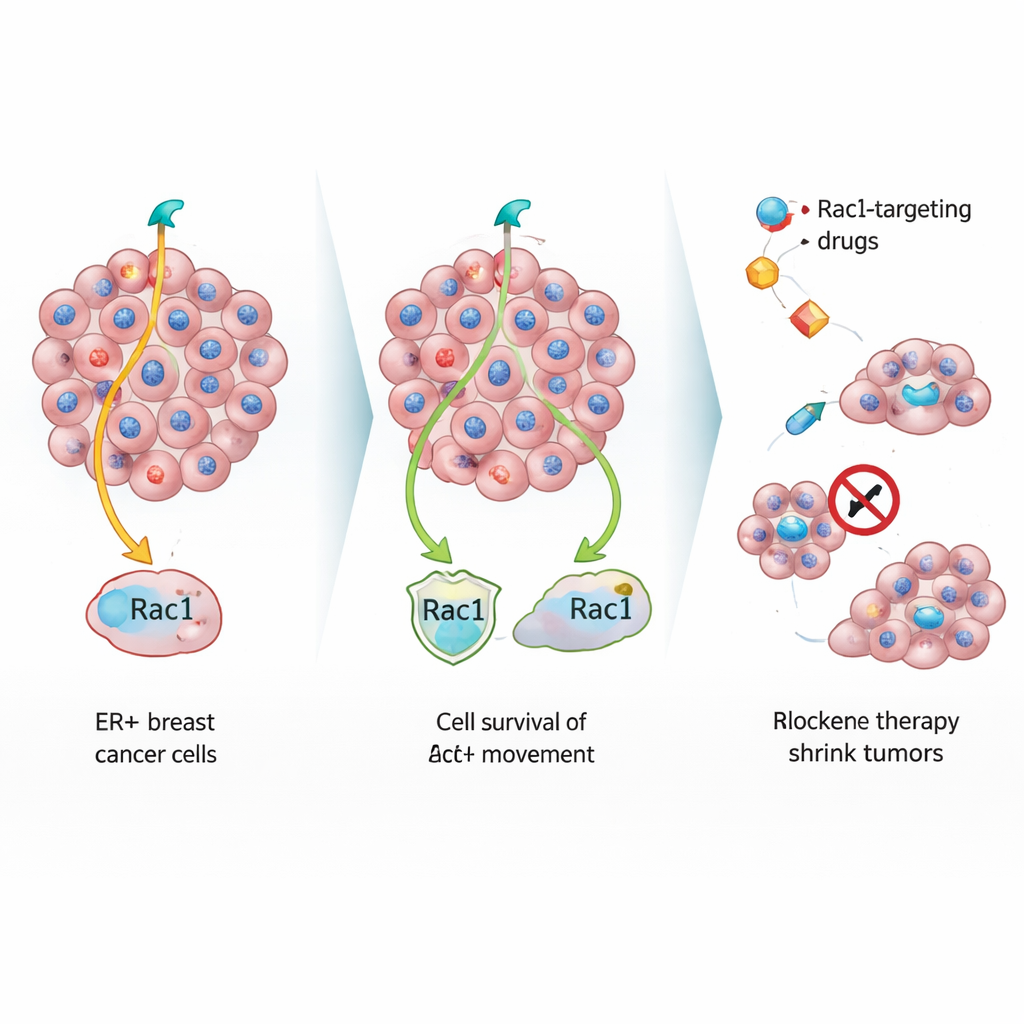
Przełącznik ruchu włączony przez leczenie
Zespół następnie zastosował sekwencjonowanie RNA pojedynczych komórek, technikę czytającą aktywność tysięcy genów w pojedynczych komórkach, aby zobaczyć, jak terapia hormonalna przeprogramowuje tych ocalałych. Odkryli, że leczenie endokrynologiczne wprowadza podzbiór komórek w stan podobny do starzenia komórkowego (senescencji), gdzie podziały zwalniają, ale szlaki przetrwania pozostają aktywne. W tych komórkach silnie nasiliła się ścieżka sygnalizacyjna skoncentrowana wokół białek P-Rex1 i Rac1. Rac1 kontroluje kształt i ruch komórek, a P-Rex1 jest jednym z jego kluczowych aktywatorów. Wolne, oporne komórki polegały na tej osi w kwestii zdolności do migracji, a próbki pacjentów wykazały wysokie poziomy P-Rex1 w nowotworach z receptorem estrogenowym i ich przerzutach, szczególnie w przypadkach nawrotów późnych.
Testowanie nowych kombinacji leków
Ponieważ szlak P-Rex1/Rac1 wyglądał na napęd ruchu i przetrwania tych tolerancyjnych komórek, badacze przetestowali leki tłumiące aktywność Rac1. W hodowlach te inhibitory zmniejszały formowanie kolonii i spowalniały zamykanie się „zranień” przez wolne, oporne komórki bardziej niż przez komórki szybkie. W modelach mysich wyposażonych w fluorescencyjne sensory aktywności Rac1, dwa związki ukierunkowane na Rac1 widocznie obniżały sygnalizację Rac1 w guzach leczonych tamoksyfenem. W modelu guza pochodzącym od pacjentki, której rak był już oporny na wielokrotną terapię hormonalną, inhibitory Rac1 same w sobie umiarkowanie spowolniły wzrost guza i wydłużyły przeżycie. W połączeniu z tamoksyfenem powodowały jednak kurczenie się guzów i znacząco zmniejszały ostateczną masę guza.
Wskazówki z leków przeciwbólowych stosowanych w praktyce
Jednym z czynników blokujących Rac1 jest R-ketorolak, enancjomer leku już stosowanego w łagodzeniu bólu po zabiegach chirurgicznych. Zespół przeprowadził metaanalizę wcześniejszych badań klinicznych śledzących wyniki u pacjentek, które otrzymały ketorolak w okresie okołozabiegowym. W tych badaniach stosowanie ketorolaku wiązało się z niższym ryzykiem nawrotu choroby, podczas gdy inne leki przeciwbólowe bez aktywności wobec Rac1 nie wykazywały takiego związku. Chociaż samo w sobie nie jest to dowód, ten populacyjny sygnał wspiera hipotezę, że czasowe zablokowanie Rac1 w krytycznych oknach terapeutycznych może zmniejszyć szansę, że tolerancyjne komórki zasieją przyszłe przerzuty.
Co to oznacza na przyszłość
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że terapia hormonalna może niezamierzenie przekształcić część komórek raka piersi w wolno dzielących się, ale wysoce zdolnych do podróży „wędrowców”. Praca ta identyfikuje ścieżkę P-Rex1/Rac1 jako pokrętło kontrolne tego zachowania i pokazuje na zwierzętach, że przygłuszenie tego pokrętła, zwłaszcza w połączeniu ze standardowymi lekami hormonalnymi, może zmniejszać oporne guzy. Wyniki te nie przekładają się jeszcze na nowy standard leczenia, ale sugerują, że dodanie bezpiecznych strategii ukierunkowanych na Rac1, być może nawet adaptowanych z istniejących leków przeciwbólowych, mogłoby pewnego dnia pomóc zapobiegać późnym, zagrażającym życiu nawrotom raka piersi napędzanego estrogenem.
Cytowanie: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Słowa kluczowe: rak piersi z receptorem estrogenowym, oporność na terapię endokrynologiczną, przerzuty, sygnalizacja Rac1, P-Rex1