Clear Sky Science · es
La terapia endocrina reprograma el cáncer de mama y facilita la fuga metastásica mediante la activación de la vía P-Rex1/Rac1
Por qué esta investigación importa para los pacientes
Muchos cánceres de mama se alimentan de la hormona estrógeno y se tratan con fármacos que bloquean esa señal durante años tras la cirugía. Aun así, una gran proporción de estos cánceres pueden regresar silenciosamente mucho después de que el tratamiento parezca haber terminado. Este estudio revela cómo la terapia anti‑hormonal puede empujar a algunas células tumorales hacia un estado de crecimiento lento pero listas para desplazarse, y muestra que bloquear una vía celular específica de movimiento podría ayudar a detener estas recaídas tardías y letales. 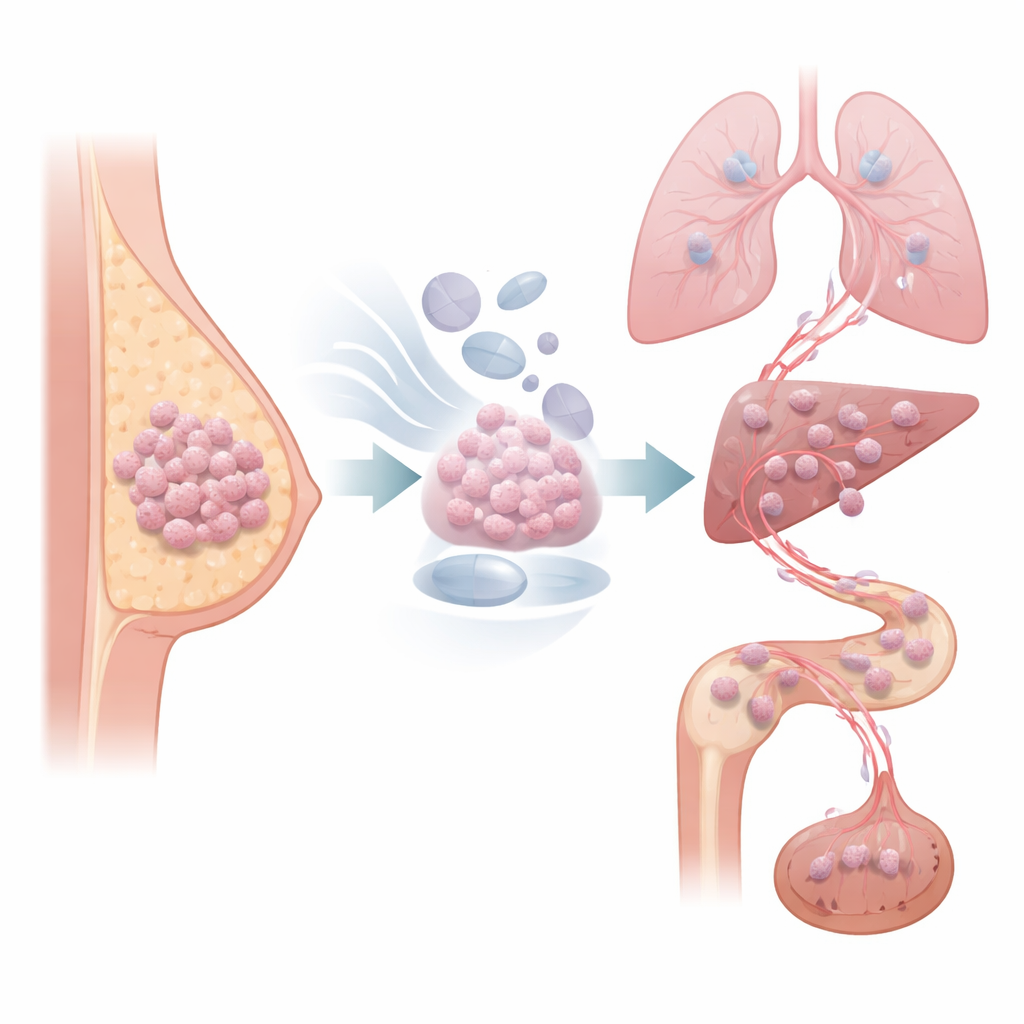
Células cancerosas lentas pero peligrosas
Los médicos llevan tiempo observando que algunos cánceres de mama con receptor de estrógeno positivo reaparecen una década o más después del tratamiento inicial. Estas recurrencias tardías con frecuencia crecen despacio pero son difíciles de curar una vez que se han diseminado. Al examinar tejidos de pacientes, los investigadores encontraron que las metástasis de tumores impulsados por estrógeno contenían con frecuencia menos células en división activa que los tumores mamarios originales. Esto sugiere que las células de crecimiento lento, y no solo las de división rápida, podrían ser impulsoras clave de la diseminación tardía.
Construyendo un modelo de escape silencioso
Para estudiar a estos «artistas del escape» silenciosos, el equipo trató en el laboratorio células de cáncer de mama sensibles al estrógeno con fármacos estándar que bloquean las hormonas. Con el tiempo, surgieron dos tipos de supervivientes: células resistentes de crecimiento rápido y un segundo grupo que se dividía lentamente pero se negaba a morir. Cuando las células más lentas se implantaron en ratones, formaron tumores mamarios primarios más pequeños con rasgos semejantes a células envejecidas o estresadas, incluyendo núcleos grandes y deformados y colágeno denso a su alrededor. A pesar de ese crecimiento lánguido en el sitio primario, estas células se diseminaron a pulmón y hueso con la misma eficiencia que las células de crecimiento rápido, revelando que velocidad de crecimiento y capacidad de diseminación no son lo mismo. 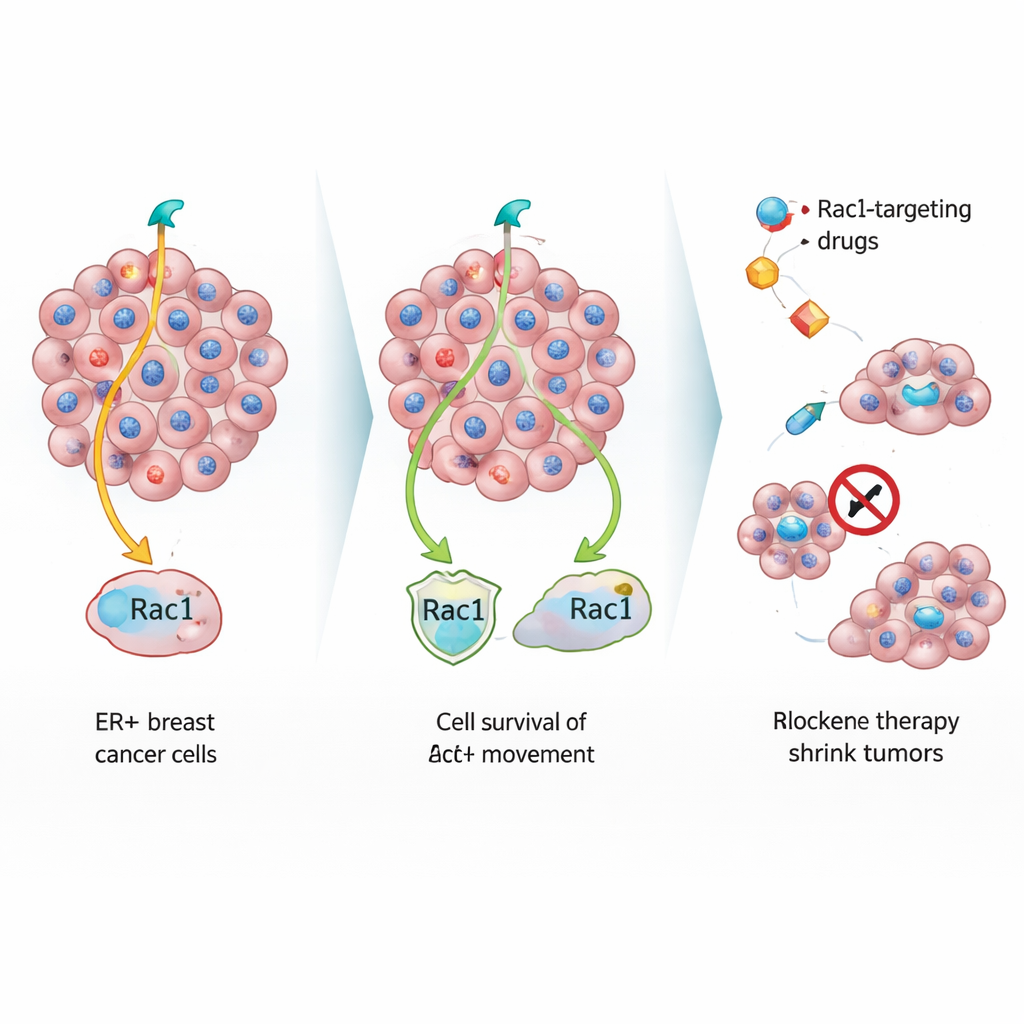
Un interruptor de movimiento activado por el tratamiento
El equipo usó entonces secuenciación de ARN a célula única, una técnica que lee la actividad de miles de genes en células individuales, para ver cómo la terapia hormonal estaba reconfigurando a estos supervivientes. Descubrieron que el tratamiento endocrino empujó a un subconjunto de células hacia un estado parecido a la senescencia, donde la división se ralentiza pero las vías de supervivencia permanecen activas. En estas células, una ruta de señalización centrada en las proteínas P-Rex1 y Rac1 estaba fuertemente activada. Rac1 ayuda a controlar la forma y el movimiento celular, y P-Rex1 es uno de sus activadores clave. Las células resistentes y lentas dependían de este eje para su capacidad de migrar, y las muestras de pacientes mostraron niveles altos de P-Rex1 en tumores con receptor de estrógeno y en sus metástasis, especialmente en los casos con recurrencia tardía.
Probando nuevas combinaciones de fármacos
Como la vía P-Rex1/Rac1 parecía un motor de movimiento y supervivencia para estas células tolerantes, los investigadores probaron fármacos que atenúan la actividad de Rac1. En cultivos, estos inhibidores redujeron la formación de colonias y ralentizaron el cierre tipo herida por parte de las células resistentes lentas más que en las rápidas. En modelos murinos con sensores fluorescentes incorporados para la actividad de Rac1, dos compuestos dirigidos a Rac1 disminuyeron de forma visible la señalización de Rac1 dentro de tumores tratados con tamoxifeno. En un modelo tumoral derivado de un paciente, tomado de una mujer cuyo cáncer ya había resistido múltiples terapias hormonales, los inhibidores de Rac1 por sí solos ralentizaron modestamente el crecimiento tumoral y prolongaron la supervivencia. Sin embargo, cuando se combinaron con tamoxifeno, provocaron la reducción de los tumores y disminuyeron de forma significativa el peso tumoral final.
Pistas desde analgésicos usados en la práctica clínica
Uno de los agentes bloqueadores de Rac1, R‑ketorolaco, es la imagen especular de un fármaco ya utilizado para aliviar el dolor tras la cirugía. El equipo realizó un metaanálisis de estudios clínicos previos que rastrearon los resultados del cáncer de mama en pacientes que recibieron ketorolaco alrededor del momento de la cirugía. En esos estudios, el uso de ketorolaco se asoció con un menor riesgo de recurrencia del cáncer, mientras que otros analgésicos sin actividad sobre Rac1 no mostraron ese patrón. Aunque no es una prueba concluyente por sí sola, esta pista a nivel poblacional respalda la idea de que bloquear temporalmente Rac1 durante ventanas clave del tratamiento podría reducir la probabilidad de que células tolerantes siembren metástasis futuras.
Qué significa esto para el futuro
Para el público general, el mensaje central es que la terapia hormonal puede reconfigurar involuntariamente algunas células de cáncer de mama en células de baja división pero muy capaces de viajar. Este trabajo identifica la vía P-Rex1/Rac1 como un regulador de ese comportamiento y demuestra en animales que bajar la actividad de esa vía, especialmente en combinación con fármacos hormonales estándar, puede reducir tumores resistentes. Los hallazgos todavía no se traducen en un nuevo estándar terapéutico, pero sugieren que añadir estrategias seguras para apuntar a Rac1, posiblemente incluso adaptadas de analgésicos existentes, podría algún día ayudar a prevenir las recurrencias tardías y potencialmente mortales del cáncer de mama impulsado por estrógeno.
Cita: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
Palabras clave: cáncer de mama con receptor de estrógeno positivo, resistencia a la terapia endocrina, metástasis, señalización Rac1, P-Rex1