Clear Sky Science · zh
从人多能干细胞衍生的胰腺前体高效控制嗜铬细胞样细胞与胰岛分化的平衡
将干细胞变成定制的胰岛素工厂
对于1型糖尿病患者,替换已丧失的产胰岛素细胞未来可能让他们摆脱胰岛素注射。科学家已经能诱导人类干细胞形成类似体内胰岛素“工厂”的微型胰腺簇,但这些实验室生长的“胰岛”往往包含杂类细胞:除期望的产胰岛素细胞外,常常出现不需要的细胞类型。本文研究了一个对未来治疗具有重大意义的实用问题:我们能否可靠地引导干细胞朝向理想的胰腺细胞谱系,同时限制离靶细胞的出现?
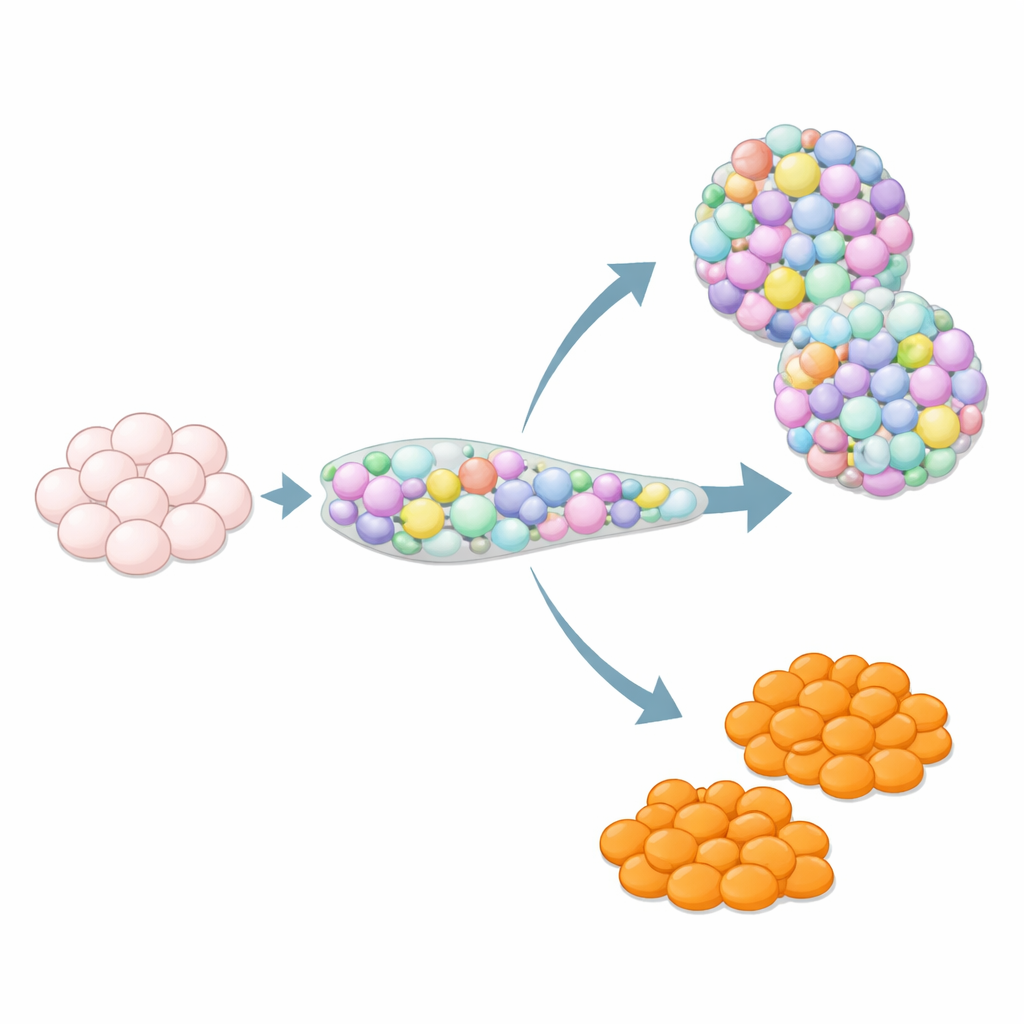
为何额外的细胞类型可能是隐患
当干细胞被引导分化为胰腺组织时,它们并不总是按剧本走。出现的“惊喜”中包括类似嗜铬细胞(enterochromaffin cells)的细胞,这是一类罕见的肠道细胞,正常存在于胃肠道并通过释放血清素参与肠道运动和信号传递。在干细胞衍生的胰岛中,这类嗜铬样细胞经常出现,尽管它们并不属于正常的人类胰岛。它们对胰岛功能和安全性的影响尚不明确,因此许多研究者把它们视为污染物。与此同时,由于真正的肠类类器官常常难以生成足量的嗜铬细胞,这些胰腺来源的离靶细胞若能被控制出现时机,也可能成为研究肠道生物学的宝贵资源。
打造更好的起始点
作者首先改进了将人类多能干细胞诱导为“原条”(primitive streak)再到明确内胚层(definitive endoderm)的早期步骤,明确内胚层是将来形成胰腺及其他器官的组织。他们发现,短暂用一种名为latrunculin A的化合物扰动细胞的内骨架,可以使这一最初的转变更为稳健,尤其在通常响应较差的高密度培养中效果显著。该调整产生了更均一的早期内胚层,进而形成更多的胰腺前体和类似胰岛β细胞的产胰岛素细胞。重要的是,同样的早期微调也改善了其他内胚层来源谱系(如肺和间叶系细胞)的形成,提示这是一种可广泛应用以减少干细胞分化变异性的方法。
掌舵命运:胰腺谱系与肠样细胞之争
在获得更稳健的胰腺前体起始群体后,研究组系统地测试了后期不同信号分子的组合,观察它们如何影响最终分泌细胞类型的构成。有些处理(包括抑制MAPK/ERK和BMP通路)强烈推动前体向嗜铬样细胞分化,而另一些处理(如生长因子FGF2、betacellulin和BMP4)则抑制这些细胞,转而有利于经典的胰腺细胞类型,如α、β和δ细胞。他们还表明,单纯早期提高一个已知的胰腺标志物NKX6-1不足以阻止嗜铬样细胞的出现。相反,最终结果取决于早期模式化(前体如何被预设)与后期模式化(在内分泌承诺阶段所接受的信号)之间的相互作用。通过混合搭配这些步骤,研究者们设计出不同配方,既能得到富含β细胞且具备强烈葡萄糖刺激胰岛素分泌的类胰岛簇,也能得到高度富集嗜铬样细胞的簇。
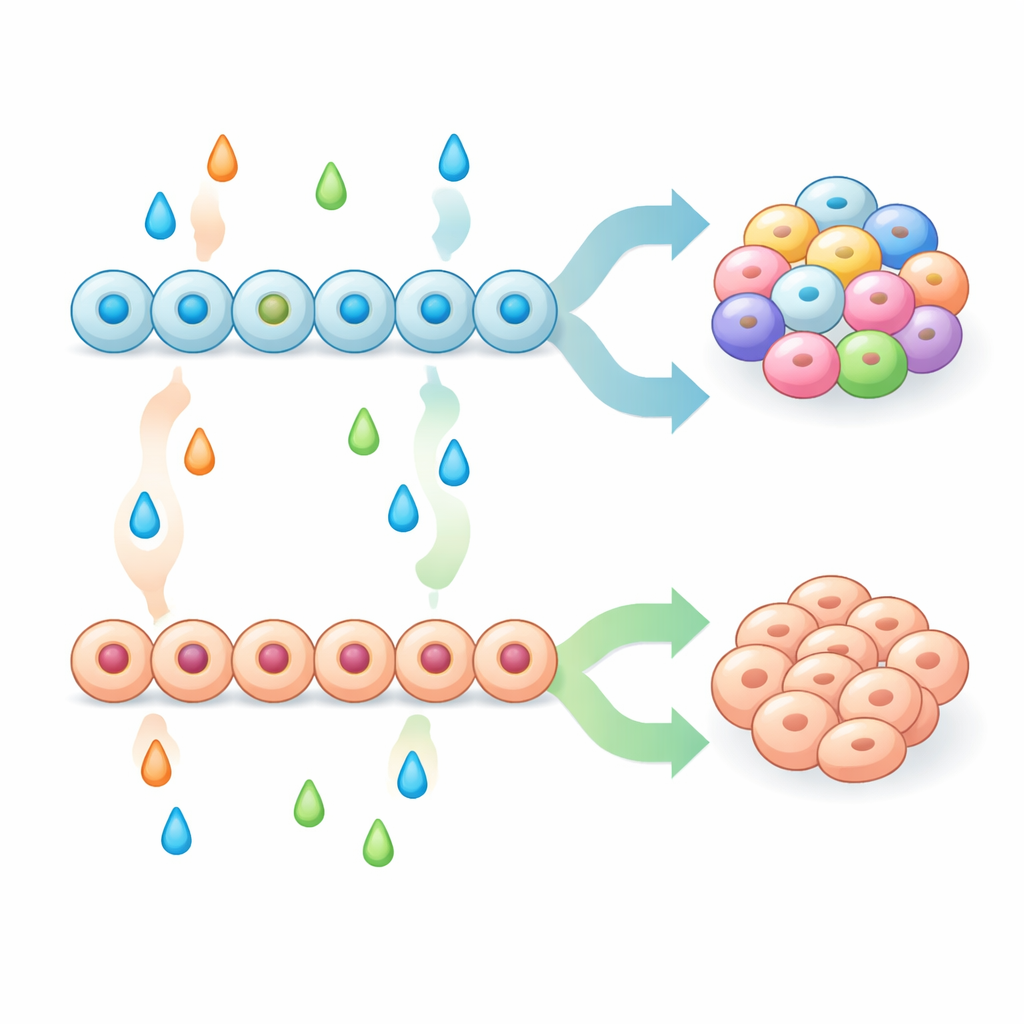
来自小鼠模型和基因活动的线索
为检验胰腺组织天然是否具备产生嗜铬样细胞的能力,团队检查了在发育中内分泌细胞中失去关键调控基因Isl1的工程小鼠。在这些动物中,胰岛含有大量具嗜铬细胞特征的细胞,包括血清素产生和转运蛋白SLC18A1的表达。对小鼠和人类干细胞衍生胰岛进行单细胞基因表达谱分析显示,胰腺中的嗜铬样细胞在分子特征上与肠道嗜铬细胞共享许多相似性,但也保留胰腺特征,如NKX6-1和与胰岛素相关的基因。一个显著的共同特点是转录因子Neurogenin 3(NGN3)活动持续时间延长——而NGN3在正常内分泌发育过程中通常仅短暂激活。在嗜铬样谱系中,NGN3在小鼠和人类体系中都呈现更长时间的活性,这提示该关键因子的时间学可能有助于决定一个前体是成为胰岛细胞还是嗜铬样细胞。
为治疗与研究设计细胞簇
通过描绘早期预设与晚期信号提示如何相互作用,这项工作为从人类干细胞设计“定制”内分泌簇提供了路线图。用于糖尿病治疗的方案若能将嗜铬样细胞降到最低并最大化成熟的β样细胞,应能产生更安全、反应更可预测且具有更好胰岛素响应的移植物。相反,从胰腺前体中生成大量纯净的嗜铬样细胞的能力,为研究产血清素的肠道细胞及其相关疾病开辟了新途径。简而言之,这项研究表明,干细胞衍生的胰腺模型并非只能接受随机结果:在合适的时间施以精心选择的化学信号,科学家可以将天平倾向期望的细胞类型,远离不需要的类型。
引用: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
关键词: 干细胞衍生胰岛, β细胞替代, 嗜铬细胞, 胰腺前体, 1型糖尿病