Clear Sky Science · ar
التحكم الفعّال في تمايز الخلايا الكروماتينية المعوية مقابل جزر البنكرياس المشتقة من خلايا جذعية بشرية متعددة القدرات
تحويل الخلايا الجذعية إلى مصانع إنسولين مفصلة حسب الطلب
بالنسبة للأشخاص المصابين بداء السكري من النوع الأول، قد يؤدي استبدال خلايا البنكرياس المنتجة للإنسولين المفقودة يومًا ما إلى تحريرهم من حقن الإنسولين. يمكن للعلماء بالفعل دفع الخلايا الجذعية البشرية لتكوين تجمعات بنكرياسية مصغرة تشبه مصانع الإنسولين في الجسم، لكن هذه «الجزر» المزروعة في المختبر متباينة المكونات: فإلى جانب الخلايا المنتجة للإنسولين المرغوبة، تظهر في الغالب أنواع خلايا غير مرغوبة. تطرح هذه الدراسة سؤالًا عمليًا له آثار كبيرة على العلاجات المستقبلية: هل يمكن توجيه الخلايا الجذعية بشكل موثوق نحو أنواع خلايا بنكرياسية مفيدة مع الحد من الخلايا خارج الهدف؟
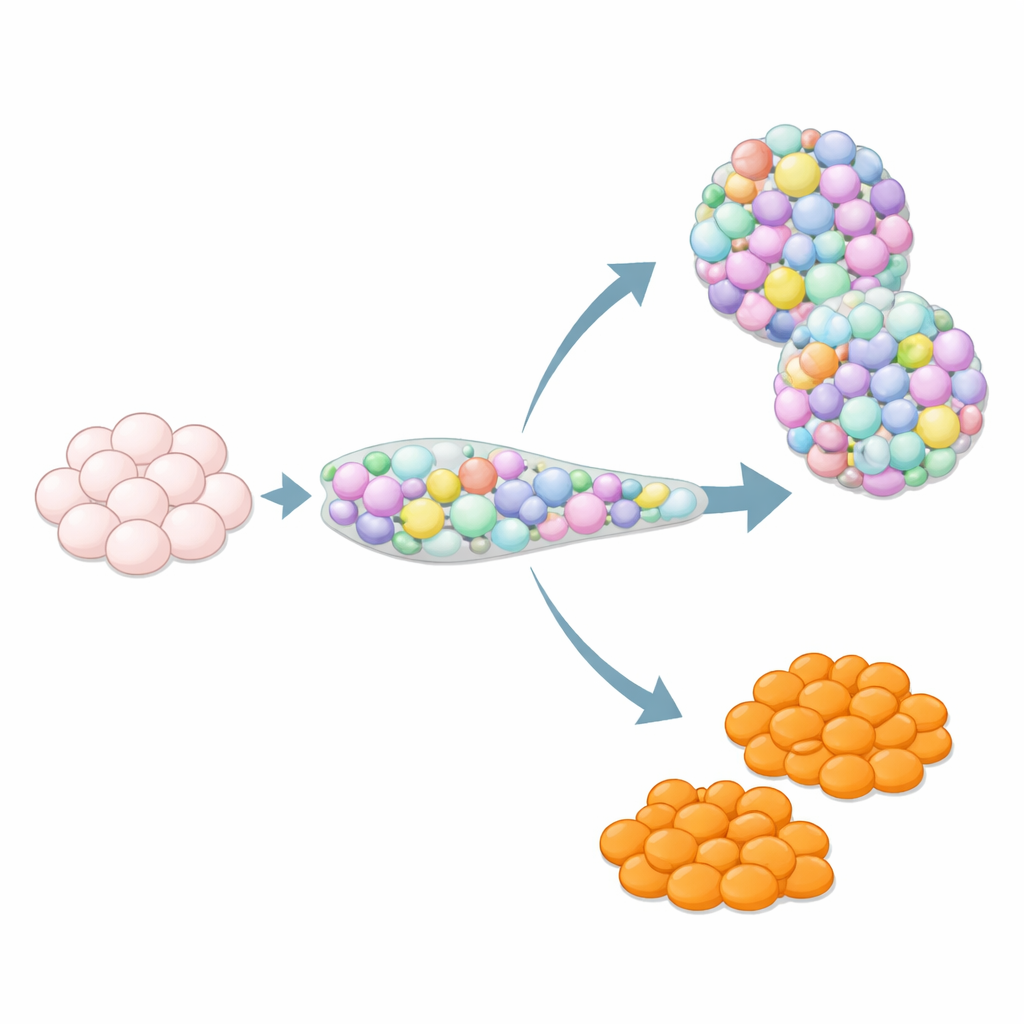
لماذا يمكن أن تكون الخلايا الإضافية مشكلة خفية
عندما تُوجَّه الخلايا الجذعية لتصبح نسيجًا بنكرياسيًا، فإنها لا تتبع دائمًا السيناريو المتوقع. من بين الضيوف المفاجئين خلايا تشبه الخلايا الكروماتينية المعوية، وهي نوع نادر من خلايا الأمعاء التي تعيش عادةً في المعدة والأمعاء وتساعد في التحكم بحركة وإشارات القناة الهضمية عن طريق إفراز السيروتونين. تظهر هذه الخلايا الشبيهة بالكروماتينية المعوية كثيرًا في الجزر المشتقة من الخلايا الجذعية، رغم أنها ليست جزءًا من جزر البنكرياس البشرية الطبيعية. وطالما أن تأثيرها على أداء الجزر وسلامتها غير مؤكد، يعتبرها الكثير من الباحثين ملوثات. في الوقت نفسه، وبما أن الأعضية المعوية الحقيقية غالبًا ما تجد صعوبة في إنتاج ما يكفي من الخلايا الكروماتينية المعوية، فقد تكون هذه الخلايا خارج الهدف ذات قيمة لدراسة بيولوجيا الأمعاء—إذا تمكن العلماء من التحكم في موعد ظهورها.
بناء نقطة انطلاق أفضل
بدأ المؤلفون بتحسين الخطوات الأولى لتحويل الخلايا الجذعية متعددة القدرات البشرية إلى «الخط البدائي» ثم إلى الأديم الباطن المحدد، النسيج الذي يتطور لاحقًا ليُكوّن البنكرياس وأعضاء أخرى. ووجدوا أن تعطيل الهيكل الخلوي الداخلي مؤقتًا بمركب يُدعى لاترنكولين A جعل هذا الانتقال الأولي أكثر ثباتًا، لا سيما في المزارعات ذات الكثافة العالية التي عادةً ما تستجيب بشكل ضعيف. أنتج هذا التعديل أديمًا باطنًا مبكرًا أكثر تجانسًا، وما تلاه كان المزيد من السلفيات البنكرياسية وخلايا شبيهة ببيتا قادرة على إنتاج الإنسولين. ومن المهم أن نفس التعديل المبكر حسّن أيضًا تكوين سلالات أخرى من الأديم الباطن مثل خلايا الرئة والخلايا الميزودرمية، مما يشير إلى طريقة مفيدة عمومًا لتقليل التباين في تمايز الخلايا الجذعية.
توجيه المصير: البنكرياسي مقابل الخلايا الشبيهة بالأمعاء
بوجود مجموعة انطلاق أقوى من السلفيات البنكرياسية، اختبرت الفريق تراكيب مختلفة من جزيئات الإشارة في المراحل اللاحقة بشكل منهجي ليروا كيف تشكل الخليط النهائي من الخلايا الصماء. دفعت بعض المعالجات، بما في ذلك مثبطات مسارات MAPK/ERK وBMP، السلفيات بقوة نحو الخلايا الشبيهة بالكروماتينية المعوية، في حين أن أخرى، مثل عوامل النمو FGF2 وبتاسيلكتين وBMP4، كبتت هذه الخلايا وفضّلت بدلاً من ذلك الأنواع البنكرياسية الكلاسيكية مثل خلايا ألفا وبيتا ودلتا. وأظهروا أن مجرد زيادة علامة بنكرياسية معروفة، NKX6-1، في وقت مبكر لم تكن كافية لمنع ظهور الخلايا الشبيهة بالكروماتينية المعوية. وبدلًا من ذلك، كان الناتج يعتمد على تفاعل بين التشكيل المبكر (كيفية تهيئة السلفيات) والتشكيل المتأخر (الإشارات التي تلقتها أثناء الالتزام الصمائي). من خلال مزج ومطابقة هذه الخطوات، أنشأ الباحثون وصفات أدت إما إلى تجمعات شبيهة بالجزر غنية بخلايا بيتا ذات إفراز قوي للإنسولين استجابة للجلوكوز، أو تجمعات غنية جدًا بالخلايا الشبيهة بالكروماتينية المعوية.
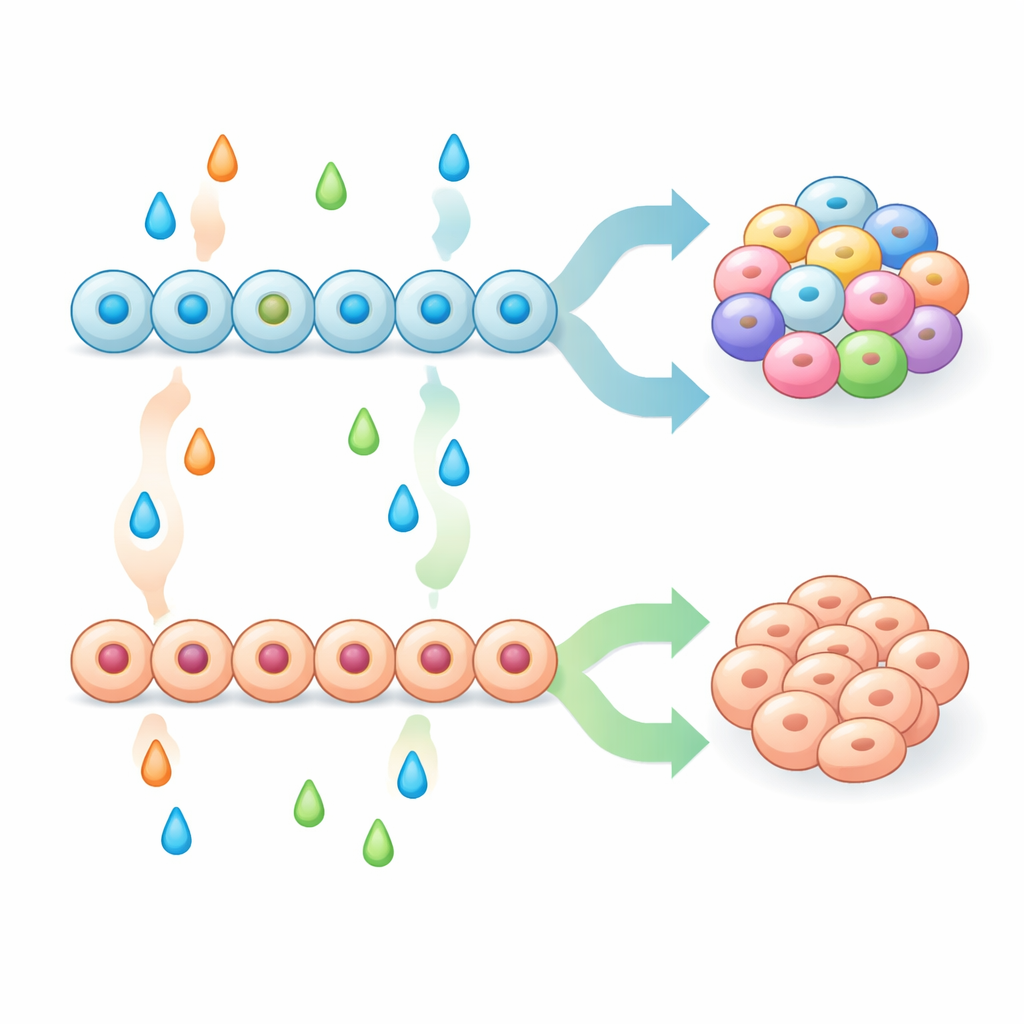
دلائل من نماذج الفئران ونشاط الجينات
لاختبار ما إذا كانت أنسجة البنكرياس بطبيعتها قادرة على إنتاج خلايا شبيهة بالكروماتينية المعوية، فحص الفريق فئرانًا مُعدَّلة لإزالة جين تنظيمي رئيسي، Isl1، في الخلايا الصماء النامية. في هذه الحيوانات، احتوت الجزر على العديد من الخلايا ذات خصائص الخلايا الكروماتينية المعوية، بما في ذلك إنتاج السيروتونين والتعبير عن ناقل SLC18A1. كشفت ملفات التعبير الجيني على مستوى الخلية الواحدة في كل من الفئران والجزر المشتقة من الخلايا الجذعية البشرية أن هذه الخلايا البنكرياسية الشبيهة بالكروماتينية المعوية تتشارك العديد من السمات الجزيئية مع خلايا كروماتينية معوية معوية، لكنها أيضًا تحمل علامات بنكرياسية مثل NKX6-1 وجينات مرتبطة بالإنسولين. ومن السمات المشتركة اللافتة نشاط مطول لعامل النسخ Neurogenin 3 (NGN3)، الذي عادةً ما ينشط لفترة قصيرة فقط أثناء التطور الصمائي. في السلالة الشبيهة بالكروماتينية المعوية، ظل NGN3 نشطًا لفترة أطول، في كل من نظامي الفأر والإنسان، مما يوحي بأن توقيت هذا العامل الرئيسي قد يساعد في تقرير ما إذا كانت السلفية ستصبح خلية جزيرية بنكرياسية أم خلية شبيهة بالكروماتينية المعوية.
تصميم تجمعات خلوية للعلاج والبحث
من خلال رسم خريطة لكيفية تفاعل التهيئة المبكرة وإشارات المراحل المتأخرة، يقدم هذا العمل خارطة طريق لتصميم تجمعات صماء «مصنوعة حسب الطلب» من الخلايا الجذعية البشرية. للاستخدام العلاجي في السكري، من المتوقع أن تُنتج البروتوكولات التي تقلل من الخلايا الشبيهة بالكروماتينية المعوية وتزيد من الخلايا الناضجة الشبيهة ببيتا طعومًا أكثر أمانًا وأكثر قابلية للتنبؤ مع استجابات إنسولين أفضل. وعلى النقيض، تفتح القدرة على إنتاج مجموعات كبيرة ونقية من الخلايا الشبيهة بالكروماتينية المعوية من السلفيات البنكرياسية طريقًا جديدًا لدراسة خلايا الأمعاء المنتجة للسيروتونين وأمراضها. ببساطة، توضح الدراسة أن نماذج البنكرياس المشتقة من الخلايا الجذعية ليست محصورة في نتائج عشوائية: باستخدام إشارات كيميائية مختارة بعناية في الأوقات المناسبة، يمكن للعلماء إمالة التوازن نحو أنواع الخلايا المرغوبة والابتعاد عن الأنواع غير المرغوبة.
الاستشهاد: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
الكلمات المفتاحية: جزر مشتقة من الخلايا الجذعية, استبدال خلايا بيتا, الخلايا الكروماتينية المعوية, السلفيات البنكرياسية, داء السكري النمط الأول