Clear Sky Science · ja
ヒト多能性幹細胞由来膵前駆細胞からのエンテロクロマフィン対アイソレット(膵島)分化の効率的制御
幹細胞をオーダーメイドのインスリン工場に変える
1型糖尿病の患者にとって、失われたインスリン産生細胞を置換できれば、将来的にインスリン注射から解放される可能性があります。研究者たちは既にヒト幹細胞を誘導して体内のインスリン工場に似たミニ膵島を作ることができますが、これらの培養由来「アイソレット」は望ましいインスリン産生細胞に混じって望ましくない細胞種が現れることが多く、混在した出来になりがちです。本研究は将来の治療に大きく関わる実践的な疑問を投げかけます:幹細胞を確実に適切な膵系細胞へ導きつつ、オフターゲットの細胞を抑制することはできるか?
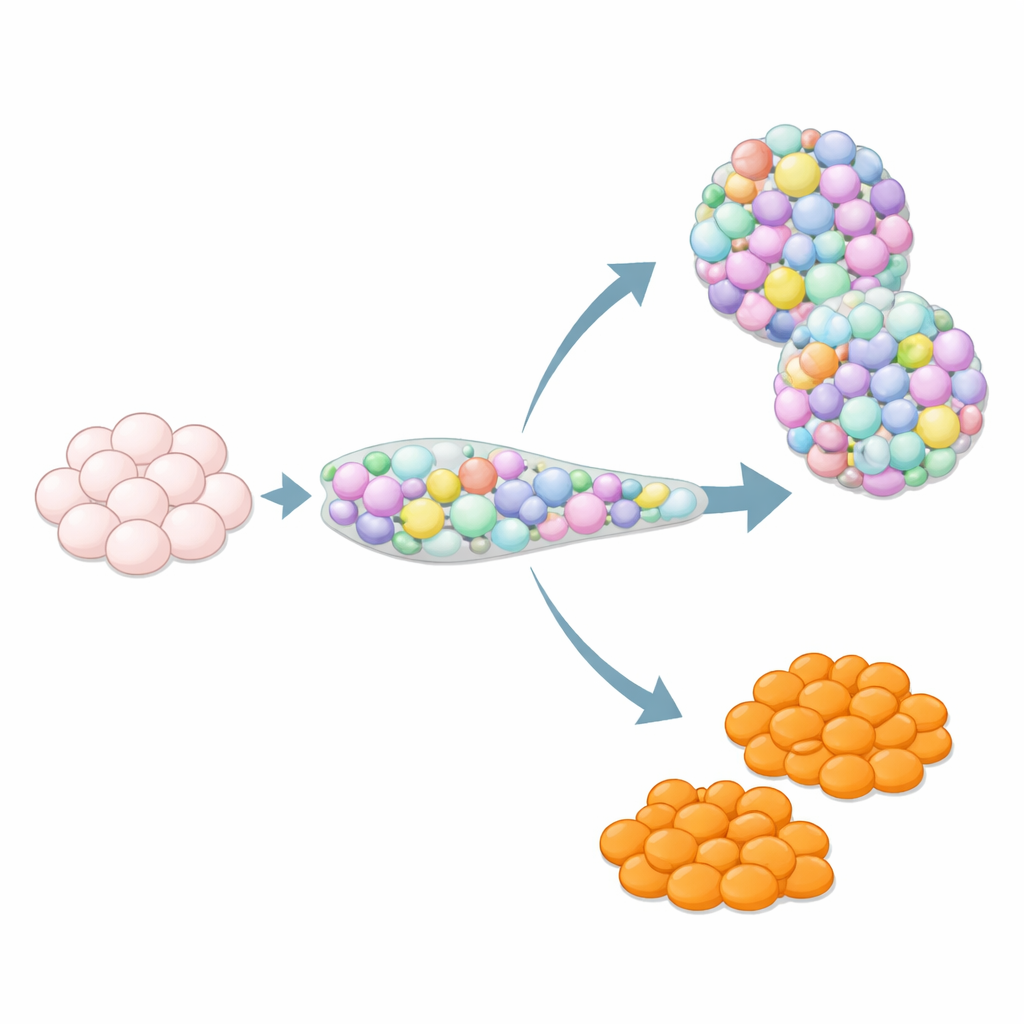
余分な細胞種が潜在的問題となる理由
幹細胞を膵組織へ導く際、必ずしも計画どおりに進むとは限りません。思いがけない訪問者の一つがエンテロクロマフィン様細胞で、これは通常胃や腸に存在し、セロトニンを放出して腸運動やシグナル伝達を制御する希少な腸細胞です。幹細胞由来のアイソレットにはこれらのエンテロクロマフィン様細胞がしばしば出現しますが、正常なヒト膵島の構成要素ではありません。これらがアイソレットの機能や安全性に与える影響は不確かで、多くの研究者はそれらを汚染物質と見なしています。一方で、本来の腸オルガノイドは十分な数のエンテロクロマフィン細胞を作るのが難しいことが多いため、オフターゲットとして現れるこれらの細胞は、出現のタイミングを制御できれば腸生物学の研究にとって貴重な資源になり得ます。
より良い出発点を作る
著者らはまず、ヒト多能性幹細胞を「原始線条(primitive streak)」、さらに膵や他の臓器のもとになる終末胚葉(definitive endoderm)へと導く初期段階を改善することから始めました。彼らは、ラトランクリンAという化合物で細胞の内部骨格を一時的に撹乱することで、この最初の遷移がより確実になることを見いだしました。特に通常は反応が悪い高密度播種培養で有効でした。この調整により初期の終末胚葉がより均一になり、その後に続く膵前駆細胞やインスリン産生に類似したベータ様細胞の生成が増加しました。重要なのは、同じ初期の調整が肺や中胚葉由来の細胞など他の胚葉由来系譜の形成も改善したことで、幹細胞分化のばらつきを減らす広く有用な手法であることが示唆されます。
運命の舵取り:膵系か腸様か
膵前駆細胞としての出発集団を強化したうえで、研究チームは後期の段階でのシグナル分子の組み合わせを系統的に試し、最終的な内分泌細胞の混合比にどう影響するかを調べました。MAPK/ERKやBMP経路の阻害剤など一部の処理は前駆細胞を強くエンテロクロマフィン様細胞へ傾けましたが、FGF2、ベータセルチュリン、BMP4といった成長因子はこれらを抑制し、アルファ・ベータ・デルタといった古典的な膵細胞型を好む結果をもたらしました。彼らは、よく知られた膵マーカーであるNKX6-1を早期に増加させるだけではエンテロクロマフィン様細胞の出現を防ぐには不十分であることを示しました。むしろ、結果は初期パターニング(前駆細胞がどのように事前に規定されたか)と後期パターニング(内分泌分化の際に受けたシグナル)の相互作用に左右されました。これらのステップを組み合わせることで、低グルコース環境でのインスリン分泌が強いベータ細胞に富むアイソレット様クラスターを得るレシピや、エンテロクロマフィン様細胞に高度に富むクラスターを得るレシピを作り出しました。
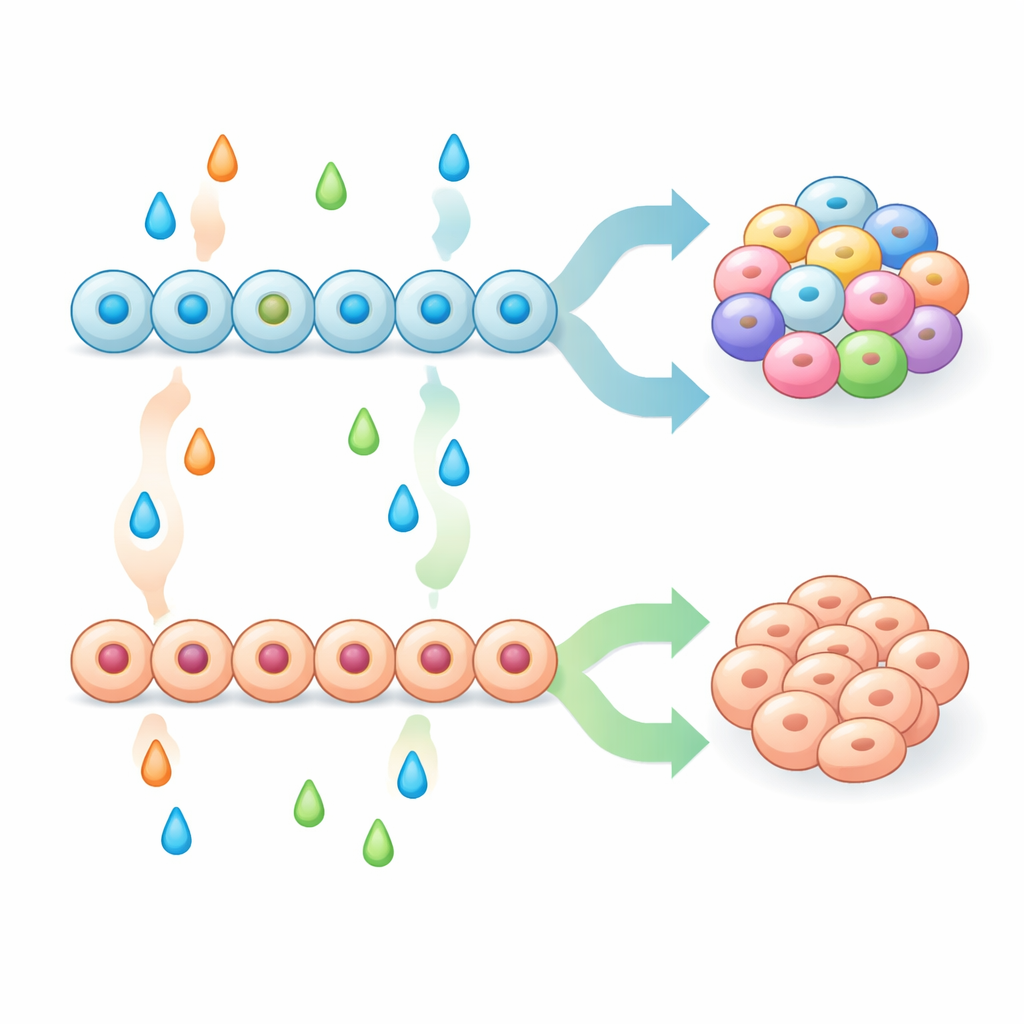
マウスモデルと遺伝子活動からの手がかり
膵組織が自然にエンテロクロマフィン様細胞を生み出す能力を持つかを調べるため、チームは発生中の内分泌細胞で主要な制御遺伝子Isl1を失うよう操作したマウスを調べました。これらの動物では、アイソレットにセロトニン産生や輸送体SLC18A1の発現などエンテロクロマフィン細胞の特徴を持つ多くの細胞が含まれていました。マウスおよびヒト幹細胞由来アイソレットのシングルセル遺伝子発現プロファイリングは、これら膵由来のエンテロクロマフィン様細胞が腸のエンテロクロマフィン細胞と多くの分子的特性を共有する一方で、NKX6-1やインスリン関連遺伝子といった膵の指標も持つことを明らかにしました。顕著な共通点は、転写因子Neurogenin 3(NGN3)の持続的な活性化で、通常は内分泌発生の間だけ短時間オンになるはずの因子が、エンテロクロマフィン様系譜ではより長く活性を保っていました。これはこの重要因子の発現タイミングが、前駆細胞が膵アイソレット細胞になるかエンテロクロマフィン様細胞になるかを決める一因であることを示唆します。
治療と研究のための細胞クラスター設計
初期のプライミングと後期のシグナルがどのように相互作用するかをマッピングすることで、本研究はヒト幹細胞から「注文どおり」の内分泌クラスターを設計するためのロードマップを提供します。糖尿病治療においては、エンテロクロマフィン様細胞を最小限に抑え成熟したベータ様細胞を最大化するプロトコルが、より安全で予測可能な移植片と優れたインスリン応答をもたらすはずです。逆に、膵前駆細胞から大量で純度の高いエンテロクロマフィン様細胞を作る能力は、セロトニン産生腸細胞とその疾患を研究する新しい道を開きます。簡潔に言えば、この研究は幹細胞由来膵モデルが偶然の結果に縛られているわけではないことを示しており、適切なタイミングで慎重に選んだ化学シグナルを与えることで、望ましい細胞型に傾け、望ましくない型を減らすことができると示しています。
引用: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
キーワード: 幹細胞由来アイソレット, ベータ細胞置換, エンテロクロマフィン細胞, 膵前駆細胞, 1型糖尿病