Clear Sky Science · es
Control eficiente de la diferenciación hacia células enterocromafines frente a islotes a partir de progenitores pancreáticos derivados de células madre pluripotentes humanas
Convertir células madre en fábricas de insulina a medida
Para las personas con diabetes tipo 1, reemplazar las células productoras de insulina perdidas del páncreas podría algún día liberarlas de las inyecciones de insulina. Los científicos ya pueden inducir a células madre humanas para formar racimos pancreáticos en miniatura que se parecen a las fábricas de insulina del cuerpo, pero estos «islotes» cultivados en laboratorio son una mezcla: junto a las deseadas células productoras de insulina, aparecen a menudo tipos celulares no deseados. Este estudio plantea una cuestión práctica con grandes implicaciones para futuras terapias: ¿podemos dirigir de forma fiable a las células madre hacia los tipos celulares pancreáticos correctos limitando a la vez los desvíos?
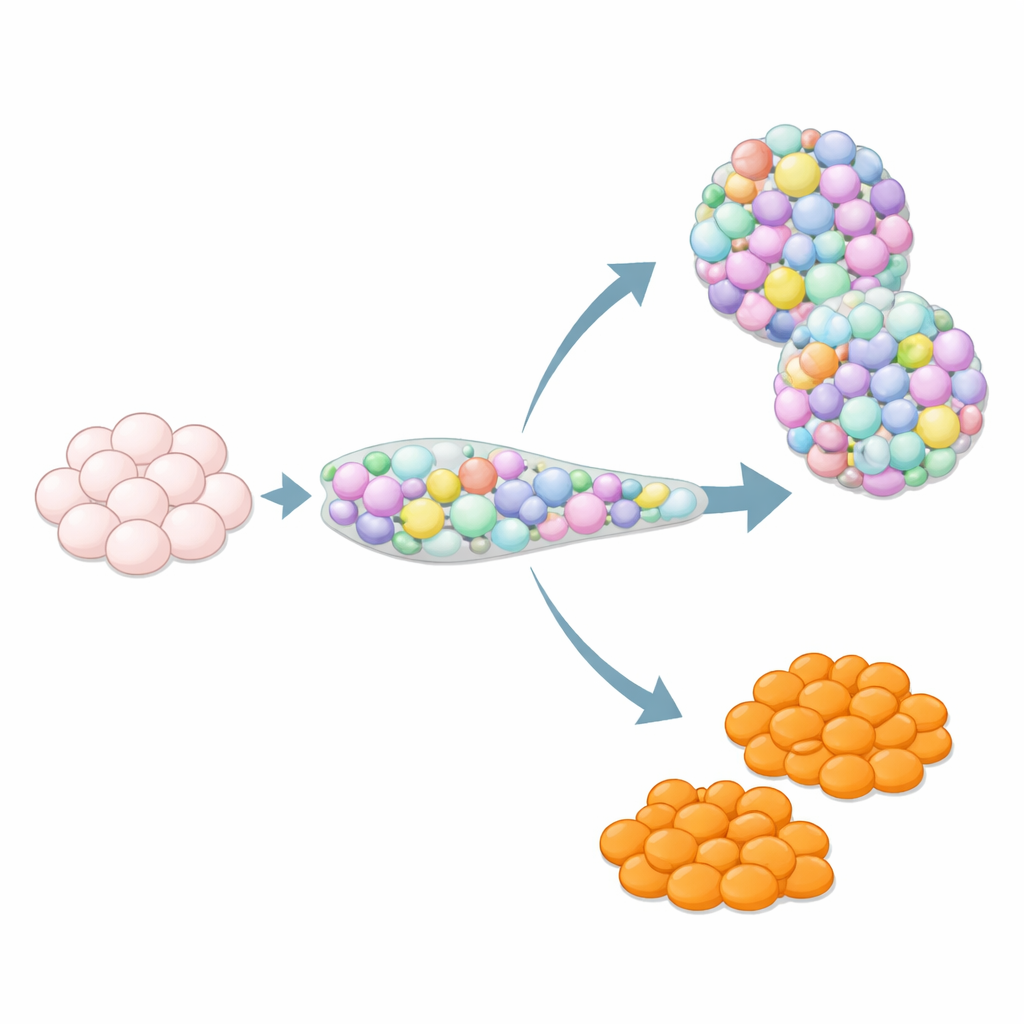
Por qué los tipos celulares extra pueden ser un problema oculto
Cuando se guía a las células madre para que se conviertan en tejido pancreático, no siempre siguen el guion. Entre los invitados sorpresa aparecen células que se parecen a las enterocromafines, un tipo celular poco frecuente del intestino que normalmente reside en el estómago y el intestino y contribuye al movimiento y la señalización intestinal liberando serotonina. En los islotes derivados de células madre, estas células similares a enterocromafines aparecen con frecuencia, aunque no formen parte de los islotes pancreáticos humanos normales. Su efecto sobre el rendimiento y la seguridad de los islotes es incierto, por lo que muchos investigadores las consideran contaminantes. Al mismo tiempo, dado que los organoides intestinales reales a menudo tienen dificultades para generar suficientes enterocromafines, estas células fuera de objetivo podrían ser valiosas para estudiar la biología intestinal, si los científicos pueden controlar cuándo aparecen.
Construir un mejor punto de partida
Los autores empezaron mejorando los pasos iniciales para convertir células madre pluripotentes humanas en la «línea primitiva» y luego en endodermo definitivo, el tejido que finalmente da lugar al páncreas y otros órganos. Encontraron que interrumpir brevemente el armazón interno de las células con un compuesto llamado latrunculina A hizo que esta primera transición fuera más robusta, especialmente en cultivos con alta densidad que normalmente responden mal. Esta modificación produjo un endodermo temprano más uniforme y, aguas abajo, más progenitores pancreáticos y células similares a las beta productoras de insulina. Importante: el mismo ajuste temprano también mejoró la formación de otras líneas basadas en endodermo, como células pulmonares y mesodérmicas, lo que sugiere una forma de uso general para reducir la variabilidad en la diferenciación de células madre.
Dirigir el destino: células pancreáticas frente a similares al intestino
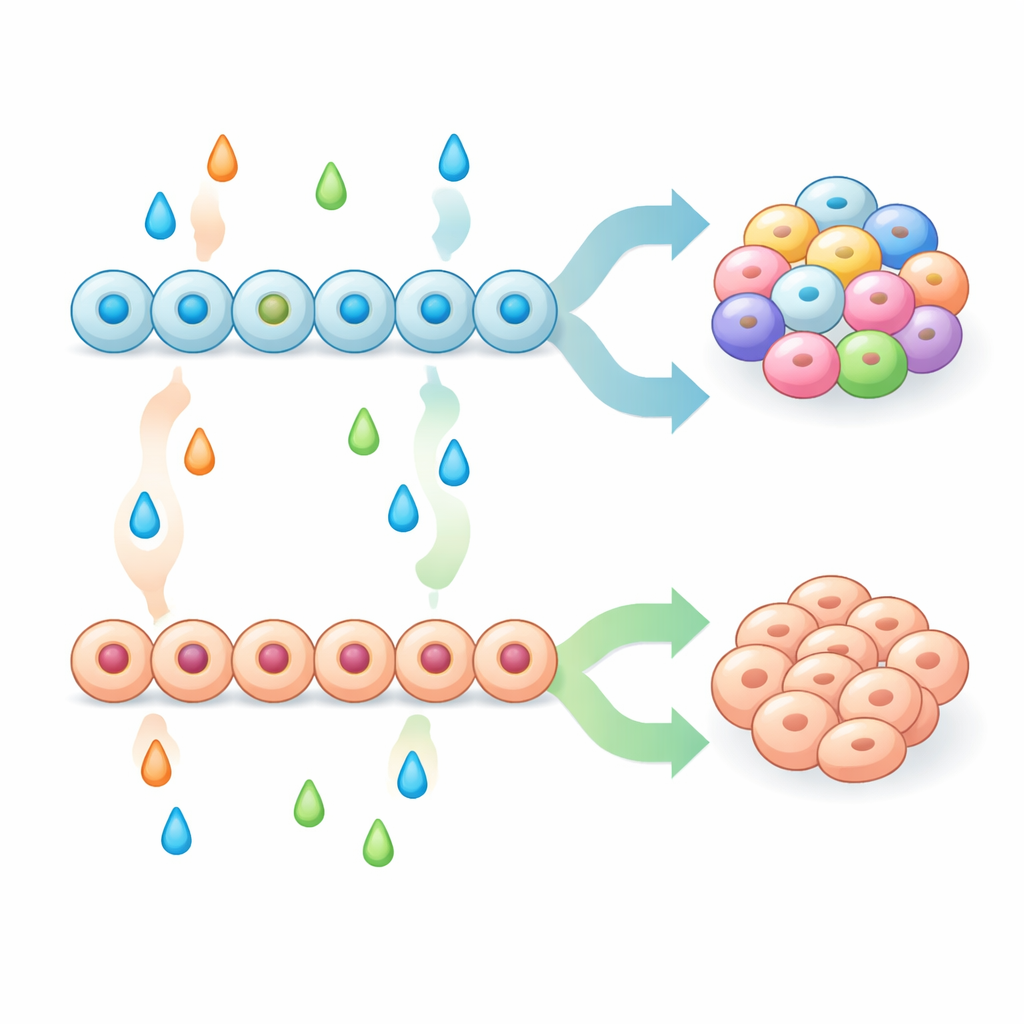
Con una población inicial más sólida de progenitores pancreáticos, el equipo probó de forma sistemática combinaciones de moléculas señalizadoras en etapas tardías para ver cómo moldeaban la mezcla final de tipos celulares endocrinos. Algunos tratamientos, incluidos inhibidores de las vías MAPK/ERK y BMP, empujaron a los progenitores con fuerza hacia células similares a las enterocromafines, mientras que otros, como los factores de crecimiento FGF2, betacelulina y BMP4, suprimieron estas células y favorecieron tipos pancreáticos clásicos como las células alfa, beta y delta. Mostraron que simplemente aumentar temprano un marcador pancreático bien conocido, NKX6-1, no fue suficiente para evitar la aparición de células similares a enterocromafines. Más bien, el resultado dependió de una interacción entre el patrón temprano (cómo se habían preparado los progenitores) y el patrón tardío (las señales que recibieron durante el compromiso endocrino). Al combinar y comparar estos pasos, los investigadores crearon recetas que producían racimos tipo islote enriquecidos en células beta con fuerte secreción de insulina estimulada por glucosa, o racimos altamente enriquecidos en células similares a enterocromafines.
Pistas de modelos en ratón y de la actividad génica
Para probar si los tejidos pancreáticos tienen de forma natural la capacidad de producir células similares a enterocromafines, el equipo examinó ratones diseñados para perder un gen regulador clave, Isl1, en células endocrinas en desarrollo. En estos animales, los islotes contenían muchas células con rasgos de enterocromafines, incluida la producción de serotonina y la expresión del transportador SLC18A1. El perfilado génico a nivel de una sola célula tanto en ratones como en islotes derivados de células madre humanas reveló que estas células pancreáticas similares a enterocromafines comparten muchos rasgos moleculares con las enterocromafines intestinales, pero también presentan rasgos pancreáticos como NKX6-1 y genes relacionados con la insulina. Una característica compartida llamativa fue la actividad prolongada del factor de transcripción Neurogenina 3 (NGN3), que normalmente se activa solo brevemente durante el desarrollo endocrino. En la línea similar a enterocromafines, NGN3 permaneció activo durante más tiempo, tanto en modelos de ratón como en sistemas humanos, lo que sugiere que el tiempo de actividad de este factor clave puede ayudar a decidir si un progenitor se convierte en una célula de islote pancreático o en una célula similar a enterocromafines.
Diseñar racimos celulares para terapia e investigación
Al cartografiar cómo interactúan el cebado temprano y las señales tardías, este trabajo ofrece una hoja de ruta para diseñar racimos endocrinos «hechos a medida» a partir de células madre humanas. Para el uso terapéutico en diabetes, los protocolos que minimicen las células similares a enterocromafines y maximicen las células beta maduras deberían producir injertos más seguros y predecibles con mejores respuestas de insulina. Por el contrario, la capacidad de generar poblaciones grandes y puras de células similares a enterocromafines a partir de progenitores pancreáticos abre una nueva vía para estudiar las células intestinales productoras de serotonina y sus enfermedades. En términos sencillos, el estudio demuestra que los modelos pancreáticos derivados de células madre no están condenados a resultados aleatorios: con señales químicas elegidas con cuidado en los momentos adecuados, los científicos pueden inclinar la balanza hacia los tipos celulares deseados y alejarse de los no deseados.
Cita: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Palabras clave: islotes derivados de células madre, reemplazo de células beta, células enterocromafines, progenitores pancreáticos, diabetes tipo 1