Clear Sky Science · pt
Controle eficiente da diferenciação entre células enterochromaffin e ilhotas a partir de progenitores pancreáticos derivados de células-tronco pluripotentes humanas
Transformando células-tronco em fábricas de insulina sob medida
Para pessoas com diabetes tipo 1, substituir as células produtoras de insulina perdidas do pâncreas pode, um dia, livrá‑las das injeções de insulina. Cientistas já conseguem induzir células-tronco humanas a formar pequenos aglomerados pancreáticos que se assemelham às “fábricas” de insulina do corpo, mas essas ilhotas cultivadas em laboratório são mistas: junto às desejadas células produtoras de insulina surgem frequentemente tipos celulares indesejados. Este estudo faz uma pergunta prática com grandes implicações para terapias futuras: podemos direcionar de forma confiável as células-tronco para os tipos pancreáticos desejáveis enquanto limitamos os destinos fora do alvo?
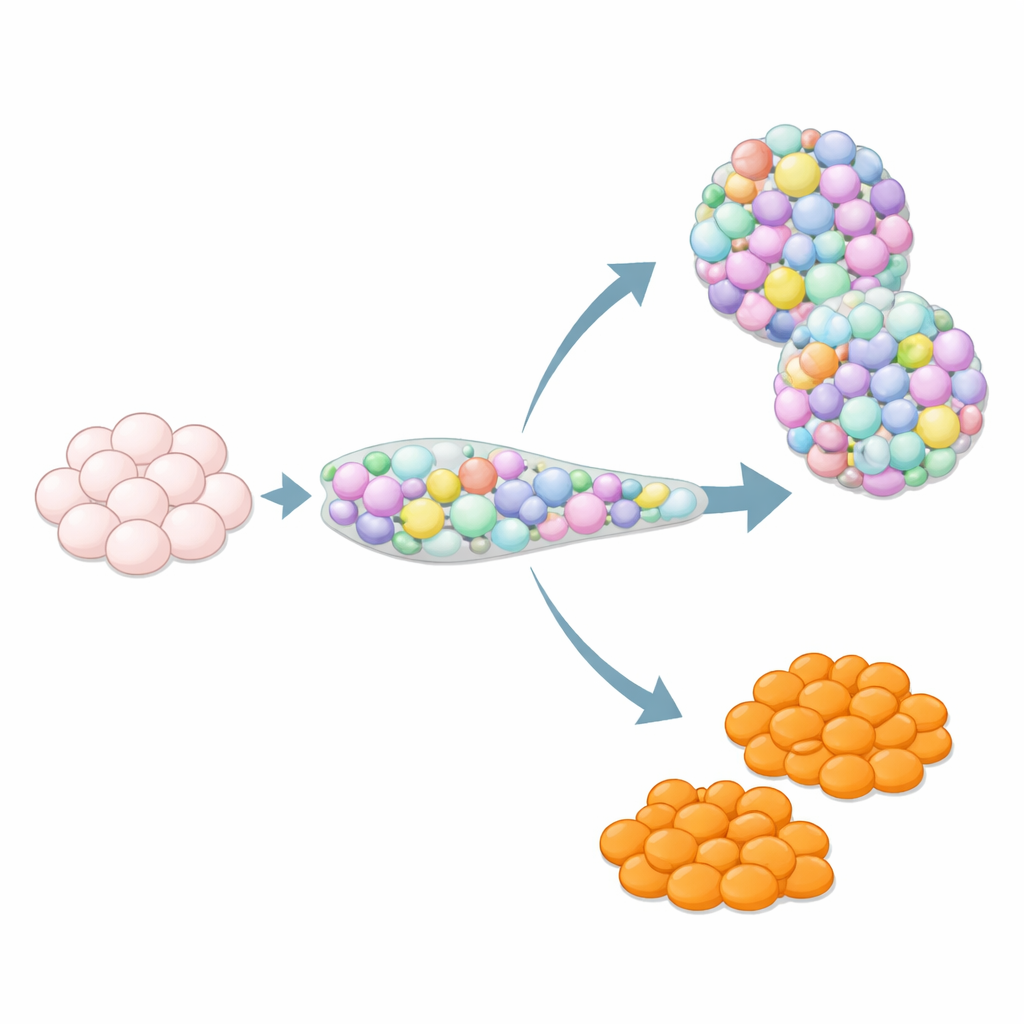
Por que tipos celulares extras podem ser um problema oculto
Quando células-tronco são guiadas para se tornarem tecido pancreático, elas nem sempre seguem o roteiro. Entre os convidados-surpresa estão células que se assemelham às enterochromaffin, um tipo raro de célula intestinal que normalmente vive no estômago e no intestino e ajuda a controlar o movimento e o sinalização do trato digestivo liberando serotonina. Nas ilhotas derivadas de células-tronco, essas células do tipo enterochromaffin aparecem com frequência, embora não façam parte das ilhotas pancreáticas humanas normais. Seu efeito sobre o desempenho e a segurança das ilhotas é incerto, por isso muitos pesquisadores as consideram contaminantes. Ao mesmo tempo, porque organoides intestinais reais frequentemente têm dificuldade em produzir número suficiente de células enterochromaffin, esses tipos fora do alvo podem ser valiosos para estudar a biologia intestinal — se os cientistas conseguirem controlar quando eles aparecem.
Construindo um ponto de partida melhor
Os autores começaram melhorando os passos iniciais de transformação de células-tronco pluripotentes humanas em “primitive streak” e depois em endoderma definitivo, o tecido que eventualmente dá origem ao pâncreas e a outros órgãos. Eles descobriram que interromper brevemente o arcabouço interno das células com um composto chamado latrunculina A tornou essa primeira transição mais robusta, especialmente em culturas densamente semeadas que geralmente respondem mal. Esse ajuste produziu um endoderma inicial mais uniforme e, a jusante, mais progenitores pancreáticos e células semelhantes às beta produtoras de insulina. Importante: a mesma modificação inicial também melhorou a formação de outras linhagens baseadas em endoderma, como células pulmonares e mesodérmicas, sugerindo uma forma amplamente útil de reduzir a variabilidade na diferenciação de células-tronco.
Direcionando o destino: células pancreáticas versus semelhantes às intestinais
Com uma população inicial mais forte de progenitores pancreáticos, a equipe testou sistematicamente combinações de moléculas sinalizadoras em estágios posteriores para ver como moldavam a mistura final de tipos celulares endócrinos. Alguns tratamentos, incluindo inibidores das vias MAPK/ERK e BMP, empurraram fortemente os progenitores na direção de células tipo enterochromaffin, enquanto outros, como os fatores de crescimento FGF2, betacelulina e BMP4, suprimiram essas células e favoreceram tipos pancreáticos clássicos, como células alfa, beta e delta. Eles demonstraram que simplesmente aumentar cedo um marcador pancreático bem conhecido, NKX6-1, não foi suficiente para prevenir o surgimento de células do tipo enterochromaffin. Em vez disso, o resultado dependia da interação entre o padronamento inicial (como os progenitores foram primados) e o padronamento tardio (os sinais que receberam durante o comprometimento endócrino). Ao combinar esses passos, os pesquisadores criaram receitas que geraram tanto aglomerados semelhantes a ilhotas enriquecidos em células beta com forte secreção de insulina estimulada por glicose, quanto aglomerados altamente enriquecidos em células do tipo enterochromaffin.
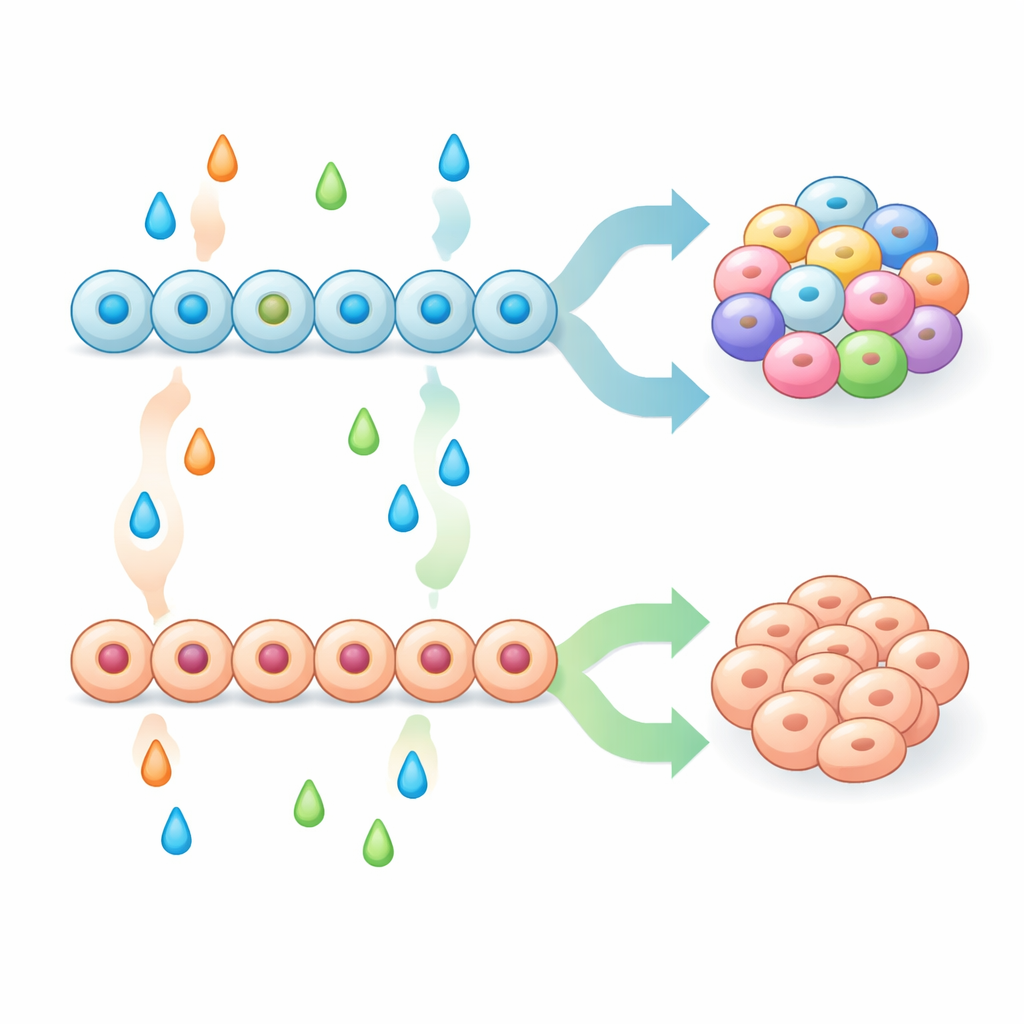
Pistas de modelos de camundongo e atividade gênica
Para testar se tecidos pancreáticos têm naturalmente a capacidade de produzir células do tipo enterochromaffin, a equipe examinou camundongos geneticamente modificados para perder um gene regulador chave, Isl1, em células endócrinas em desenvolvimento. Nesses animais, as ilhotas continham muitas células com características de enterochromaffin, incluindo produção de serotonina e expressão do transportador SLC18A1. Perfilagem gênica em célula única tanto em camundongos quanto em ilhotas derivadas de células-tronco humanas revelou que essas células pancreáticas tipo enterochromaffin compartilham muitos traços moleculares com células enterochromaffin intestinais, mas também carregam marcas pancreáticas como NKX6-1 e genes relacionados à insulina. Uma característica compartilhada marcante foi a atividade prolongada do fator de transcrição Neurogenin 3 (NGN3), que normalmente é ativado apenas por um breve período durante o desenvolvimento endócrino. Na linhagem tipo enterochromaffin, o NGN3 permaneceu ativo por mais tempo, tanto em sistemas de camundongo quanto humanos, sugerindo que o tempo de atuação desse fator chave pode ajudar a decidir se um progenitor se torna uma célula de ilhota pancreática ou uma célula do tipo enterochromaffin.
Projetando aglomerados celulares para terapia e pesquisa
Ao mapear como o priming inicial e as pistas de sinalização tardia interagem, este trabalho oferece um roteiro para projetar aglomerados endócrinos “feitos sob medida” a partir de células-tronco humanas. Para uso terapêutico no diabetes, protocolos que minimizem células do tipo enterochromaffin e maximizem células beta maduras devem produzir enxertos mais seguros e previsíveis, com melhores respostas de insulina. Por outro lado, a capacidade de gerar populações grandes e puras de células tipo enterochromaffin a partir de progenitores pancreáticos abre uma nova via para estudar células intestinais produtoras de serotonina e suas doenças. Em termos simples, o estudo mostra que modelos pancreáticos derivados de células-tronco não estão condenados a resultados aleatórios: com sinais químicos escolhidos com cuidado nos momentos certos, os cientistas podem inclinar a balança em direção aos tipos celulares desejados e afastar os indesejados.
Citação: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Palavras-chave: ilhotas derivadas de células-tronco, substituição de células beta, células enterochromaffin, progenitores pancreáticos, diabetes tipo 1