Clear Sky Science · de
Effiziente Steuerung der Differenzierung zu enterochromaffinen versus Inselzellen aus pankreatischen Vorläuferzellen humaner pluripotenter Stammzellen
Aus Stammzellen maßgeschneiderte Insinfabriken herstellen
Für Menschen mit Typ‑1‑Diabetes könnte das Ersetzen der verlorenen insulinproduzierenden Zellen der Bauchspeicheldrüse eines Tages die Notwendigkeit von Insulininjektionen überflüssig machen. Wissenschaftler können menschliche Stammzellen bereits dazu anleiten, miniaturisierte Pankreas‑Cluster zu bilden, die den insulinproduzierenden Inseln im Körper ähneln. Diese im Labor gezüchteten „Inseln“ sind jedoch gemischt: Neben den gewünschten insulinproduzierenden Zellen treten häufig unerwünschte Zelltypen auf. Die vorliegende Studie stellt eine praktische Frage mit großen Konsequenzen für künftige Therapien: Lassen sich Stammzellen zuverlässig in die erwünschten pankreatischen Zelltypen lenken und zugleich die Off‑Target‑Zellen begrenzen?
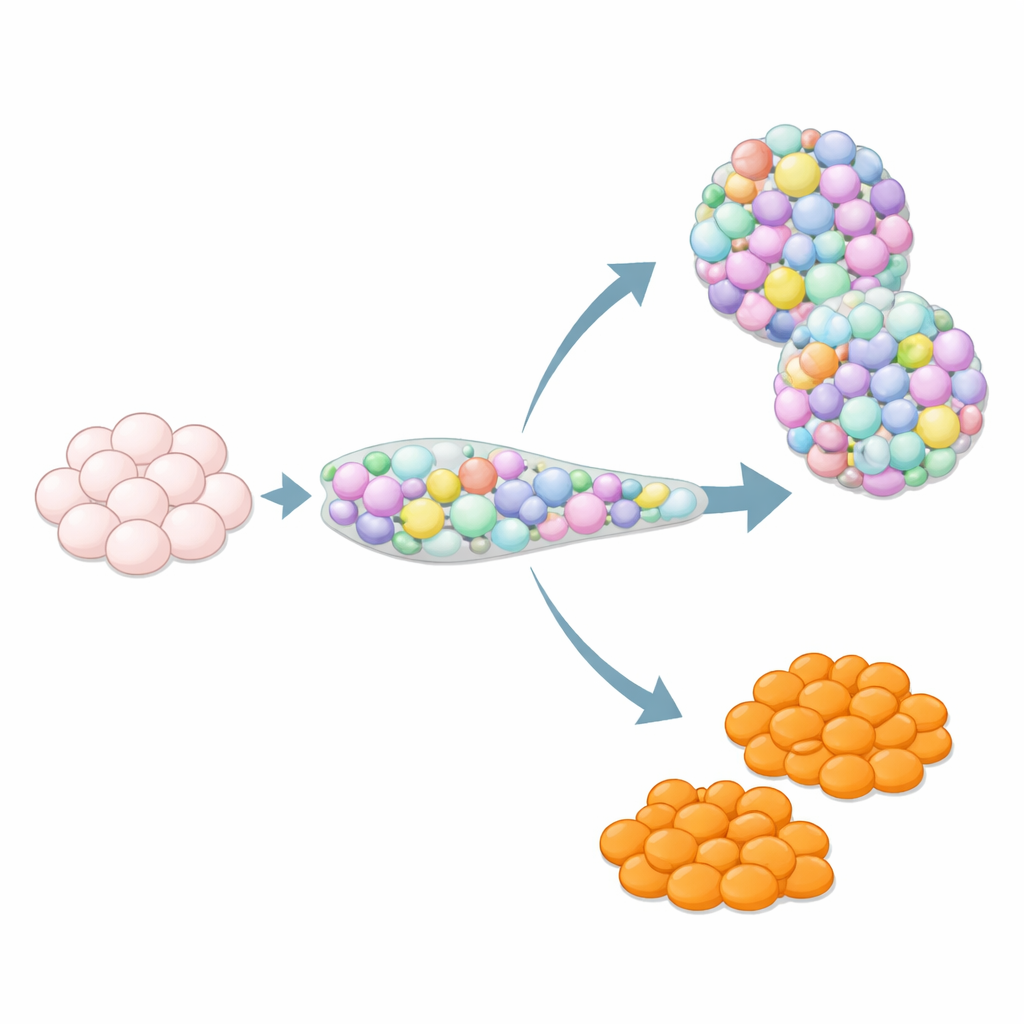
Warum zusätzliche Zelltypen ein verborgenes Problem sein können
Wenn Stammzellen auf dem Weg zur Pankreasbildung geleitet werden, halten sie sich nicht immer an das Drehbuch. Unter den unerwarteten Gästen finden sich Zellen, die enterochromaffinen Zellen ähneln — ein seltener Darmzelltyp, der normalerweise im Magen und Darm vorkommt und durch Serotoninfreisetzung Darmbewegung und Signalgebung steuert. In stammzellabgeleiteten Inseln tauchen diese enterochromaffin‑ähnlichen Zellen häufig auf, obwohl sie nicht zu normalen menschlichen Pankreas‑Inseln gehören. Ihre Auswirkung auf Funktion und Sicherheit der Inseln ist unklar, weshalb viele Forschende sie als Verunreinigungen betrachten. Gleichzeitig sind echte Darmorganoide oft schlecht darin, ausreichend enterochromaffine Zellen zu erzeugen; daher könnten diese Off‑Target‑Zellen wertvoll für das Studium der Darmbiologie sein — vorausgesetzt, Forscher können kontrollieren, wann sie entstehen.
Ein besserer Ausgangspunkt
Die Autorinnen und Autoren begannen damit, die frühesten Schritte der Umwandlung humaner pluripotenter Stammzellen in den „primitiven Streifen“ und anschließend in das definitive Endoderm zu verbessern — das Gewebe, aus dem schließlich Pankreas und andere Organe hervorgehen. Sie fanden heraus, dass eine kurzzeitige Störung des zellulären Gerüsts mit einem Wirkstoff namens Latrunculin A diesen ersten Übergang robuster machte, insbesondere in dicht besiedelten Kulturen, die sonst schlecht reagieren. Diese Anpassung erzeugte ein einheitlicheres frühes Endoderm und nachfolgend mehr pankreatische Vorläufer und insulinproduzierende Beta‑ähnliche Zellen. Wichtig ist, dass dieselbe frühe Modifikation auch die Bildung anderer endodermaler Linien wie Lungen‑ und mesodermaler Zellen verbesserte, was auf eine allgemein nützliche Methode zur Verringerung der Variabilität in der Stammzelldifferenzierung hindeutet.
Das Schicksal lenken: pankreatische versus darmähnliche Zellen
Mit einer stärkeren Ausgangspopulation pankreatischer Vorläufer testete das Team systematisch Kombinationen von Signalstoffen in späteren Stadien, um zu sehen, wie sie die endgültige Mischung endokriner Zelltypen beeinflussten. Einige Behandlungen, darunter Inhibitoren der MAPK/ERK‑ und BMP‑Signalwege, drängten die Vorläufer stark in Richtung enterochromaffin‑ähnlicher Zellen, während andere, wie die Wachstumsfaktoren FGF2, Betacellulin und BMP4, diese Zellen unterdrückten und stattdessen klassische pankreatische Typen wie Alpha‑, Beta‑ und Delta‑Zellen förderten. Sie zeigten, dass die alleinige frühe Erhöhung eines bekannten Pankreasmarkers, NKX6‑1, nicht ausreichte, um das Auftreten enterochromaffin‑ähnlicher Zellen zu verhindern. Vielmehr hing das Ergebnis von einer Wechselwirkung zwischen früher Musterung (wie Vorläufer vorgeprägt wurden) und späterer Musterung (den Signalen während der endokrinen Festlegung) ab. Durch das Kombinieren dieser Schritte entwickelten die Forschenden Protokolle, die entweder zu Beta‑Zell‑angereicherten, inselähnlichen Clustern mit starker glukosestimulierten Insulinsekretion führten oder zu Clustern mit hoher Anreicherung an enterochromaffin‑ähnlichen Zellen.
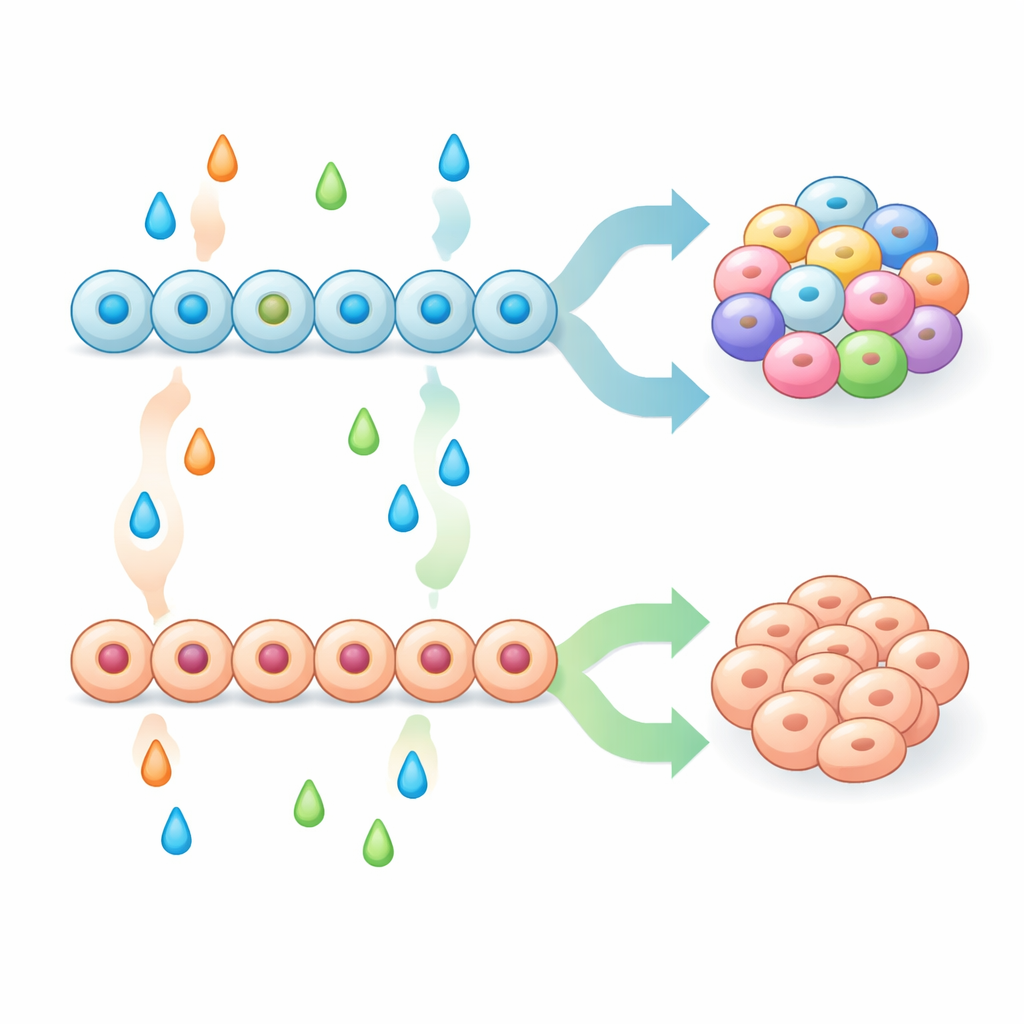
Hinweise aus Mausmodellen und Genaktivität
Um zu prüfen, ob pankreatische Gewebe natürlicherweise die Fähigkeit besitzen, enterochromaffin‑ähnliche Zellen zu produzieren, untersuchte das Team Mäuse, bei denen ein wichtiges Regulationsgen, Isl1, in sich entwickelnden endokrinen Zellen ausgeschaltet war. In diesen Tieren enthielten die Inseln viele Zellen mit Merkmalen enterochromaffiner Zellen, einschließlich Serotoninproduktion und Expression des Transporters SLC18A1. Einzelzell‑Genprofilierungen in sowohl Mäusen als auch stammzellabgeleiteten menschlichen Inseln zeigten, dass diese pankreatischen enterochromaffin‑ähnlichen Zellen viele molekulare Merkmale mit intestinalen enterochromaffinen Zellen teilen, aber auch pankreatische Kennzeichen wie NKX6‑1 und insulinbezogene Gene tragen. Ein auffälliges gemeinsames Merkmal war anhaltende Aktivität des Transkriptionsfaktors Neurogenin 3 (NGN3), der normalerweise während der endokrinen Entwicklung nur kurz aktiv ist. In der enterochromaffin‑ähnlichen Linie blieb NGN3 länger aktiv, sowohl in Maus‑ als auch in Humanmodellen, was darauf hindeutet, dass das Timing dieses Schlüssel‑Faktors mitentscheidet, ob ein Vorläufer zu einer pankreatischen Inselzelle oder zu einer enterochromaffin‑ähnlichen Zelle wird.
Zellcluster für Therapie und Forschung entwerfen
Indem die Studie aufzeigt, wie frühe Prägung und späte Signale miteinander interagieren, liefert sie eine Landkarte zum Entwerfen „maßgeschneiderter“ endokriner Cluster aus humanen Stammzellen. Für die therapeutische Anwendung bei Diabetes sollten Protokolle, die enterochromaffin‑ähnliche Zellen minimieren und reife Beta‑ähnliche Zellen maximieren, sicherere und vorhersagbarere Transplantate mit besseren Insulinantworten liefern. Umgekehrt eröffnet die Fähigkeit, große, reine Populationen enterochromaffin‑ähnlicher Zellen aus pankreatischen Vorläufern zu erzeugen, einen neuen Weg, serotoninerzeugende Darmzellen und ihre Erkrankungen zu erforschen. Kurz gesagt zeigt die Studie, dass stammzellabgeleitete Pankreasmodelle nicht dem Zufall ausgeliefert sind: Mit sorgfältig gewählten chemischen Signalen zur richtigen Zeit können Wissenschaftler das Gleichgewicht zugunsten gewünschter Zelltypen und zulasten unerwünschter verschieben.
Zitation: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Schlüsselwörter: stammzellabgeleitete Inseln, Beta-Zell-Ersatz, enterochromaffine Zellen, pankreatische Vorläuferzellen, Typ-1-Diabetes