Clear Sky Science · nl
Efficiënte sturing van enterochromaffiene versus eiland-differentiatie van humane pluripotente stamcel-afgeleide pancreatische voorlopercellen
Stamcellen omvormen tot op maat gemaakte insulinefabrieken
Voor mensen met type 1 diabetes kan het vervangen van de verloren gegane insulineproducerende cellen in de alvleesklier hen op termijn bevrijden van insuline-injecties. Wetenschappers kunnen inmiddels menselijke stamcellen stimuleren tot het vormen van mini-pancreasachtige clusterjes die lijken op de insulinefabrieken van het lichaam, maar deze in het laboratorium gekweekte “eilandjes” zijn niet altijd zuiver: naast de gewenste insulineproducerende cellen verschijnen vaak ook ongewenste celtypen. Deze studie stelt een praktische vraag met grote implicaties voor toekomstige therapieën: kunnen we stamcellen betrouwbaar sturen naar de gewenste pancreatische celtypen en tegelijkertijd off-target cellen beperken?
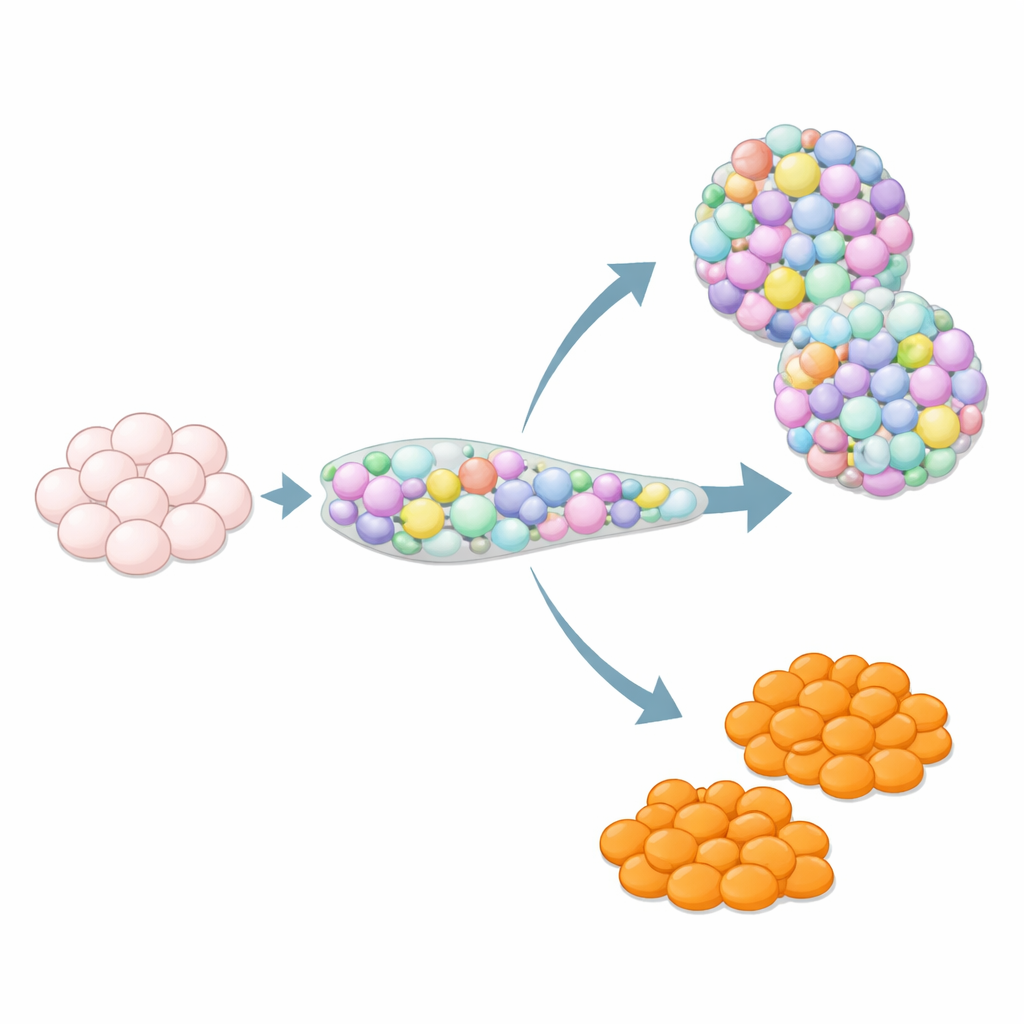
Waarom extra celtypen een verborgen probleem kunnen zijn
Wanneer stamcellen worden geleid naar pancreasweefsel, volgen ze niet altijd het verwachte traject. Tussen de verrassende aanwezigen zitten cellen die lijken op enterochromaffiene cellen, een zeldzaam type darmcel dat normaal in maag en darm voorkomt en de beweging en signalering van het darmstelsel helpt regelen door serotonine vrij te geven. In stamcel-afgeleide eilandjes duiken deze enterochromaffiene-achtige cellen vaak op, hoewel ze geen deel uitmaken van normale menselijke pancreaseilandjes. Hun invloed op de functie en veiligheid van eilandjes is onzeker, dus veel onderzoekers zien ze als verontreiniging. Tegelijkertijd, omdat echte darmorganoïden vaak moeite hebben voldoende enterochromaffiene cellen te produceren, kunnen deze off-target cellen waardevol zijn voor het bestuderen van darmbiologie — mits wetenschappers kunnen bepalen wanneer ze verschijnen.
Een beter beginpunt bouwen
De auteurs begonnen met het verbeteren van de vroegste stappen in het omzetten van menselijke pluripotente stamcellen naar de “primitieve strook” en vervolgens naar definitief endoderm, het weefsel dat uiteindelijk de pancreas en andere organen voortbrengt. Ze ontdekten dat het kort verstoren van het interne cytoskelet van de cellen met een verbinding genaamd latrunculine A deze eerste overgang robuuster maakte, vooral in dicht uitgezette culturen die normaal gesproken slecht reageren. Deze aanpassing leverde uniformer vroege endodermcellen op en downstream meer pancreatische voorlopercellen en bètacelachtige insulineproducerende cellen. Belangrijk is dat dezelfde vroege aanpassing ook de vorming van andere endodermgebaseerde lijnages, zoals long- en mesodermaal cellen, verbeterde, wat suggereert dat dit een algemeen bruikbare manier is om variabiliteit in stamcel-differentiatie te verminderen.
Het lot sturen: pancreatisch versus darmachtig
Met een sterker uitgangspopulatie van pancreatische voorlopercellen testte het team systematisch combinaties van signaalmoleculen in latere fases om te zien hoe die de uiteindelijke mix van endocriene celtypen bepaalden. Sommige behandelingen, waaronder remmers van de MAPK/ERK- en BMP-pathways, duwden voorlopercellen sterk richting enterochromaffiene-achtige cellen, terwijl andere, zoals groeifactoren FGF2, betacelluline en BMP4, deze cellen onderdrukten en in plaats daarvan klassieke pancreastypen zoals alfa-, bèta- en delta-cellen bevoordeelden. Ze toonden aan dat het simpelweg vroeg verhogen van een bekende pancreatische marker, NKX6-1, niet voldoende was om het verschijnen van enterochromaffiene-achtige cellen te voorkomen. De uitkomst hing eerder af van een wisselwerking tussen vroege pitvorming (hoe voorlopercellen werden geprimed) en latere signalering (de signalen die ze ontvingen tijdens endocriene toewijding). Door deze stappen te combineren konden de onderzoekers recepten maken die ofwel eilandachtige clusterjes opleverden die verrijkt waren in bètacellen met sterke glucosegestimuleerde insulineafgifte, of clusterjes die sterk verrijkt waren in enterochromaffiene-achtige cellen.
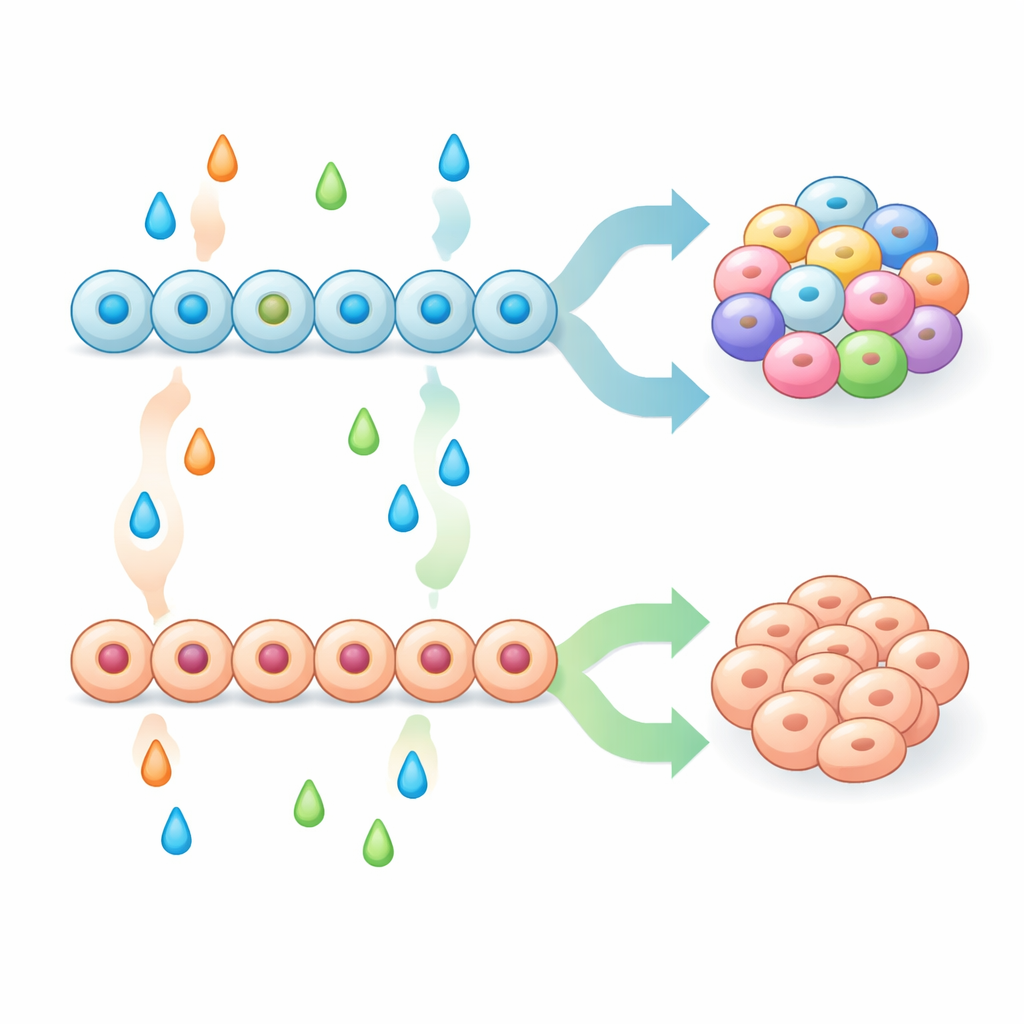
Aanhangsels uit muismodellen en genactiviteit
Om te testen of pancreatisch weefsel van nature de capaciteit heeft enterochromaffiene-achtige cellen te produceren, onderzochten de onderzoekers muizen die genetisch zo waren gemodificeerd dat ze een sleutelregelgen, Isl1, misten in zich ontwikkelende endocriene cellen. Bij deze dieren bevatten de eilandjes veel cellen met kenmerken van enterochromaffiene cellen, inclusief serotonineproductie en expressie van de transporter SLC18A1. Single-cell genprofilering in zowel muizen als humane stamcel-afgeleide eilandjes liet zien dat deze pancreatische enterochromaffiene-achtige cellen vele moleculaire eigenschappen delen met intestinale enterochromaffiene cellen, maar ook pancreatische kenmerken dragen zoals NKX6-1 en insuline-gerelateerde genen. Een opvallende gedeelde eigenschap was langdurige activiteit van de transcriptiefactor Neurogenin 3 (NGN3), die normaal gesproken slechts kort actief is tijdens endocriene ontwikkeling. In de enterochromaffiene-achtige lijn bleef NGN3 langer actief, in zowel muis- als humanosystemen, wat suggereert dat het tijdschema van deze sleutelregulator kan meebepalen of een voorlopercel een pancreatische eilandcel of een enterochromaffiene-achtige cel wordt.
Ontwerpen van celclusterjes voor therapie en onderzoek
Door in kaart te brengen hoe vroege priming en late signaleringen op elkaar inwerken, biedt dit werk een routekaart voor het ontwerpen van “op maat gemaakte” endocriene clusterjes uit menselijke stamcellen. Voor therapeutisch gebruik bij diabetes zouden protocollen die enterochromaffiene-achtige cellen minimaliseren en rijpe bètacelachtige cellen maximaliseren veiliger en beter voorspelbare grafts moeten opleveren met verbeterde insulineantwoorden. Omgekeerd opent het vermogen om grote, zuivere populaties enterochromaffiene-achtige cellen uit pancreatische voorlopers te genereren een nieuwe weg om serotonine-producerende darmcellen en hun ziektes te bestuderen. In eenvoudige bewoordingen toont de studie aan dat stamcel-afgeleide pancreasmodellen niet vastzitten aan willekeurige uitkomsten: met zorgvuldig gekozen chemische signalen op de juiste momenten kunnen wetenschappers het evenwicht kantelen naar gewenste celtypen en weg van ongewenste.
Bronvermelding: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Trefwoorden: stamcel-afgeleide eilandjes, vervanging van bètacellen, enterochromaffiene cellen, pancreatische voorlopercellen, type 1 diabetes