Clear Sky Science · fr
Contrôle efficace de la différenciation en cellules entérochromaffines versus îlots à partir de progéniteurs pancréatiques dérivés de cellules souches pluripotentes humaines
Transformer des cellules souches en usines d’insuline sur mesure
Pour les personnes atteintes de diabète de type 1, remplacer les cellules productrices d’insuline perdues du pancréas pourrait un jour les libérer des injections d’insuline. Les scientifiques savent déjà provoquer la différenciation de cellules souches humaines en amas pancréatiques miniatures qui ressemblent aux usines à insuline du corps, mais ces « îlots » cultivés en laboratoire sont hétérogènes : en plus des cellules productrices d’insuline recherchées, des types cellulaires indésirables apparaissent souvent. Cette étude pose une question pratique aux grandes implications pour les thérapies futures : peut-on orienter de manière fiable les cellules souches vers les bons types cellulaires pancréatiques tout en limitant les populations hors cible ?
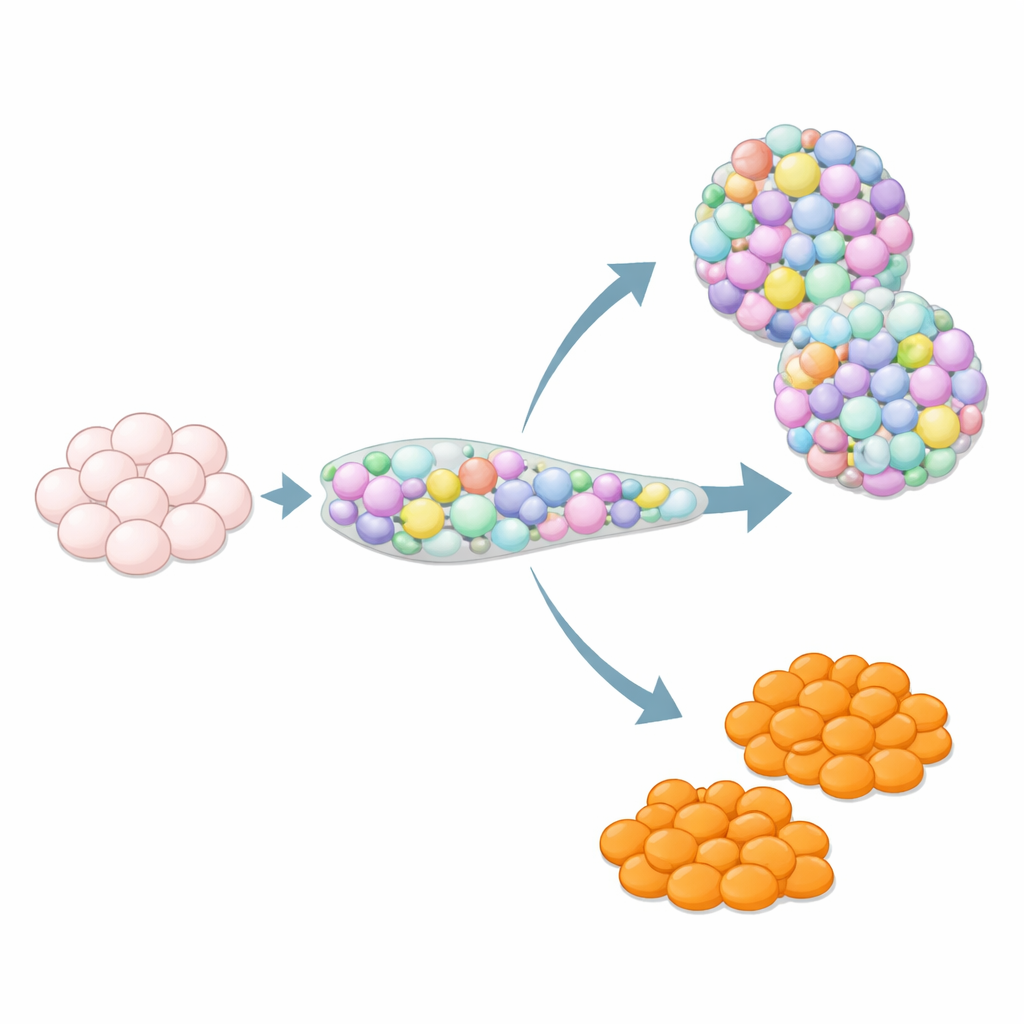
Pourquoi des types cellulaires supplémentaires peuvent poser problème
Lorsque les cellules souches sont dirigées pour devenir du tissu pancréatique, elles ne suivent pas toujours le scénario prévu. Parmi les invités surprises figurent des cellules ressemblant aux entérochromaffines, un type cellulaire rare de l’intestin qui vit normalement dans l’estomac et l’intestin et aide à contrôler le mouvement intestinal et la signalisation en libérant de la sérotonine. Dans les îlots dérivés de cellules souches, ces cellules de type entérochromaffine apparaissent fréquemment, bien qu’elles ne fassent pas partie des îlots pancréatiques humains normaux. Leur effet sur la performance et la sécurité des îlots est incertain, si bien que de nombreux chercheurs les considèrent comme des contaminants. Dans le même temps, parce que les véritables organoïdes intestinaux peinent souvent à produire suffisamment de cellules entérochromaffines, ces populations hors cible pourraient être précieuses pour étudier la biologie intestinale — à condition que les chercheurs puissent contrôler leur apparition.
Construire un meilleur point de départ
Les auteurs ont commencé par améliorer les premières étapes de la transformation des cellules souches pluripotentes humaines en « ligne primitive » puis en endoderme définitif, le tissu qui donnera plus tard naissance au pancréas et à d’autres organes. Ils ont découvert que perturber brièvement le échafaudage interne des cellules avec un composé appelé latrunculine A rendait cette première transition plus robuste, en particulier dans des cultures à densité élevée qui répondent habituellement mal. Cet ajustement a produit un endoderme précoce plus homogène et, en aval, davantage de progéniteurs pancréatiques et de cellules de type bêta productrices d’insuline. Fait important, la même modification précoce a également amélioré la formation d’autres lignées d’origine endodermique telles que les cellules pulmonaires et mésodermiques, suggérant une façon largement utile de réduire la variabilité lors de la différenciation des cellules souches.
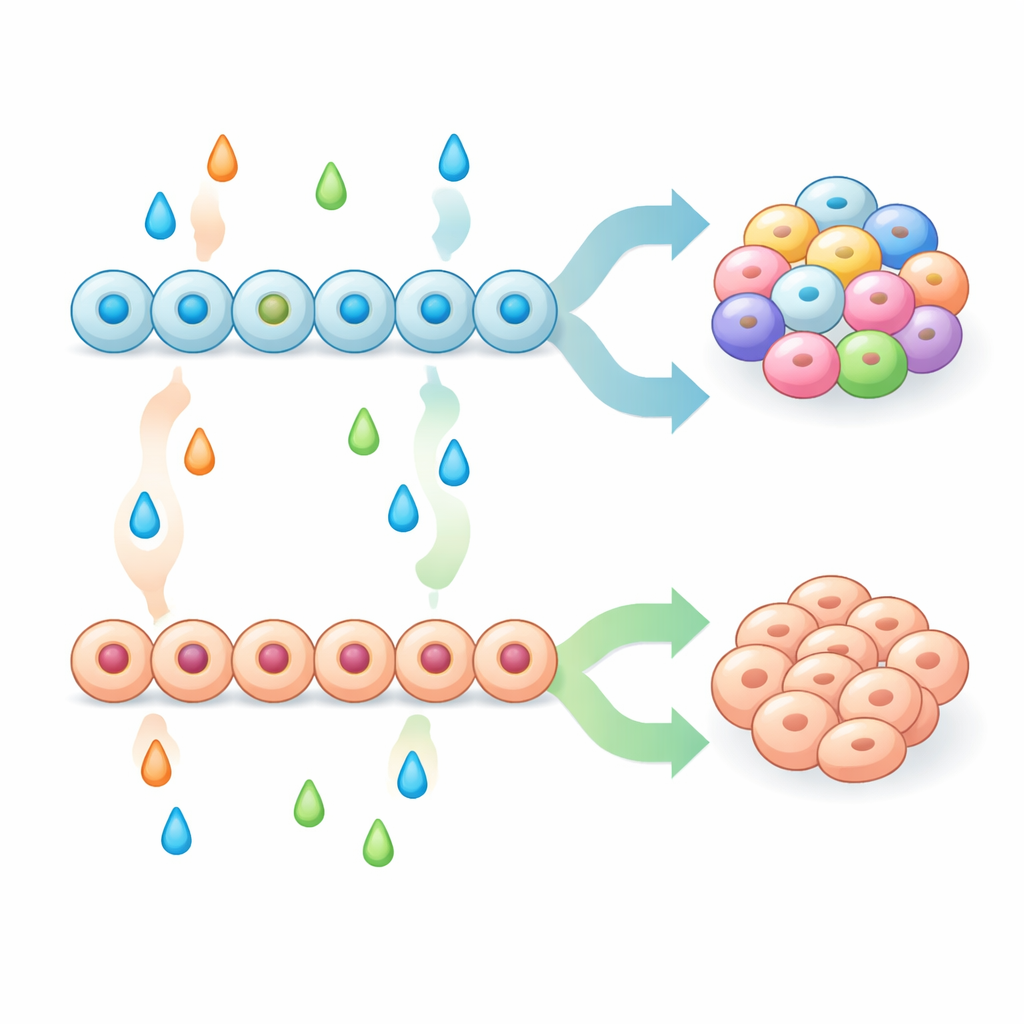
Orienter le destin : cellules pancréatiques contre cellules de type intestinal
Avec une population initiale de progéniteurs pancréatiques renforcée, l’équipe a testé systématiquement des combinaisons de molécules de signalisation aux stades ultérieurs pour voir comment elles façonnaient le mélange final des types cellulaires endocriniens. Certains traitements, notamment des inhibiteurs des voies MAPK/ERK et BMP, ont fortement poussé les progéniteurs vers des cellules de type entérochromaffine, tandis que d’autres, comme les facteurs de croissance FGF2, la bétacelluline et BMP4, ont supprimé ces cellules et favorisé à la place des types pancréatiques classiques tels que les cellules alpha, bêta et delta. Ils ont montré que l’augmentation précoce d’un marqueur pancréatique bien connu, NKX6-1, ne suffisait pas à empêcher l’apparition de cellules de type entérochromaffine. En réalité, le résultat dépendait d’une interaction entre le patronage précoce (la façon dont les progéniteurs étaient amorcés) et le patronage tardif (les signaux reçus lors de l’engagement endocrinien). En combinant ces étapes, les chercheurs ont créé des protocoles produisant soit des amas de type îlot enrichis en cellules bêta avec une forte sécrétion d’insuline stimulée par le glucose, soit des amas fortement enrichis en cellules de type entérochromaffine.
Indices provenant de modèles murins et de l’activité génique
Pour vérifier si les tissus pancréatiques ont naturellement la capacité de produire des cellules de type entérochromaffine, l’équipe a examiné des souris génétiquement modifiées pour perdre un gène régulateur clé, Isl1, dans les cellules endocrines en développement. Chez ces animaux, les îlots contenaient de nombreuses cellules présentant des caractéristiques d’entérochromaffines, notamment la production de sérotonine et l’expression du transporteur SLC18A1. Le profilage génique unicellulaire chez la souris et dans les îlots dérivés de cellules souches humaines a révélé que ces cellules pancréatiques de type entérochromaffine partagent de nombreux traits moléculaires avec les entérochromaffines intestinales, mais portent aussi des marqueurs pancréatiques tels que NKX6-1 et des gènes liés à l’insuline. Une caractéristique frappante commune était une activité prolongée du facteur de transcription Neurogenin 3 (NGN3), qui s’active normalement de façon brève pendant le développement endocrinien. Dans la lignée de type entérochromaffine, NGN3 restait actif plus longtemps, tant chez la souris que dans les systèmes humains, suggérant que le timing de ce facteur clé pourrait aider à décider si un progéniteur devient une cellule d’un îlot pancréatique ou une cellule de type entérochromaffine.
Concevoir des amas cellulaires pour la thérapie et la recherche
En cartographiant l’interaction entre l’amorçage précoce et les signaux tardifs, ce travail offre une feuille de route pour concevoir des amas endocriniens « fabriqués sur mesure » à partir de cellules souches humaines. Pour un usage thérapeutique dans le diabète, des protocoles qui minimisent les cellules de type entérochromaffine et maximisent les cellules bêta matures devraient produire des greffons plus sûrs et plus prévisibles avec de meilleures réponses à l’insuline. À l’inverse, la capacité à générer de larges populations pures de cellules de type entérochromaffine à partir de progéniteurs pancréatiques ouvre une nouvelle voie pour étudier les cellules intestinales productrices de sérotonine et leurs maladies. En termes simples, l’étude montre que les modèles pancréatiques dérivés de cellules souches ne sont pas condamnés à des résultats aléatoires : avec des signaux chimiques choisis au bon moment, les scientifiques peuvent infléchir l’équilibre en faveur des types cellulaires souhaités et à l’encontre des indésirables.
Citation: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Mots-clés: îlots dérivés de cellules souches, remplacement des cellules bêta, cellules entérochromaffines, progéniteurs pancréatiques, diabète de type 1