Clear Sky Science · it
Controllo efficiente della differenziazione verso cellule enterochromaffini rispetto alle isole pancreatiche da progenitori pancreatici derivati da cellule staminali pluripotenti umane
Trasformare le cellule staminali in fabbriche di insulina su misura
Per le persone con diabete di tipo 1, sostituire le cellule pancreatiche produttrici di insulina perdute potrebbe un giorno liberarle dalle iniezioni di insulina. Gli scienziati sono già in grado di indurre le cellule staminali umane a formare mini aggregazioni pancreatiche che somigliano alle “fabbriche” di insulina del corpo, ma queste isole coltivate in laboratorio sono eterogenee: insieme alle cellule produttrici di insulina desiderate, spesso compaiono tipi cellulari non voluti. Questo studio pone una domanda pratica con grandi implicazioni per le terapie future: possiamo indirizzare in modo affidabile le cellule staminali verso i tipi pancreatici desiderati limitando quelli fuori bersaglio?
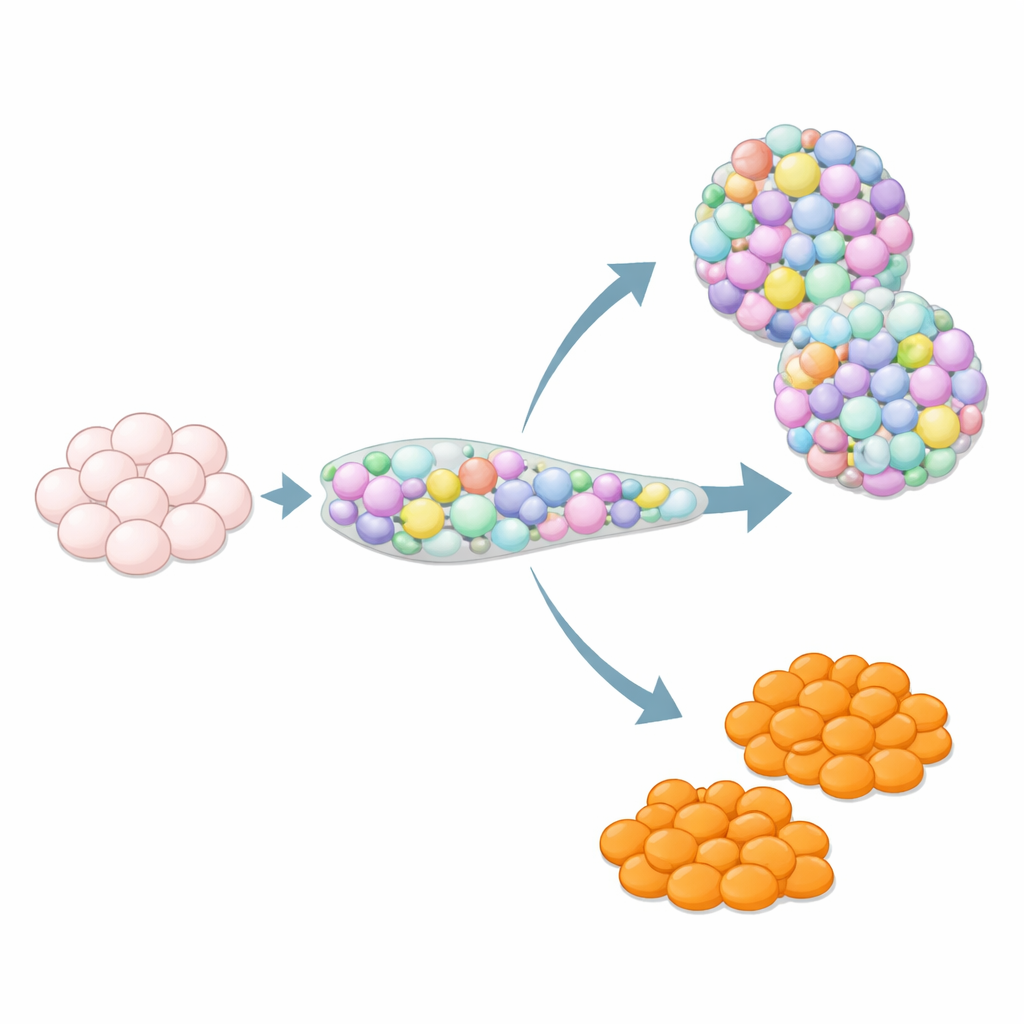
Perché i tipi cellulari extra possono essere un problema nascosto
Quando le cellule staminali vengono guidate a diventare tessuto pancreatico, non seguono sempre lo schema previsto. Tra gli ospiti inattesi ci sono cellule somiglianti alle enterochromaffini, un raro tipo cellulare dell’intestino che normalmente risiede nello stomaco e nell’intestino e contribuisce a regolare il movimento e il segnalamento gastrointestinale rilasciando serotonina. Nelle isole derivate da cellule staminali, queste cellule simili alle enterochromaffini compaiono frequentemente, anche se non fanno parte delle isole pancreatiche umane normali. Il loro impatto sul funzionamento e sulla sicurezza delle isole è incerto, quindi molti ricercatori le considerano contaminanti. Allo stesso tempo, poiché gli organoidi intestinali reali spesso fanno fatica a generare un numero sufficiente di cellule enterochromaffini, questi elementi fuori bersaglio potrebbero essere preziosi per studiare la biologia intestinale—se gli scienziati riescono a controllare quando compaiono.
Costruire un punto di partenza migliore
Gli autori hanno iniziato migliorando i primi passaggi della trasformazione delle cellule staminali pluripotenti umane in “primitive streak” e poi in endoderma definitivo, il tessuto che alla fine dà origine al pancreas e ad altri organi. Hanno scoperto che brevemente perturbare l’impalcatura interna delle cellule con un composto chiamato latrunculina A rendeva questa prima transizione più robusta, specialmente nelle colture ad alta densità che di solito rispondono male. Questa modifica ha prodotto un endoderma precoce più uniforme e, a valle, più progenitori pancreatici e cellule simili alle beta produttrici di insulina. Importante, lo stesso aggiustamento precoce ha anche migliorato la formazione di altre linee derivate dall’endoderma come polmone e cellule mesodermiche, suggerendo un modo di uso generale per ridurre la variabilità nella differenziazione delle cellule staminali.
Indirizzare il destino: cellule pancreatiche versus simili all’intestino
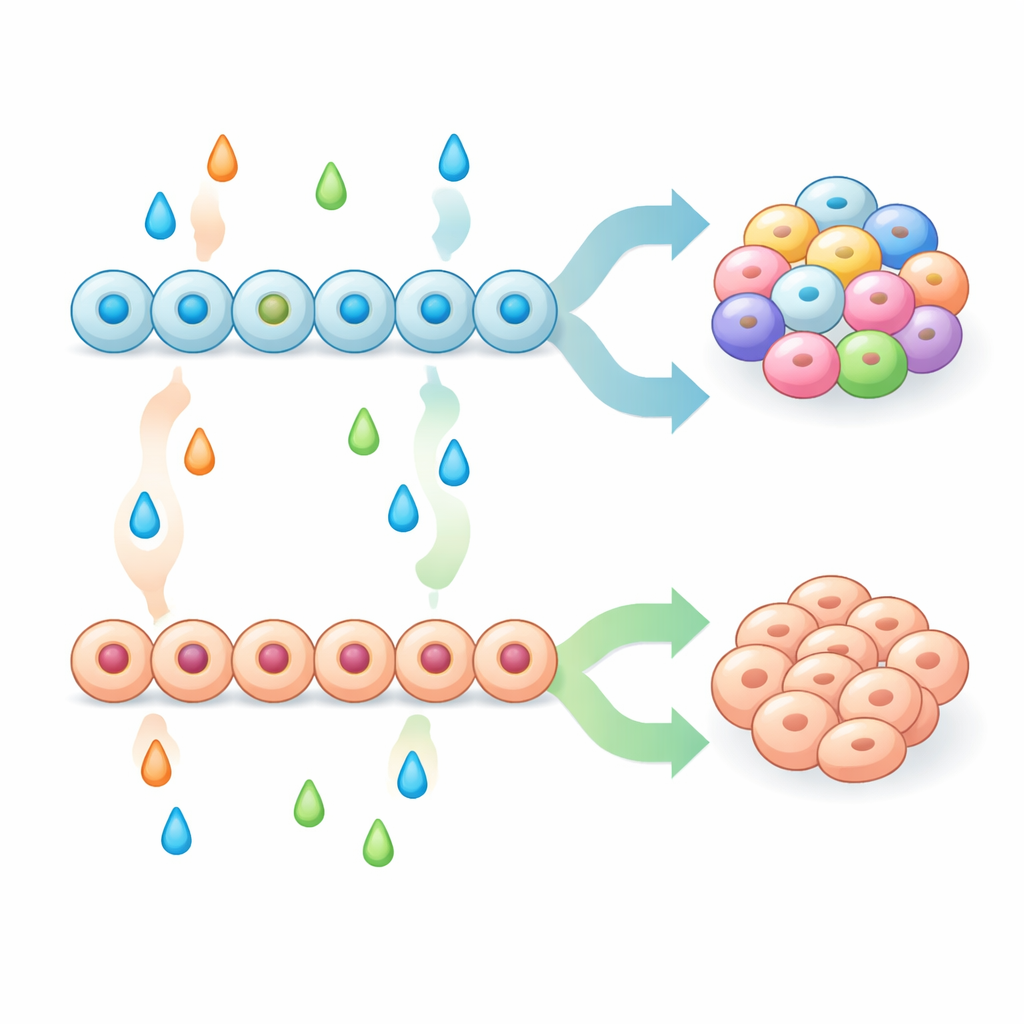
Con una popolazione di progenitori pancreatici più solida, il gruppo ha testato sistematicamente combinazioni di molecole di segnalazione nelle fasi successive per vedere come modellavano la miscela finale dei tipi cellulari endocrini. Alcuni trattamenti, inclusi inibitori delle vie MAPK/ERK e BMP, spingevano fortemente i progenitori verso cellule simili alle enterochromaffini, mentre altri, come i fattori di crescita FGF2, betacellulina e BMP4, sopprimevano queste cellule e favorivano invece tipi pancreatici classici come cellule alfa, beta e delta. Hanno dimostrato che aumentare semplicemente, nelle fasi iniziali, un marker pancreatico noto come NKX6-1 non era sufficiente a prevenire la comparsa di cellule simili alle enterochromaffini. Piuttosto, l’esito dipendeva da un’interazione tra il patterning precoce (come i progenitori erano stati preparati) e il patterning tardivo (i segnali ricevuti durante l’impegno endocrino). Mescolando e abbinando questi passaggi, i ricercatori hanno creato protocolli che generavano o grappoli simili alle isole arricchiti in cellule beta con forte secrezione di insulina stimolata dal glucosio, o grappoli altamente arricchiti in cellule simili alle enterochromaffini.
Indizi dai modelli murini e dall’attività genica
Per verificare se i tessuti pancreatici hanno naturalmente la capacità di produrre cellule simili alle enterochromaffini, il team ha esaminato topi ingegnerizzati per perdere un gene regolatore chiave, Isl1, nelle cellule endocrine in sviluppo. In questi animali, le isole contenevano molte cellule con caratteristiche di enterochromaffini, inclusa la produzione di serotonina e l’espressione del trasportatore SLC18A1. Il profilo genico a singola cellula sia nei topi sia nelle isole derivate da cellule staminali umane ha rivelato che queste cellule pancreatiche simili alle enterochromaffini condividono molti tratti molecolari con le enterochromaffini intestinali, ma presentano anche segni distintivi pancreatici come NKX6-1 e geni correlati all’insulina. Una caratteristica comune sorprendente era l’attività prolungata del fattore di trascrizione Neurogenin 3 (NGN3), che normalmente si attiva solo per un breve periodo durante lo sviluppo endocrino. Nella linea simile alle enterochromaffini, NGN3 restava attivo più a lungo, sia nei sistemi murini sia in quelli umani, suggerendo che la tempistica di questo fattore chiave potrebbe contribuire a decidere se un progenitore diventi una cellula delle isole pancreatiche o una cellula simile alle enterochromaffini.
Progettare aggregati cellulari per terapia e ricerca
Mappando come il priming precoce e i segnali tardivi interagiscono, questo lavoro offre una mappa per progettare cluster endocrini “su misura” a partire da cellule staminali umane. Per l’uso terapeutico nel diabete, i protocolli che minimizzano le cellule simili alle enterochromaffini e massimizzano le cellule beta mature dovrebbero produrre innesti più sicuri e prevedibili con migliori risposte insuliniche. Al contrario, la capacità di generare grandi popolazioni pure di cellule simili alle enterochromaffini a partire da progenitori pancreatici apre una nuova via per studiare le cellule intestinali produttrici di serotonina e le relative patologie. In termini semplici, lo studio mostra che i modelli pancreatici derivati da cellule staminali non sono condannati a risultati casuali: con segnali chimici scelti con cura nei momenti giusti, gli scienziati possono inclinare l’equilibrio verso i tipi cellulari desiderati e lontano da quelli indesiderati.
Citazione: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Parole chiave: isole derivate da cellule staminali, sostituzione delle cellule beta, cellule enterochromaffini, progenitori pancreatici, diabete di tipo 1