Clear Sky Science · ru
Эффективное управление дифференцировкой энтерохромаффинных и островковых клеток из панкреатических предшественников, полученных от плюрипотентных стволовых клеток человека
Превращение стволовых клеток в индивидуальные фабрики по производству инсулина
Для людей с сахарным диабетом 1 типа замена утраченых инсулин-продуцирующих клеток поджелудочной железы однажды может избавить от необходимости делать инъекции инсулина. Ученые уже умеют направлять человеческие стволовые клетки на формирование миниатюрных панкреатических кластеров, напоминающих природные «островки», где синтезируется инсулин, но эти лабораторные островки — смесь разных клеток: наряду с желанными инсулин-продуцирующими клетками часто появляются нежелательные типы. В этом исследовании поставлен практический вопрос с важными последствиями для будущих терапий: можно ли надежно направлять стволовые клетки в нужные панкреатические типы и при этом ограничивать появление побочных клеток?
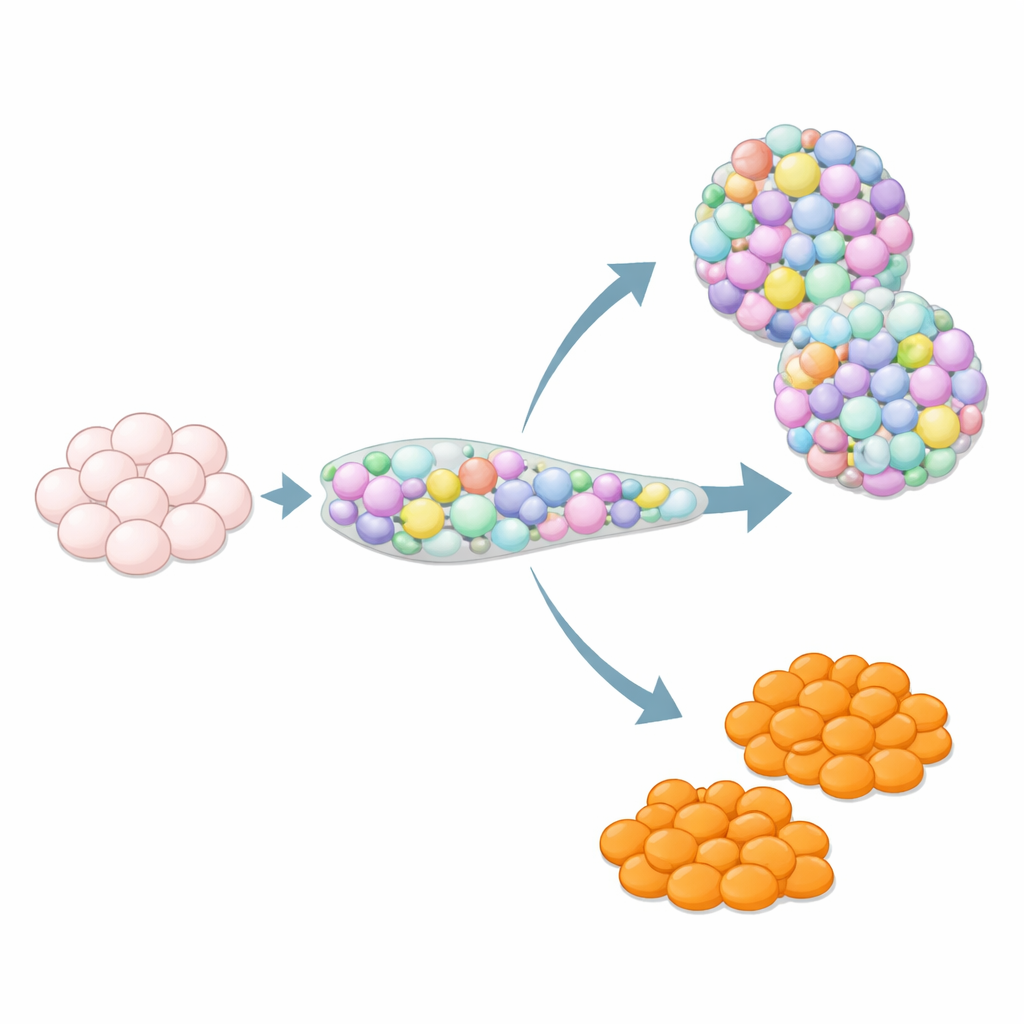
Почему дополнительные типы клеток могут быть скрытой проблемой
Когда стволовые клетки направляют на формирование панкреатической ткани, они не всегда действуют по сценарию. Среди «непрошенных гостей» оказываются клетки, похожие на энтерохромаффинные клетки — редкий тип клеток кишечника, который обычно находится в желудке и кишечнике и участвует в контроле моторики и сигнализации ЖКТ, выделяя серотонин. В островках, полученных из стволовых клеток, такие энтерохромаффиноподобные клетки появляются часто, хотя в нормальных человеческих панкреатических островках их нет. Их влияние на функциональность и безопасность островков пока неясно, поэтому многие исследователи рассматривают их как загрязнение. В то же время, поскольку настоящим органоидам кишечника иногда трудно дать достаточно энтерохромаффинных клеток, эти побочные клетки могли бы представлять ценность для изучения биологии кишечника — при условии, что ученые смогут контролировать их появление.
Создание лучшей начальной точки
Авторы начали с улучшения самых ранних этапов превращения человеческих плюрипотентных стволовых клеток в «примитивную полоску», а затем — в дефинитивный энтодерм, ткань, из которой в итоге развиваются поджелудочная железа и другие органы. Они обнаружили, что кратковременное нарушение внутреннего цитоскелета с помощью соединения латрункулин A делает этот первый переход более надежным, особенно в плотных культурах, которые обычно реагируют плохо. Эта корректировка дала более однородный ранний энтодерм и, далее по цепочке, больше панкреатических предшественников и бета-подобных клеток, продуцирующих инсулин. Важно, что та же ранняя модификация улучшала и формирование других линий, происходящих из энтодермы, таких как легочные и мезодермальные клетки, что указывает на широко применимый способ уменьшить вариабельность при дифференцировке стволовых клеток.
Направление судьбы: панкреатические против кишечноподобных клеток
Имея более сильную исходную популяцию панкреатических предшественников, команда систематически тестировала сочетания сигнальных молекул на поздних этапах, чтобы выяснить, как они формируют окончательный состав эндокринных клеток. Некоторые обработки, включая ингибиторы путей MAPK/ERK и BMP, сильно сдвигали предшественников в сторону энтерохромаффиноподобных клеток, тогда как другие, такие как факторы роста FGF2, бетацеллутин и BMP4, подавляли эти клетки и вместо них способствовали классическим панкреатическим типам — альфа-, бета- и дельта-клеткам. Авторы показали, что простое повышение раннего уровня хорошо известного панкреатического маркера NKX6-1 было недостаточно, чтобы предотвратить появление энтерохромаффиноподобных клеток. Вместо этого результат зависел от взаимодействия между ранним «распределением» (как предшественники были запрограммированы) и поздним «распределением» (сигналами, которые они получали во время эндокринной кляссификации). Подбирая и комбинируя эти этапы, исследователи создали рецептуры, которые давали либо обогащенные бета-клетками островкообразные кластеры с сильной глюкозозависимой секрецией инсулина, либо кластеры с высоким содержанием энтерохромаффиноподобных клеток.
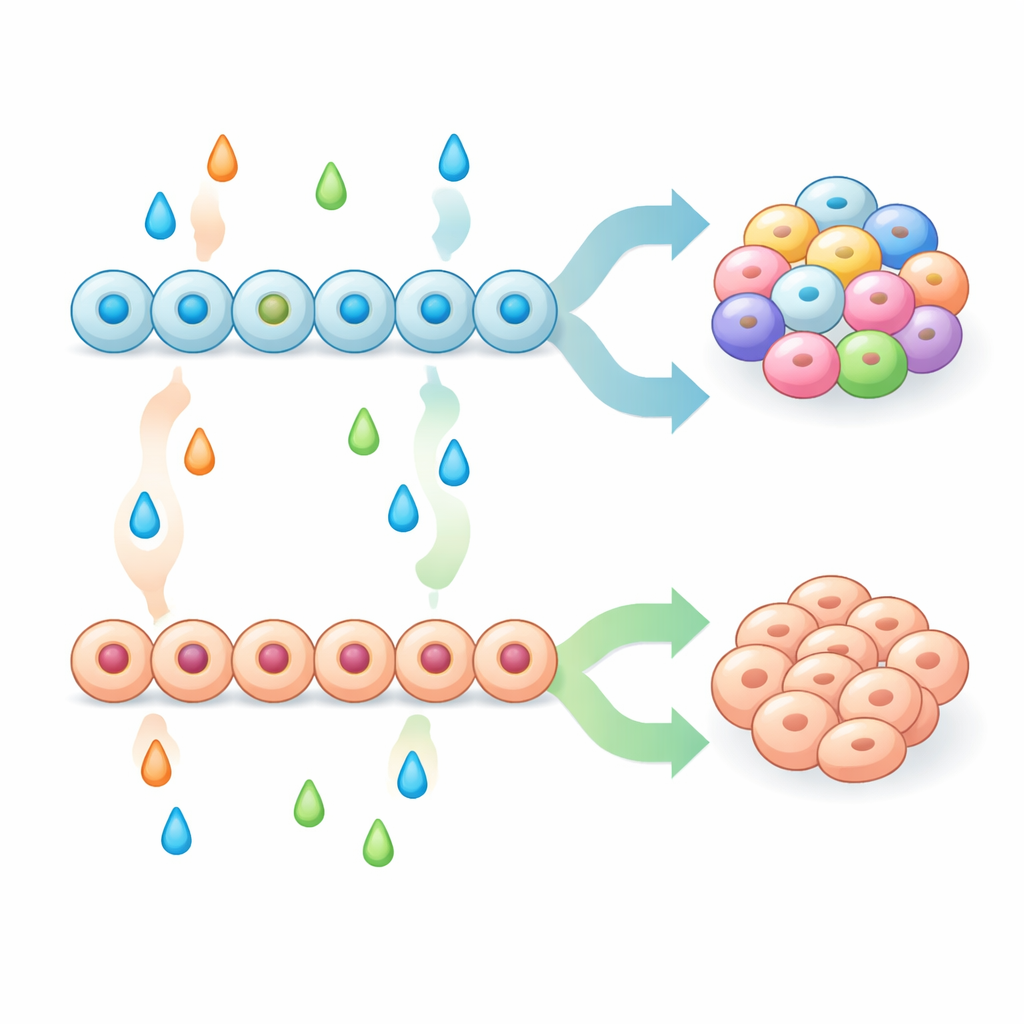
Подсказки от моделей на мышах и активности генов
Чтобы проверить, есть ли у панкреатической ткани природная способность производить энтерохромаффиноподобные клетки, команда изучила мышей, в которых был направленно удален ключевой регуляторный ген Isl1 в развивающихся эндокринных клетках. У этих животных в островках находилось много клеток с признаками энтерохромаффинных клеток, включая продукцию серотонина и экспрессию транспортера SLC18A1. Единоклеточный профиль экспрессии генов как у мышей, так и в островках, полученных из человеческих стволовых клеток, показал, что эти панкреатические энтерохромаффиноподобные клетки разделяют многие молекулярные черты с кишечными энтерохромаффинными клетками, но также несут панкреатические характеристики, такие как NKX6-1 и гены, связанные с инсулином. Поразительной общей чертой была продолжительная активность транскрипционного фактора Neurogenin 3 (NGN3), который обычно включается лишь кратко во время эндокринного развития. В энтерохромаффиноподобной линии NGN3 оставался активным дольше, как в мышиных, так и в человеческих системах, что намекает на то, что временные характеристики этого ключевого фактора могут помочь решить, станет ли предшественник клеткой панкреатического островка или энтерохромаффиноподобной клеткой.
Проектирование клеточных кластеров для терапии и исследований
Отображая взаимодействие ранней подготовки и поздних сигнальных подсказок, эта работа предлагает план по созданию «на заказ» эндокринных кластеров из человеческих стволовых клеток. Для терапевтического применения при диабете протоколы, минимизирующие наличие энтерохромаффиноподобных клеток и максимизирующие зрелые бета-подобные клетки, должны приводить к более безопасным и предсказуемым трансплантатам с лучшим инсулиновым ответом. Напротив, способность генерировать большие чистые популяции энтерохромаффиноподобных клеток из панкреатических предшественников открывает новый путь для изучения серотонин-продуцирующих клеток кишечника и связанных с ними заболеваний. Проще говоря, исследование показывает, что модели поджелудочной железы, полученные из стволовых клеток, не обречены на случайные исходы: при правильно выбранных химических сигналах в нужное время ученые могут склонить баланс в сторону желанных типов клеток и отвести его от нежеланных.
Цитирование: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Ключевые слова: островки, полученные из стволовых клеток, замена бета-клеток, энтерохромаффинные клетки, панкреатические предшественники, сахарный диабет 1 типа