Clear Sky Science · pl
Efektywna kontrola różnicowania komórek enterochromafinowych versus wysepek trzustkowych z ludzkich pluripotentnych komórek macierzystych pochodzących z progenitorów trzustkowych
Przekształcanie komórek macierzystych w szyte na miarę fabryki insuliny
Dla osób z cukrzycą typu 1 zastąpienie utraconych komórek produkujących insulinę w trzustce mogłoby kiedyś uwolnić je od zastrzyków z insuliną. Naukowcy potrafią już skłaniać ludzkie komórki macierzyste do tworzenia miniaturowych skupisk trzustkowych przypominających fabryki insuliny w organizmie, lecz te hodowane w laboratorium „wyspy” są mieszanką: obok pożądanych komórek produkujących insulinę często pojawiają się niechciane typy komórek. W badaniu zadano praktyczne pytanie o duże znaczenie dla przyszłych terapii: czy można wiarygodnie ukierunkować komórki macierzyste na pożądane typy trzustkowe przy jednoczesnym ograniczeniu komórek poza celem?
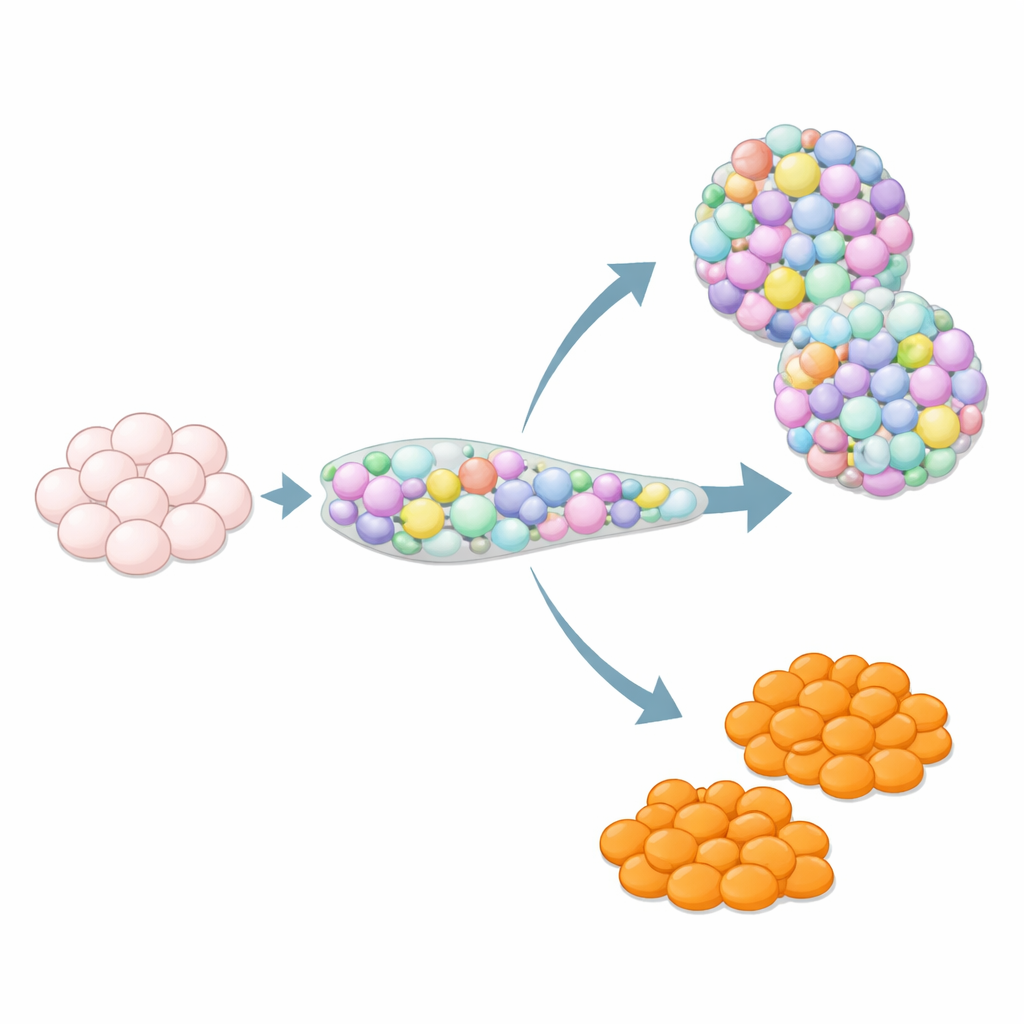
Dlaczego dodatkowe typy komórek mogą być ukrytym problemem
Gdy komórki macierzyste są kierowane ku tkance trzustki, nie zawsze trzymają się scenariusza. Wśród niespodziewanych gości pojawiają się komórki przypominające enterochromafinowe, rzadki typ komórek jelitowych, który normalnie występuje w żołądku i jelicie i pomaga kontrolować ruchy jelit oraz sygnalizację przez uwalnianie serotoniny. W wyspach pochodzących z komórek macierzystych komórki podobne do enterochromafinowych pojawiają się często, mimo że nie są częścią normalnych ludzkich wysepek trzustkowych. Ich wpływ na funkcjonowanie i bezpieczeństwo wysp jest niepewny, dlatego wielu badaczy traktuje je jako zanieczyszczenia. Jednocześnie, ponieważ prawdziwe organoidy jelitowe często mają trudności z wytworzeniem wystarczającej liczby komórek enterochromafinowych, te komórki poza celem mogą być cenne do badania biologii jelit — o ile naukowcy potrafią kontrolować, kiedy się pojawiają.
Budowanie lepszego punktu startowego
Autorzy zaczęli od udoskonalenia najwcześniejszych etapów przekształcania ludzkich pluripotentnych komórek macierzystych w „wstęgę pierwotną”, a następnie w endodermę definitywną, tkankę, z której ostatecznie powstaje trzustka i inne narządy. Stwierdzili, że krótkotrwałe zakłócenie wewnętrznego rusztowania komórek za pomocą związku zwanego latrunculiną A uczyniło ten pierwszy przejściowy etap bardziej solidnym, zwłaszcza w gęsto wysianych hodowlach, które zwykle reagują słabo. Ta modyfikacja dała bardziej jednorodną wczesną endodermę, a w dalszym etapie więcej progenitorów trzustkowych i komórek przypominających beta produkujących insulinę. Co ważne, ta sama wczesna korekta poprawiła także formowanie innych linii pochodzących z endodermy, takich jak komórki płucne i mezodermalne, co sugeruje szeroko użyteczny sposób redukcji zmienności w różnicowaniu komórek macierzystych.
Kierowanie losu: komórki trzustkowe kontra przypominające jelitowe
Mając silniejszą populację progenitorów trzustkowych, zespół systematycznie testował kombinacje molekuł sygnałowych na późniejszych etapach, aby sprawdzić, jak kształtują one końcowy skład typów komórek endokrynnych. Niektóre zabiegi, w tym inhibitory ścieżek MAPK/ERK i BMP, silnie przesuwały progenitory w kierunku komórek podobnych do enterochromafinowych, podczas gdy inne, takie jak czynniki wzrostu FGF2, betacellulina i BMP4, hamowały te komórki i zamiast tego faworyzowały klasyczne typy trzustkowe, takie jak komórki alfa, beta i delta. Wykazali, że samo wczesne zwiększenie dobrze znanego markera trzustkowego NKX6-1 nie wystarczyło, by zapobiec pojawieniu się komórek podobnych do enterochromafinowych. Wynik zależał raczej od interakcji między wczesnym wzorcowaniem (jak progenitory zostały uprzednio przygotowane) a późnym wzorcowaniem (sygnały, które otrzymały podczas zobowiązania endokrynnego). Mieszając i dopasowując te etapy, badacze stworzyli przepisy dające albo skupiska przypominające wyspy bogate w komórki beta z silnym wydzielaniem insuliny w odpowiedzi na glukozę, albo skupiska silnie wzbogacone w komórki podobne do enterochromafinowych.
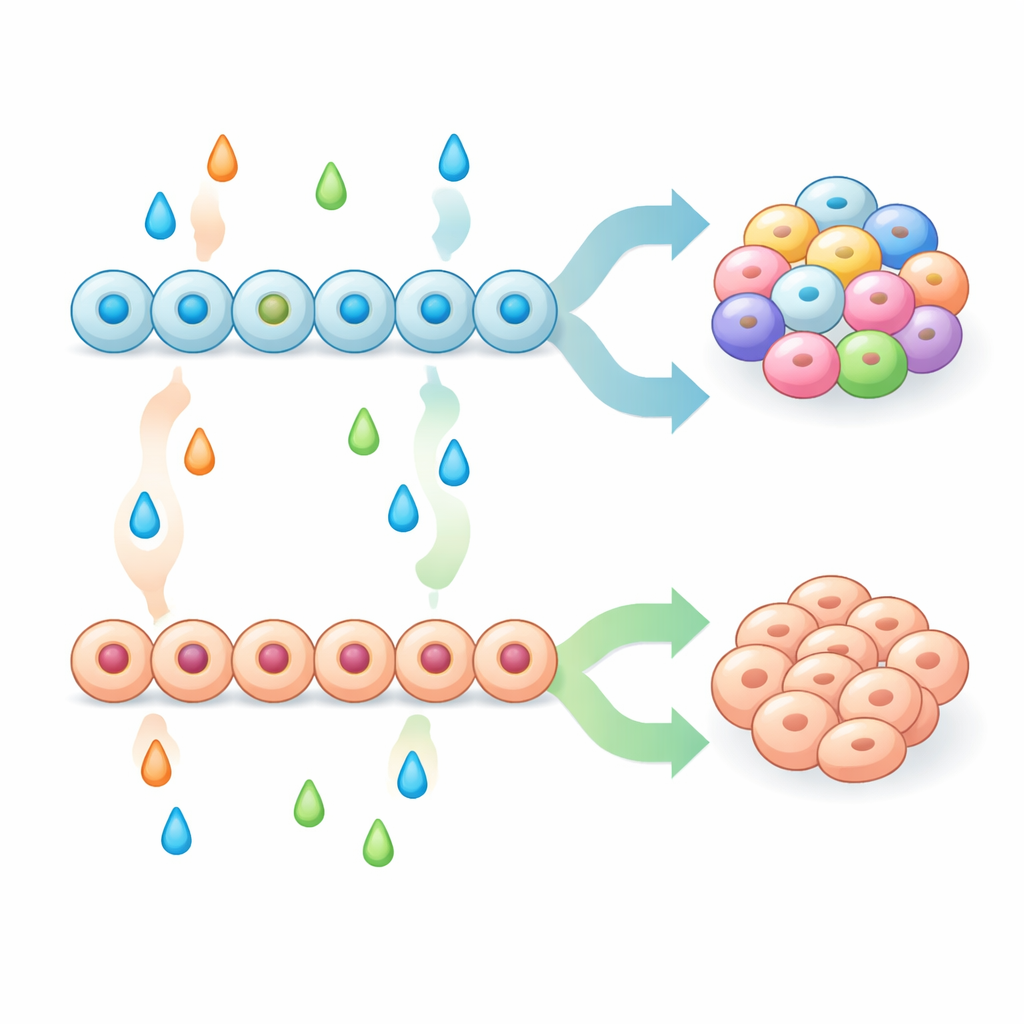
Wskazówki z modeli mysich i aktywności genów
Aby sprawdzić, czy tkanki trzustkowe mają naturalną zdolność do wytwarzania komórek podobnych do enterochromafinowych, zespół zbadał myszy zaprojektowane tak, by traciły kluczowy gen regulacyjny Isl1 w rozwijających się komórkach endokrynnych. U tych zwierząt wyspy zawierały wiele komórek z cechami komórek enterochromafinowych, w tym produkcję serotoniny i ekspresję transportera SLC18A1. Profilowanie genów pojedynczych komórek zarówno u myszy, jak i w wyspach pochodzących z ludzkich komórek macierzystych wykazało, że te trzustkowe komórki podobne do enterochromafinowych dzielą wiele cech molekularnych z jelitowymi komórkami enterochromafinowymi, ale także noszą trzustkowe znaki rozpoznawcze, takie jak NKX6-1 i geny związane z insuliną. Uderzającą wspólną cechą była przedłużona aktywność czynnika transkrypcyjnego Neurogenin 3 (NGN3), który normalnie włącza się tylko krótko podczas rozwoju endokrynnego. W linii podobnej do enterochromafinowej NGN3 pozostawał aktywny dłużej, zarówno w systemach mysich, jak i ludzkich, co sugeruje, że timing tego kluczowego czynnika może pomagać zdecydować, czy progenitor stanie się komórką wysepki trzustkowej czy komórką podobną do enterochromafinowej.
Projektowanie skupisk komórek do terapii i badań
Mapując, jak wczesne przygotowanie i późne sygnały oddziałują, ta praca oferuje mapę drogową do projektowania „na zamówienie” skupisk endokrynnych z ludzkich komórek macierzystych. Do zastosowań terapeutycznych w cukrzycy protokoły minimalizujące komórki podobne do enterochromafinowych i maksymalizujące dojrzałe komórki przypominające beta powinny dawać bezpieczniejsze, bardziej przewidywalne przeszczepy z lepszą odpowiedzią insulinową. Z kolei zdolność do generowania dużych, czystych populacji komórek podobnych do enterochromafinowych z progenitorów trzustkowych otwiera nową drogę do badań nad komórkami jelitowymi produkującymi serotoninę i ich chorobami. Mówiąc prosto, badanie pokazuje, że modele trzustki pochodzące z komórek macierzystych nie są skazane na losowe wyniki: przy starannie dobranych sygnałach chemicznych we właściwych momentach naukowcy mogą przechylić równowagę w stronę pożądanych typów komórek i z dala od niechcianych.
Cytowanie: Misra, P.S., McGaugh, E.C., Huang, H. et al. Efficient control of enterochromaffin versus islet differentiation from human pluripotent stem cell-derived pancreatic progenitors. Nat Commun 17, 4137 (2026). https://doi.org/10.1038/s41467-026-70666-y
Słowa kluczowe: wyspy pochodzące z komórek macierzystych, zastępowanie komórek beta, komórki enterochromafinowe, progenitory trzustkowe, cukrzyca typu 1