Clear Sky Science · zh
一种通过MFS三元复合体跨越革兰氏阴性菌两层膜的药物转运模型
为什么细菌中的微小泵很重要
抗生素抗性常归结为药物与细菌防御之间的显微级军备竞赛。一个强有力的防御是一些微小的泵,在抗生素造成伤害之前将其从细胞内排出。本研究揭示了大肠杆菌中名为EmrAB-TolC的此类泵的详细结构与工作模型。通过展示这个装置如何贯穿细胞的两层保护层并以一步方式排出药物,研究为破坏细菌防御、提高现有药物效力提供了新思路。
将药物送入坚固细菌的挑战
许多致病细菌被两层膜包裹,中间有一层水相空间。这个双重屏障使抗生素难以到达靶点。革兰氏阴性菌还构建分子机器,识别细胞内的有害化合物并将其排出。EmrAB-TolC就是其中之一,能处理多种抗生素。直到现在,科学家们只掌握了其各个部分的局部快照。最大的未知是这些部件如何组装在一起,以及泵如何协调地将药物完整地穿过两层膜。
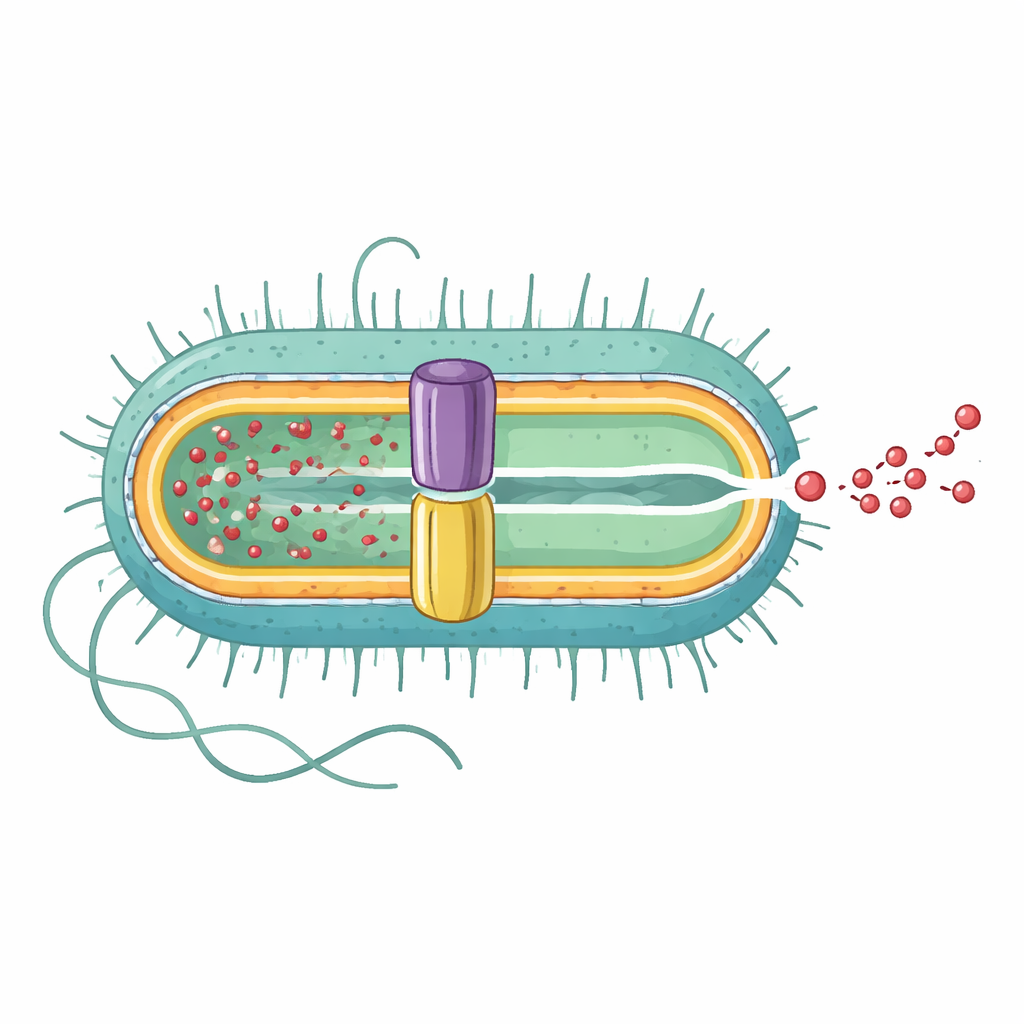
从内到外揭示完整泵结构
研究团队使用高分辨率冷冻电子显微镜确定了完整EmrAB-TolC泵的三维结构。他们发现该复合体呈细长结构,由三部分按3:6:1的比例组成:外膜通道TolC的三个拷贝、中间连接蛋白EmrA的六个拷贝,以及内膜转运体EmrB的单个拷贝。它们共同形成一条约320埃长的连续隧道,从内膜穿过膜间空间延伸至细胞外。EmrA在TolC和EmrB之间形成一个六角形护套,塑造了中心纳米通道,而TolC在与EmrA相接处张开,形成通向细胞外的直接出口。
为药物外排提供动力的内部引擎
复合体基部是EmrB,它属于一类利用质子流(定义酸性的带电粒子)来驱动货物移动的大家族转运蛋白。EmrB含有14个跨膜螺旋,排列为两个相互摆动的结构域。结构分析与计算模拟显示,一个关键的酸性残基D29及其相邻残基构成了一个对质子敏感的网络,能够在内向开放态与外向开放态之间切换。D29和附近位点的突变会显著降低细胞对多种抗生素的耐受性,这突出了它们在将质子运动耦合到药物转运中的重要性,尽管质子流也可能涉及其他残基。
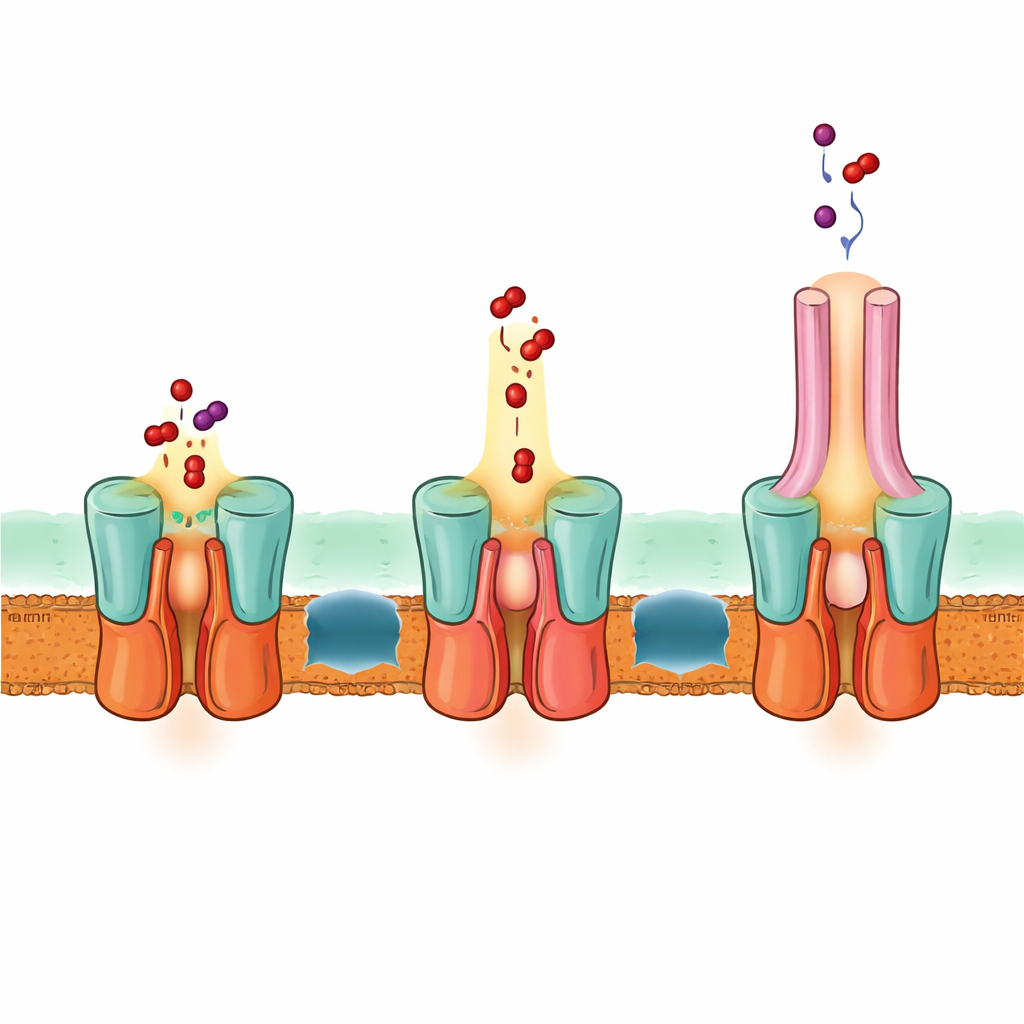
跨越两层膜的一步逃逸通路
该结构还解释了EmrA与EmrB如何相接以形成密闭的通道。EmrB外周腹膜侧的一组延伸螺旋束插入EmrA的环状区域,将转运体与连接蛋白锁定在一起。这种构型产生了一个宽敞的腔室,能够接纳从EmrB释放的药物并将其引导进入EmrA通道,随后进入TolC。基于结构、计算预测和突变学测试,作者提出EmrB从内膜或胞质中捕获药物,然后通过摆动向EmrA方向开启并将药物释放到这个共享腔室中。EmrA内的一段柔性环形成一条狭窄通道,将药物向上引导通过连接蛋白并经TolC排出,整个过程中药物并未在膜间空间内自由弥散。
这对抗击耐药性的意义
总体而言,该工作支持这样一种模型:EmrAB-TolC可实现将抗生素从细胞内直接一步性地外排到外界。该泵利用质子通量驱动EmrB的反复构象变化,进而将药物推入由EmrA和TolC形成的连续通道。通过定位对组装和功能至关重要的结构特征,例如EmrA中的疏水环和EmrB的关键残基,研究强调了可能被小分子“卡住”泵的薄弱点。针对这些位点的抑制策略可能有助于恢复现有抗生素对目前耐药的革兰氏阴性病原体的效力。
引用: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
关键词: 抗生素抗性, 外排泵, 革兰氏阴性菌, 药物转运, EmrAB-TolC