Clear Sky Science · pl
Model transportu leków przez dwie błony bakterii Gram-ujemnych przez trójskładnikowy kompleks z rodziny MFS
Dlaczego drobne pompy w bakteriach mają znaczenie
Oporność na antybiotyki często sprowadza się do mikroskopijnego wyścigu zbrojeń między lekami a mechanizmami obronnymi bakterii. Jedną z potężnych linii obrony są drobne pompy, które wyrzucają antybiotyki z komórki, zanim zdążą wyrządzić szkody. W tej pracy odsłonięto szczegółową strukturę i model działania jednej takiej pompy, zwanej EmrAB-TolC, w Escherichia coli. Pokazując, jak to urządzenie rozciąga się przez obie warstwy ochronne komórki i usuwa leki w jednym kroku, badanie dostarcza nowych pomysłów na unieszkodliwienie bakterii i zwiększenie skuteczności istniejących leków.
Problem dostarczania leków do opornych bakterii
Wiele groźnych bakterii otoczonych jest nie jedną, lecz dwiema błonami, z wodnistą przestrzenią pośrednią. Ta podwójna powłoka utrudnia antybiotykom dotarcie do celów wewnątrz komórki. Bakterie Gram-ujemne budują też maszyny molekularne, które rozpoznają szkodliwe związki w komórce i usuwają je na zewnątrz. EmrAB-TolC jest jednym z takich układów i radzi sobie z kilkoma różnymi antybiotykami. Dotychczas naukowcy mieli tylko fragmentaryczne obrazy jego poszczególnych części. Dużą niewiadomą było to, jak elementy pasują do siebie i jak pompa koordynuje transport leków przez obie błony.
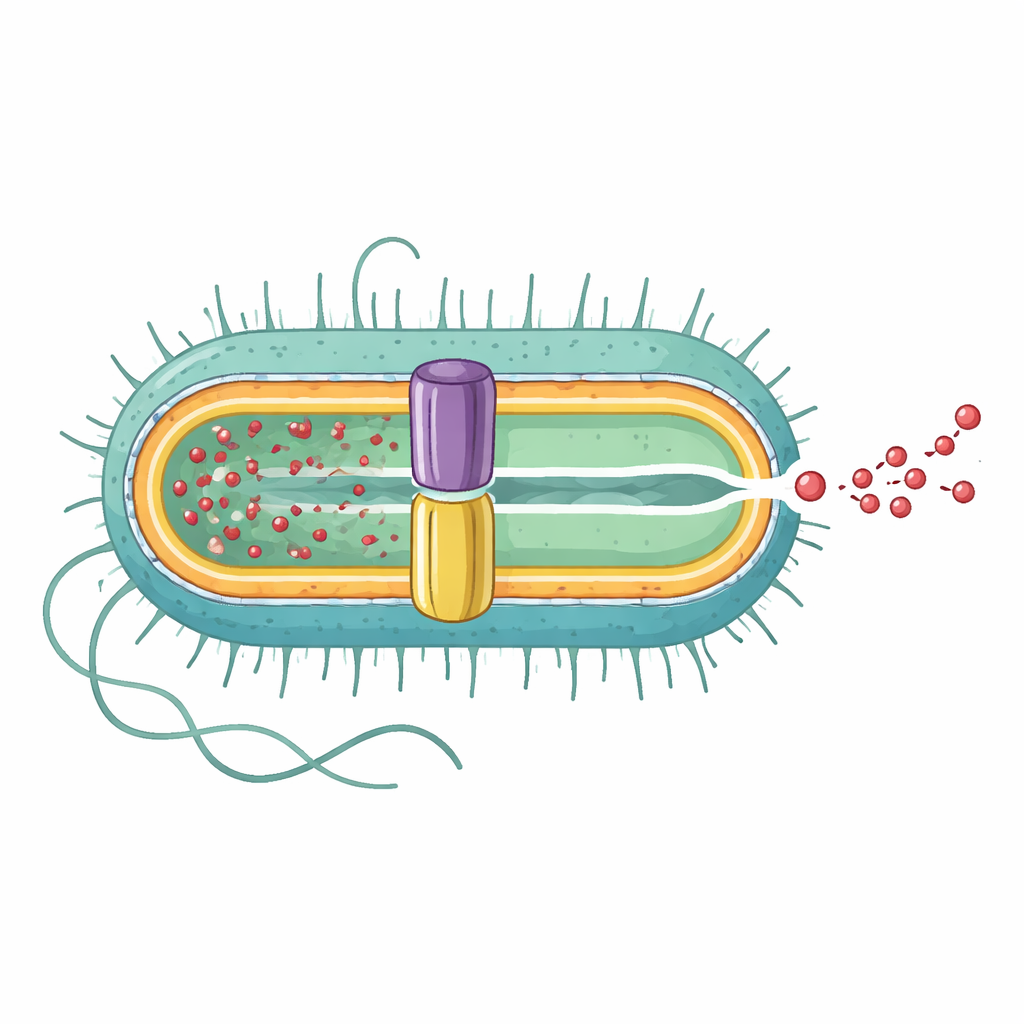
Odkrycie pełnej pompy od wnętrza na zewnątrz
Zespół badawczy wykorzystał wysokorozdzielczą kriomikroskopię elektronową, aby wyznaczyć trójwymiarową strukturę kompletnej pompy EmrAB-TolC. Stwierdzili, że jest to wydłużony kompleks złożony z trzech głównych części w stosunku 3:6:1: trzy kopie zewnętrznego kanału TolC, sześć kopii środkowego białka adapterowego EmrA i pojedyncza kopia wewnątrzbłonowego transportera EmrB. Razem tworzą ciągły tunel o długości około 320 angstremów, sięgający od błony wewnętrznej, przez przestrzeń międzybłonową, aż na zewnątrz. EmrA tworzy heksagonalną osłonę między TolC a EmrB, kształtując centralny nano-kanał, podczas gdy TolC szeroko się otwiera tam, gdzie styka się z EmrA, tworząc bezpośrednią drogę wyjściową na zewnątrz komórki.
Wewnętrzny silnik napędzający eksport leków
U podstawy kompleksu znajduje się EmrB, członek dużej rodziny transporterów wykorzystujących przepływ protonów — naładowanych cząstek definiujących kwasowość — do napędu przenoszenia ładunku. EmrB zawiera 14 helis przechodzących przez błonę, zorganizowanych w dwie domeny poruszające się względem siebie. Analizy strukturalne i symulacje komputerowe pokazują, że kluczowy kwaśny resztor, D29, i sąsiednie reszty tworzą sieć wrażliwą na protony, która może przełączać EmrB między stanami otwartymi do wewnątrz i na zewnątrz. Mutacje w D29 i pobliskich pozycjach znacznie obniżają oporność komórki na kilka antybiotyków, co podkreśla ich rolę w sprzęganiu ruchu protonów z transportem leków, choć przepływ protonów może angażować także dodatkowe reszty.
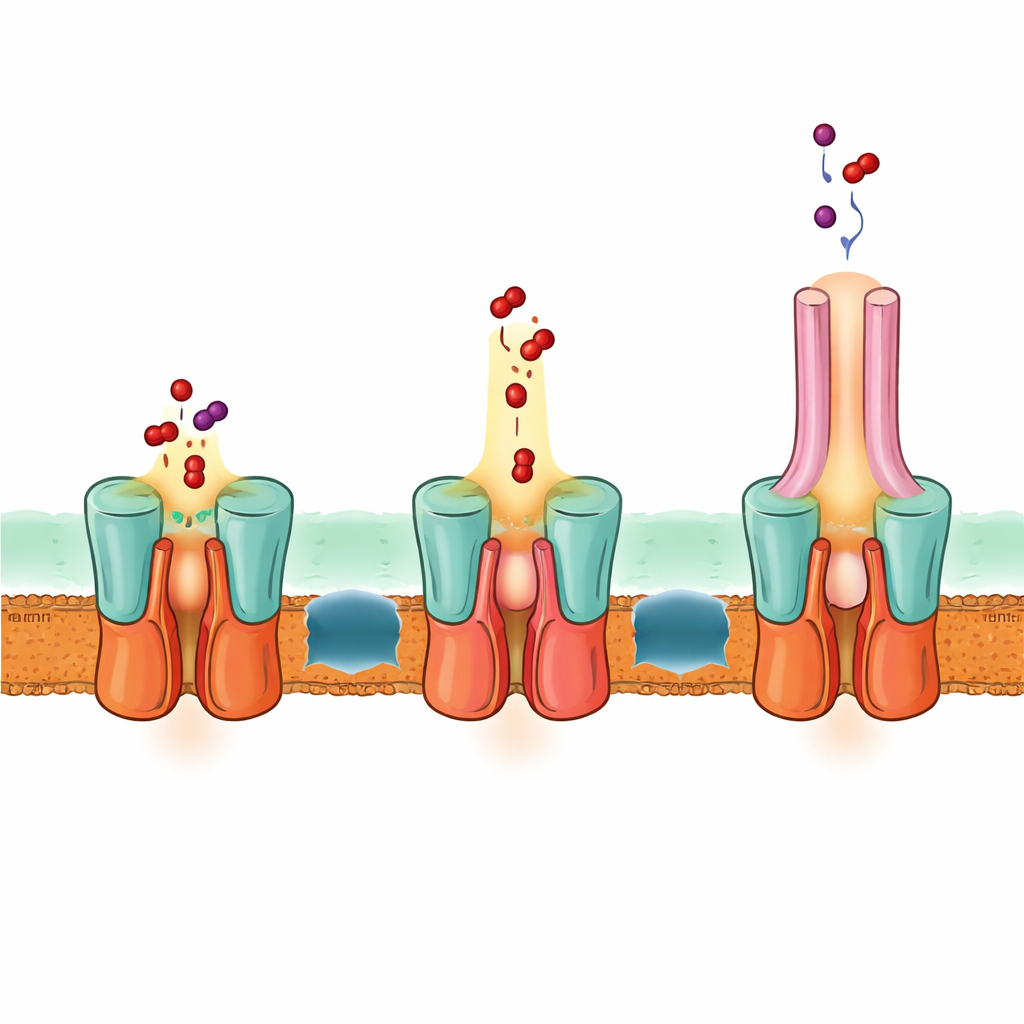
Jednofazowa droga ucieczki przez obie błony
Struktura wyjaśnia także, jak EmrA i EmrB współdziałają, tworząc uszczelniony przewód. Specjalne wydłużone wiązanie helikalne po stronie periplazmatycznej EmrB wpasowuje się w pierścieniowaty obszar EmrA, blokując transporter do adaptera. Takie ułożenie tworzy przestronną jamę, która może przyjmować leki uwolnione z EmrB i kierować je w górę do kanału EmrA, a następnie do TolC. Na podstawie struktury, predykcji komputerowych i testów mutacyjnych autorzy proponują, że EmrB chwyta leki z błony wewnętrznej lub cytoplazmy, następnie kołysze się otwierając w stronę EmrA i uwalnia je do tej wspólnej jamy. Elastyczna pętla w EmrA formuje wąską ścieżkę, która lejekuje leki ku górze przez adapter i na zewnątrz przez TolC, wszystko to bez swobodnej dyfuzji leków w przestrzeni międzybłonowej.
Znaczenie dla walki z opornością
W sumie praca wspiera model, w którym EmrAB-TolC dokonuje faktycznego jednofazowego eksportu antybiotyków bezpośrednio ze środka komórki na zewnątrz. Pompa wykorzystuje przepływ protonów do wywoływania powtarzalnych zmian kształtu EmrB, które z kolei przepychają leki do ciągłego kanału tworzonego przez EmrA i TolC. Identyfikując cechy strukturalne niezbędne dla montażu i funkcji, takie jak hydrofobowe pierścienie w EmrA i kluczowe reszty w EmrB, badanie wskazuje potencjalne słabe punkty, gdzie małe cząsteczki mogłyby zablokować pompę. Celowanie w te miejsca mogłoby pomóc przywrócić skuteczność istniejących antybiotyków wobec patogenów Gram-ujemnych, które obecnie opierają się leczeniu.
Cytowanie: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Słowa kluczowe: oporność na antybiotyki, pompa wypompowująca, bakterie Gram-ujemne, transport leków, EmrAB-TolC