Clear Sky Science · it
Un modello per il trasporto di farmaci attraverso due membrane dei batteri Gram-negativi da parte di un assemblaggio tripartito MFS
Perché le piccole pompe nei batteri contano
La resistenza agli antibiotici spesso si riduce a una corsa agli armamenti microscopica tra i farmaci e le difese batteriche. Una difesa potente è costituita da una serie di minuscole pompe che espellono gli antibiotici dalla cellula prima che possano nuocere. Questo studio svela la struttura dettagliata e il modello di funzionamento di una di queste pompe, chiamata EmrAB-TolC, in Escherichia coli. Dimostrando come questa macchina percorra entrambe le barriere protettive della cellula ed espella i farmaci in un unico passaggio, il lavoro offre nuove idee per disarmare le difese batteriche e rendere più efficaci i farmaci esistenti.
La sfida di far penetrare i farmaci nei batteri resistenti
Molti batteri pericolosi sono avvolti non da una ma da due membrane, con uno spazio acquoso interposto. Questo doppio involucro rende difficile per gli antibiotici raggiungere i loro bersagli. I batteri Gram-negativi costruiscono inoltre macchine molecolari che riconoscono composti dannosi all’interno della cellula e li espellono all’esterno. EmrAB-TolC è una di queste macchine e può gestire diversi antibiotici. Finora gli scienziati avevano solo istantanee parziali delle singole parti. Gli aspetti maggiormente sconosciuti erano come i pezzi si incastrano e come la pompa riesca a muovere i farmaci attraverso entrambe le membrane in modo coordinato.
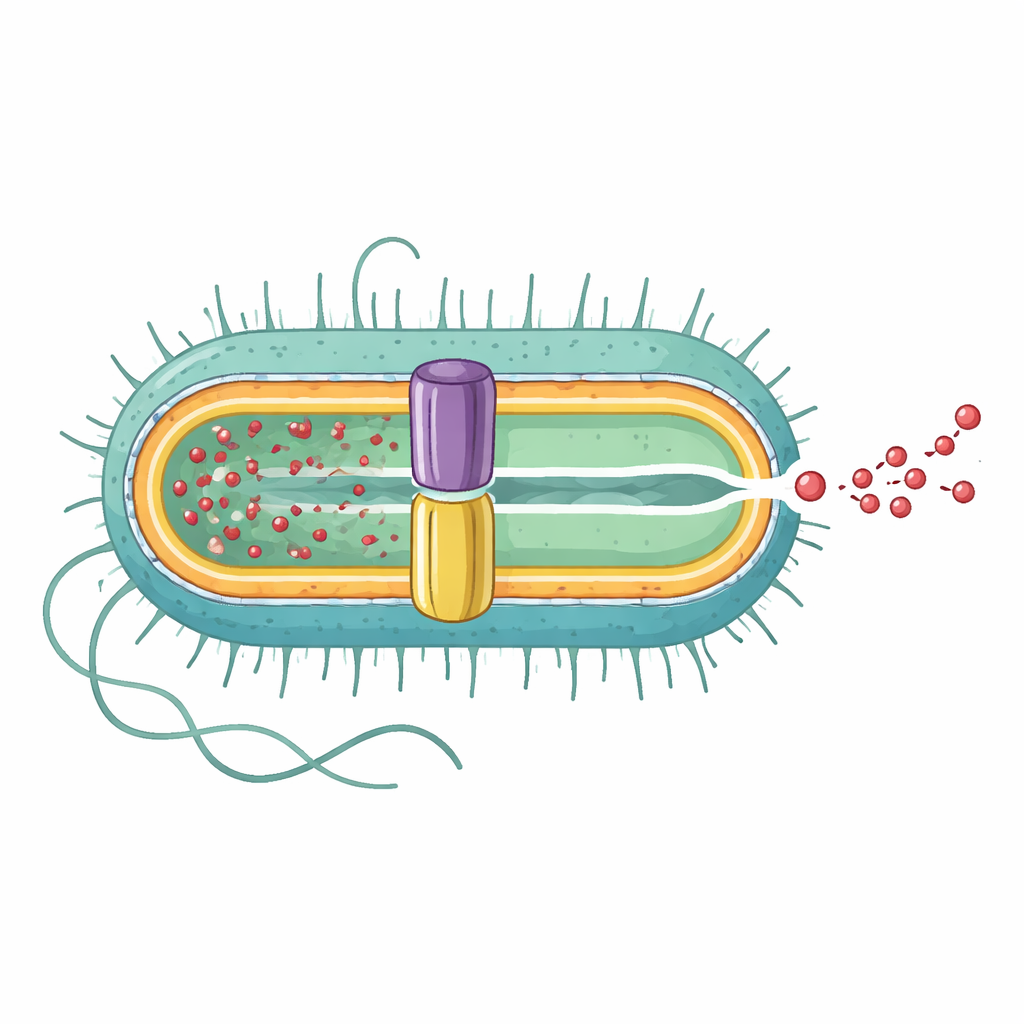
Rivelare la pompa completa dall’interno verso l’esterno
Il team di ricerca ha utilizzato la criomicroscopia elettronica ad alta risoluzione per determinare la struttura tridimensionale della pompa EmrAB-TolC completa. Hanno scoperto che si tratta di un assemblaggio allungato composto da tre parti principali in rapporto 3:6:1: tre copie del canale della membrana esterna TolC, sei copie della proteina adattatrice EmrA e una singola copia del trasportatore di membrana interna EmrB. Insieme formano un tunnel continuo lungo circa 320 angstrom che va dalla membrana interna, attraverso lo spazio periplasmico, fino all’esterno. EmrA forma una guaina esagonale tra TolC ed EmrB, modellando un nano-canale centrale, mentre TolC si apre ampiamente dove incontra EmrA, creando una via di uscita diretta verso l’esterno della cellula.
Il motore interno che alimenta l’esportazione dei farmaci
Alla base dell’assemblaggio si trova EmrB, membro di una grande famiglia di trasportatori che utilizza il flusso di protoni, le particelle cariche che definiscono l’acidità, per alimentare il movimento del carico. EmrB contiene 14 eliche transmembrana disposte in due domini che oscillano l’uno rispetto all’altro. L’analisi strutturale e le simulazioni al computer mostrano che un residuo acido chiave, D29, e i suoi vicini formano una rete sensibile ai protoni che può commutare EmrB tra stati aperti verso l’interno e verso l’esterno. Mutazioni in D29 e nelle posizioni vicine riducono notevolmente la resistenza della cellula a diversi antibiotici, evidenziandone l’importanza nel collegare il movimento dei protoni al trasporto dei farmaci, anche se il flusso protonico può coinvolgere residui aggiuntivi.
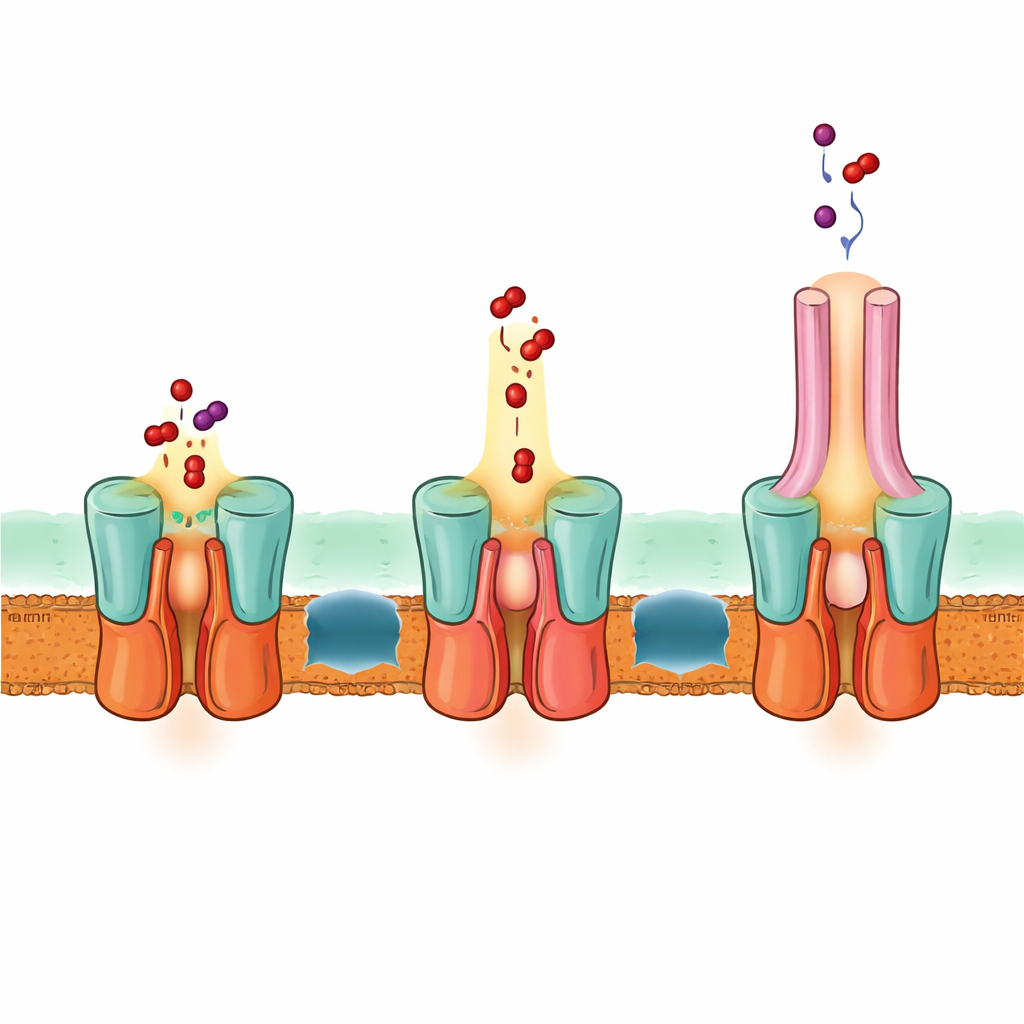
Una via di fuga in un unico passaggio attraverso entrambe le membrane
La struttura spiega anche come EmrA ed EmrB interagiscano per formare un condotto sigillato. Un particolare fascio di eliche esteso sul lato periplasmico di EmrB si inserisce in una regione ad anello di EmrA, bloccando il trasportatore all’adattatore. Questa disposizione crea una cavità spaziosa che può ricevere i farmaci rilasciati da EmrB e guidarli verso l’alto nel canale di EmrA e poi in TolC. Sulla base della struttura, di previsioni computazionali e di test mutazionali, gli autori propongono che EmrB afferri i farmaci dalla membrana interna o dal citoplasma, poi oscilli per aprirsi verso EmrA e rilasciarli in questa cavità condivisa. Un loop flessibile all’interno di EmrA modella un percorso stretto che convoglia i farmaci verso l’alto attraverso l’adattatore e fuori tramite TolC, il tutto senza che i farmaci diffondano liberamente nello spazio tra le membrane.
Cosa significa per la lotta alla resistenza
Nel complesso, il lavoro supporta un modello in cui EmrAB-TolC esegue una vera esportazione in un unico passaggio degli antibiotici, direttamente dall’interno della cellula all’esterno. La pompa usa il flusso di protoni per guidare cambiamenti conformazionali ripetuti in EmrB, che a loro volta spingono i farmaci in un canale continuo formato da EmrA e TolC. Individuando caratteristiche strutturali essenziali per l’assemblaggio e la funzione, come anelli idrofobici in EmrA e residui chiave in EmrB, lo studio mette in luce punti deboli potenziali dove piccole molecole potrebbero inceppare la pompa. Mirare a questi punti potrebbe aiutare a ripristinare l’efficacia degli antibiotici esistenti contro i patogeni Gram-negativi che attualmente resistono al trattamento.
Citazione: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Parole chiave: resistenza agli antibiotici, pompa di efflusso, batteri Gram-negativi, trasporto di farmaci, EmrAB-TolC