Clear Sky Science · de
Ein Modell für den Wirkstofftransport durch zwei Membranen gramnegativer Bakterien mittels einer MFS-Tripartit‑Assemblierung
Warum winzige Pumpen in Bakterien wichtig sind
Antibiotikaresistenz ist oft ein mikroskopischer Wettlauf zwischen Medikamenten und den Abwehrmechanismen von Bakterien. Eine starke Verteidigungslinie sind kleine Pumpen, die Antibiotika aus der Zelle befördern, bevor diese Schaden anrichten können. Diese Studie legt die detaillierte Struktur und ein Arbeitsmodell einer solchen Pumpe, EmrAB-TolC in Escherichia coli, offen. Indem gezeigt wird, wie diese Maschine beide Schutzschichten der Zelle überspannt und Wirkstoffe in einem einzigen Schritt ausstößt, liefert die Arbeit neue Ansätze, um bakterielle Abwehrmechanismen zu schwächen und vorhandene Medikamente wirksamer zu machen.
Die Herausforderung, Wirkstoffe in robuste Bakterien zu bringen
Viele gefährliche Bakterien sind nicht von einer, sondern von zwei Membranen umgeben, mit einem wässrigen Raum dazwischen. Diese doppelte Hülle erschwert es Antibiotika, ihre Ziele zu erreichen. Gramnegative Bakterien bauen zudem molekulare Maschinen, die schädliche Verbindungen im Inneren erkennen und nach außen befördern. EmrAB-TolC ist eine dieser Maschinen und kann mehrere unterschiedliche Antibiotika handhaben. Bislang gab es nur partielle Aufnahmen der einzelnen Komponenten. Die großen Unbekannten waren, wie die Teile zusammenpassen und wie die Pumpe Wirkstoffe koordiniert über beide Membranen hinweg transportiert.
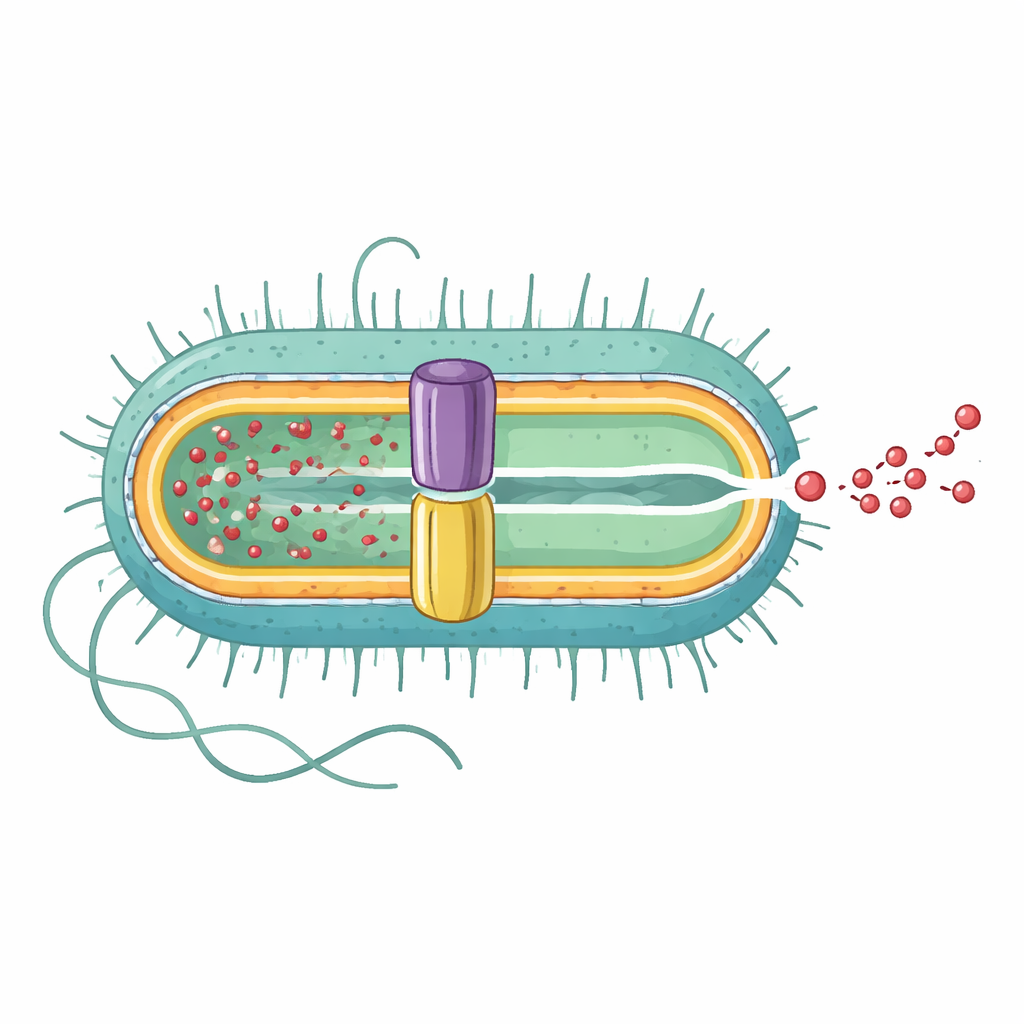
Die komplette Pumpe von innen nach außen enthüllt
Das Forschungsteam nutzte Kryo-Elektronenmikroskopie mit hoher Auflösung, um die dreidimensionale Struktur der vollständigen EmrAB-TolC-Pumpe zu bestimmen. Sie fanden heraus, dass es sich um eine langgestreckte Assemblierung aus drei Hauptteilen im Verhältnis 3:6:1 handelt: drei Kopien des Außenmembrankanals TolC, sechs Kopien des mittleren Adapterproteins EmrA und eine einzelne Kopie des Innenmembrantransporters EmrB. Gemeinsam bilden sie einen durchgehenden Tunnel von etwa 320 Å Länge, der von der Innenmembran durch den periplasmatischen Raum bis nach außen reicht. EmrA bildet eine hexagonale Manschette zwischen TolC und EmrB und gestaltet einen zentralen Nano-Kanal, während TolC dort, wo es auf EmrA trifft, weit öffnet und einen direkten Ausgang zur Zellaußenseite schafft.
Die innere Maschine, die den Wirkstoffexport antreibt
Am Fuß der Assemblierung sitzt EmrB, ein Mitglied einer großen Transporterfamilie, die den Protonenfluss—die geladenen Teilchen, die Säure definieren—nutzt, um den Transport von Fracht zu betreiben. EmrB enthält 14 membranüberspannende Helices, die in zwei Domänen angeordnet sind, die gegeneinander schaukeln. Strukturanalysen und Computersimulationen zeigen, dass ein wichtiges saureres Rest, D29, und seine Nachbarreste ein protonensensitives Netzwerk bilden, das EmrB zwischen inward‑ und outward‑open Zuständen schalten kann. Mutationen in D29 und benachbarten Positionen verringern die Resistenz der Zelle gegenüber mehreren Antibiotika deutlich und unterstreichen ihre Bedeutung bei der Kopplung von Protonenfluss an den Wirkstofftransport, auch wenn der Protonentransfer zusätzliche Reste einbeziehen kann.
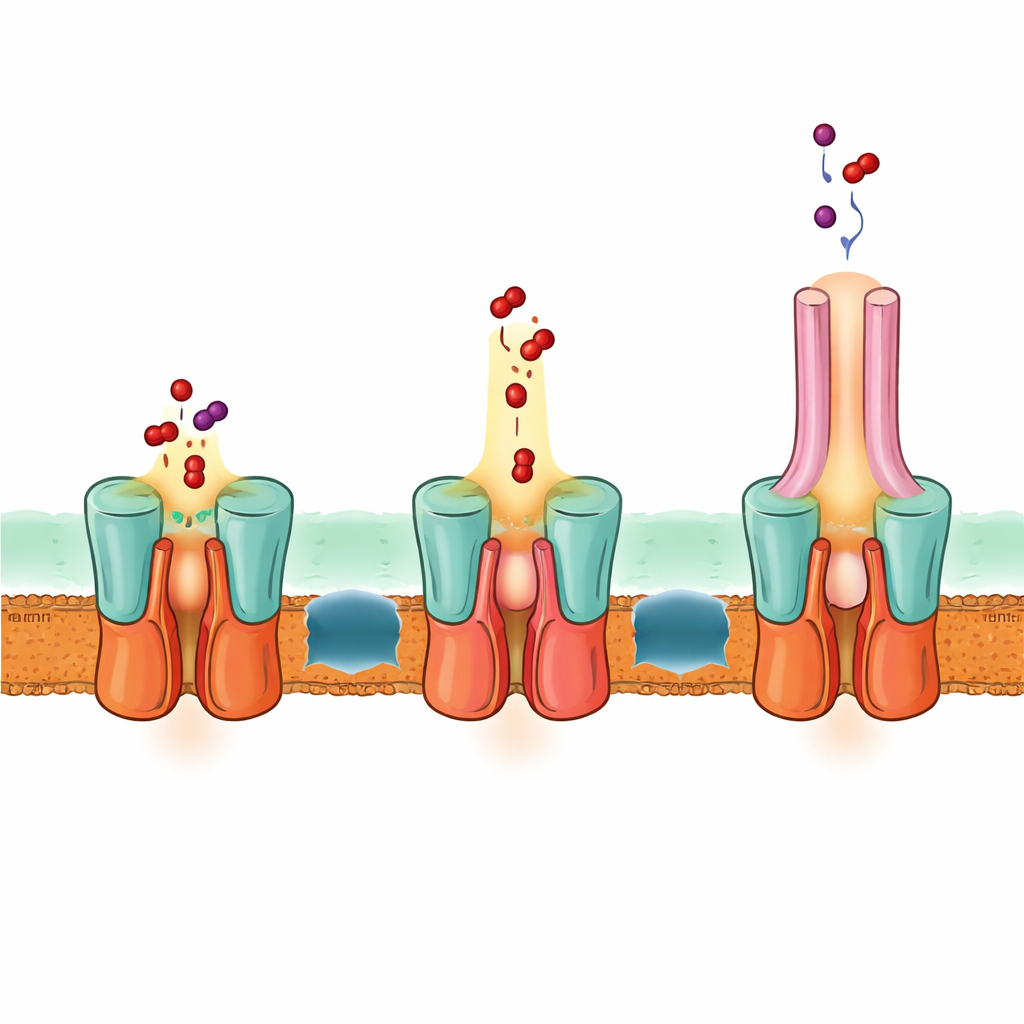
Eine einstufige Fluchtroute durch beide Membranen
Die Struktur erklärt außerdem, wie EmrA und EmrB miteinander interfaced, um einen abgedichteten Kanal zu bilden. Ein speziell verlängerter Helixbündel auf der periplasmatischen Seite von EmrB steckt in eine ringförmige Region von EmrA und verriegelt so den Transporter am Adapter. Diese Anordnung schafft eine geräumige Kavität, die Wirkstoffe aufnehmen kann, die von EmrB freigesetzt werden, und sie in den EmrA‑Kanal und dann in TolC leitet. Basierend auf der Struktur, Computerprognosen und Mutationsversuchen schlagen die Autoren vor, dass EmrB Wirkstoffe aus der Innenmembran oder dem Zytoplasma aufnimmt, dann „aufschaukelt“, um sich in Richtung EmrA zu öffnen und sie in diese gemeinsame Kavität freizusetzen. Eine flexible Schleife innerhalb von EmrA formt einen engen Pfad, der Wirkstoffe durch den Adapter nach oben leitet und durch TolC nach außen befördert, ohne dass die Wirkstoffe jemals frei im Raum zwischen den Membranen diffundieren.
Was das für den Kampf gegen Resistenz bedeutet
Insgesamt stützt die Arbeit ein Modell, in dem EmrAB-TolC einen echten einstufigen Export von Antibiotika direkt von innen nach außen durchführt. Die Pumpe nutzt Protonenfluss, um wiederholte Gestaltsänderungen in EmrB anzutreiben, welche wiederum Wirkstoffe in einen durchgehenden Kanal aus EmrA und TolC schieben. Indem strukturelle Merkmale genau lokalisiert werden, die für Assemblierung und Funktion essentiell sind—wie hydrophobe Ringe in EmrA und Schlüsselreste in EmrB—hebt die Studie potenzielle Schwachstellen hervor, an denen kleine Moleküle die Pumpe blockieren könnten. Das Anvisieren dieser Stellen könnte helfen, die Wirksamkeit existierender Antibiotika gegenüber gramnegativen Krankheitserregern wiederherzustellen, die derzeit Behandlungen widerstehen.
Zitation: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Schlüsselwörter: Antibiotikaresistenz, Effluxpumpe, gramnegative Bakterien, Wirkstofftransport, EmrAB-TolC