Clear Sky Science · sv
En modell för läkemedelstransport över två membran hos Gramnegativa bakterier genom en MFS-trippelmontage
Varför små pumpar i bakterier spelar roll
Antibiotikaresistens handlar ofta om ett mikroskopiskt kapprustningsspel mellan läkemedel och bakteriers försvar. Ett kraftfullt försvar är en uppsättning små pumpar som sparkar ut antibiotika ur cellen innan de kan göra skada. Denna studie avslöjar den detaljerade strukturen och en arbetmodell för en sådan pump, kallad EmrAB-TolC, i Escherichia coli. Genom att visa hur denna maskin sträcker sig över båda cellens skyddande lager och fördriver läkemedel i ett enda steg ger arbetet nya idéer för att oskadliggöra bakteriella försvar och göra befintliga läkemedel mer effektiva.
Utmaningen att få in läkemedel i hårda bakterier
Många farliga bakterier är omslutna av inte ett utan två membran, med ett vattentätt mellanrum däremellan. Detta dubbla hölje gör det svårt för antibiotika att nå sina mål. Gramnegativa bakterier bygger också molekylära maskiner som känner igen skadliga föreningar inne i cellen och skjuter ut dem utanför. EmrAB-TolC är en av dessa maskiner, och den kan hantera flera olika antibiotika. Fram till nu hade forskarna bara partiella ögonblicksbilder av dess enskilda delar. De stora frågorna var hur delarna passar ihop och hur pumpen lyckas flytta läkemedel hela vägen över båda membranen i ett koordinerat förlopp.
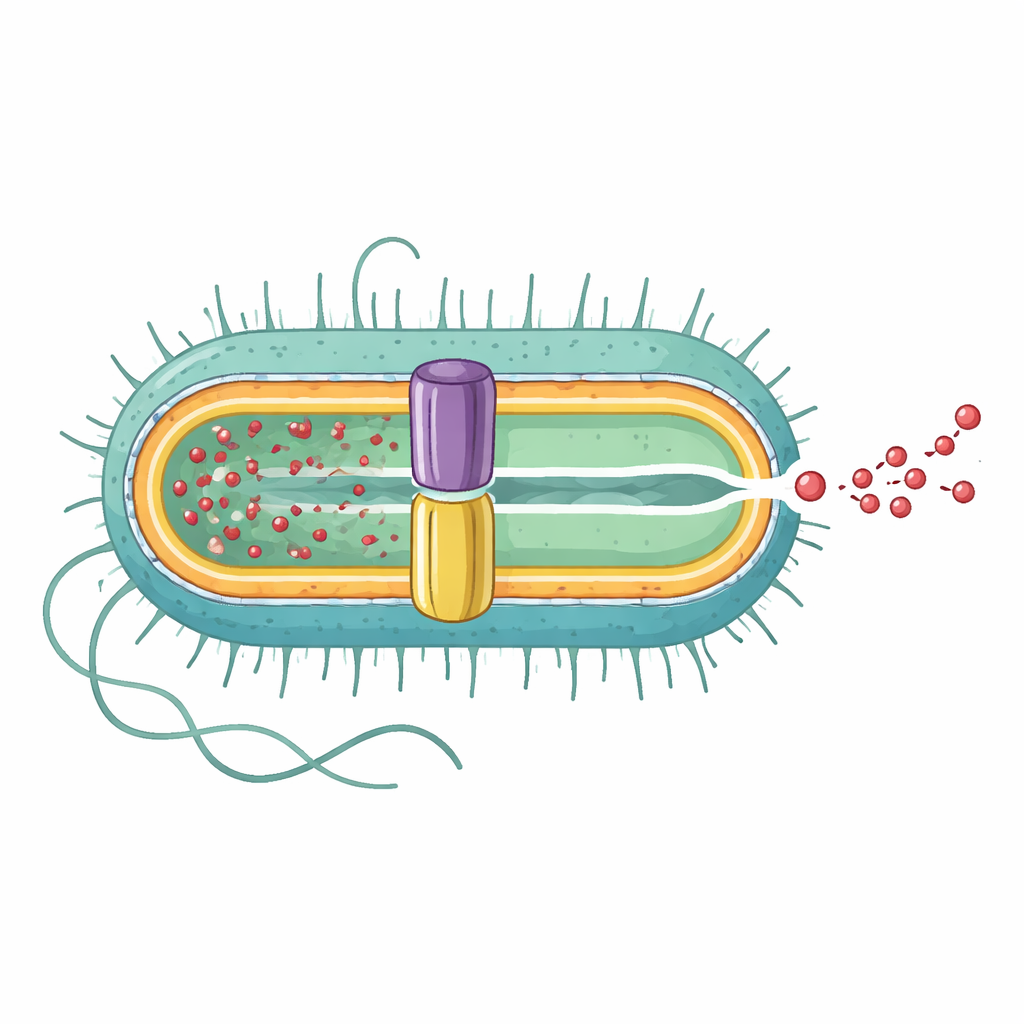
Avslöjar hela pumpen från insida till utsida
Forskarteamet använde högupplöst kryoelektronmikroskopi för att bestämma den tredimensionella strukturen av den kompletta EmrAB-TolC-pumpen. De fann att den är en förlängd sammansättning bestående av tre huvuddelar i förhållandet 3:6:1: tre kopior av det yttre membrankanalen TolC, sex kopior av den mellanliggande adapterproteinet EmrA, och en enda kopia av den inre membrantransportören EmrB. Tillsammans bildar de en kontinuerlig tunnel på ungefär 320 ångström som sträcker sig från det inre membranet, genom utrymmet mellan membranen, till utsidan. EmrA bildar en hexagonal hylsa mellan TolC och EmrB och formar en central nanokanal, medan TolC öppnar sig brett där den möter EmrA och skapar en direkt utgång mot cellens utsida.
Den inre motorn som driver läkemedelsexport
Längst ner i konstruktionen sitter EmrB, en medlem av en stor transportörfamilj som använder protonflöde — de laddade partiklar som bestämmer surhet — för att driva förflyttning av last. EmrB innehåller 14 membranövergående helixar ordnade i två domäner som gungar mot varandra. Strukturanalys och datorsimuleringar visar att en nyckelacidisk rest, D29, och dess närliggande aminosyror bildar ett protonkänsligt nätverk som kan växla EmrB mellan inåt- och utåt-öppna tillstånd. Mutationer i D29 och intilliggande positioner minskar kraftigt cellens resistens mot flera antibiotika, vilket betonar deras betydelse för att koppla protonrörelse till läkemedelstransport, även om protonflödet också kan involvera fler rester.
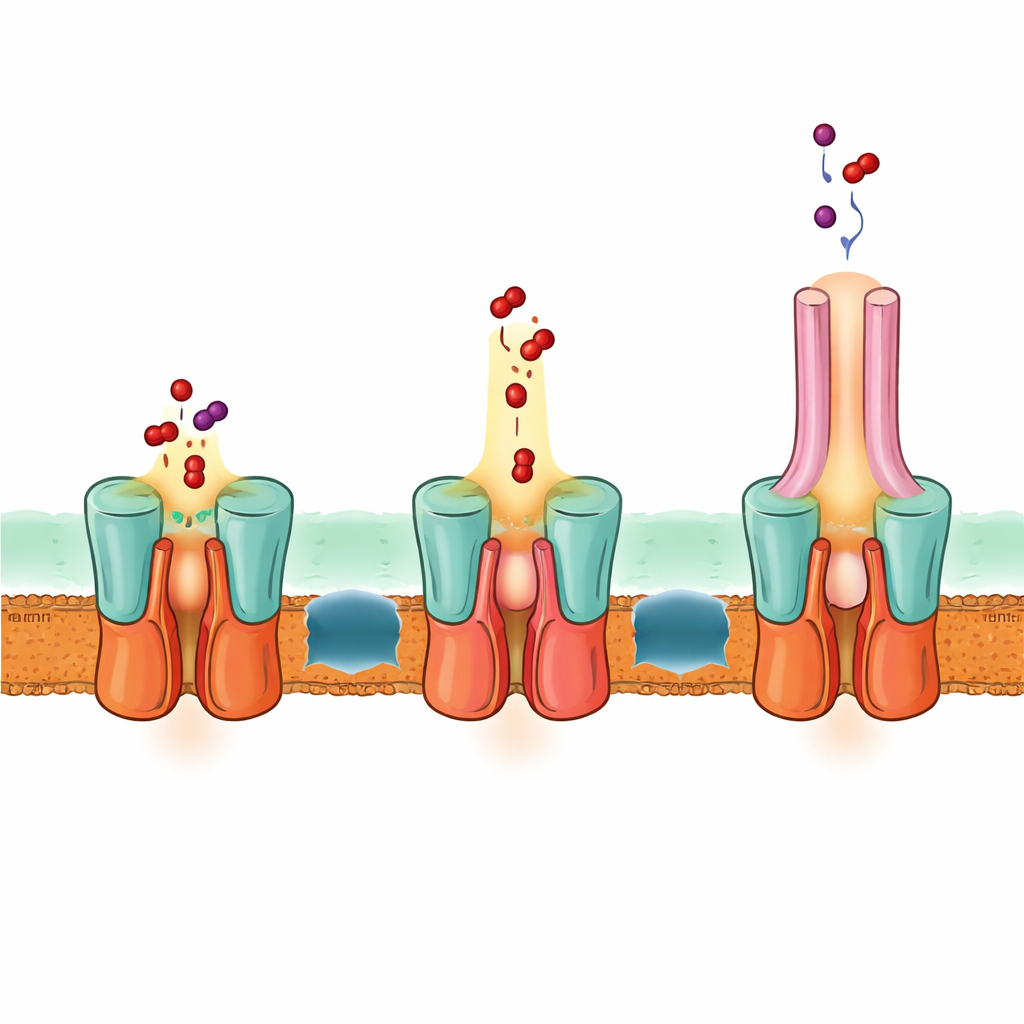
En enstegs flyktväg över båda membranen
Strukturen förklarar också hur EmrA och EmrB gränsar mot varandra för att bilda en tät ledning. Ett särskilt förlängt helixpaket på periplasmiska sidan av EmrB pluggar in i ett ringformat område i EmrA och låser transportören mot adaptern. Denna arrangemang skapar ett rymligt hålrum som kan ta emot läkemedel som släpps från EmrB och leda dem upp i EmrA-kanalen och vidare in i TolC. Baserat på strukturen, datorprediktioner och mutationsstudier föreslår författarna att EmrB fångar läkemedel från det inre membranet eller cytosolen, gungar för att öppna mot EmrA och frigör dem i detta gemensamma hålrum. En flexibel slinga i EmrA formar en trång passage som för läkemedlen uppåt genom adaptern och ut genom TolC, allt utan att läkemedlen någonsin fritt diffunderar i utrymmet mellan membranen.
Vad detta betyder för kampen mot resistens
Sammanfattningsvis stödjer arbetet en modell där EmrAB-TolC utför en verklig enstegs-export av antibiotika direkt från cellens insida till utsidan. Pumpen använder protonflöde för att driva upprepade formförändringar i EmrB, vilka i sin tur trycker läkemedel in i en kontinuerlig kanal bildad av EmrA och TolC. Genom att peka ut strukturella egenskaper som är avgörande för montering och funktion, såsom hydrofoba ringar i EmrA och nyckelrester i EmrB, framhäver studien potentiella svaga punkter där små molekyler skulle kunna fastna och blockera pumpen. Att rikta in sig på dessa punkter kan hjälpa till att återställa effekten hos befintliga antibiotika mot Gramnegativa patogener som i dag står emot behandling.
Citering: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Nyckelord: antibiotikaresistens, effluxpump, Gramnegativa bakterier, läkemedelstransport, EmrAB-TolC