Clear Sky Science · pt
Um modelo para o transporte de drogas através de duas membranas de bactérias Gram-negativas por um conjunto tripartite do tipo MFS
Por que pequenas bombas em bactérias importam
A resistência a antibióticos frequentemente se resume a uma corrida armamentista microscópica entre os fármacos e as defesas bacterianas. Uma defesa poderosa é um conjunto de pequenas bombas que expulsam os antibióticos da célula antes que possam causar dano. Este estudo revela a estrutura detalhada e o modelo de funcionamento de uma dessas bombas, chamada EmrAB-TolC, em Escherichia coli. Ao mostrar como essa máquina atravessa ambas as camadas protetoras da célula e expulsa drogas em um único passo, o trabalho oferece novas ideias para desarmar as defesas bacterianas e tornar medicamentos existentes mais eficazes.
O desafio de levar drogas a bactérias resistentes
Muitas bactérias perigosas estão envoltas não por uma, mas por duas membranas, com um espaço aquoso entre elas. Essa casca dupla dificulta a chegada dos antibióticos aos seus alvos. Bactérias Gram-negativas também constroem máquinas moleculares que reconhecem compostos nocivos dentro da célula e os ejetam para fora. EmrAB-TolC é uma dessas máquinas e pode lidar com vários antibióticos diferentes. Até agora, os cientistas dispunham apenas de instantâneos parciais de suas partes individuais. As grandes incógnitas eram como as peças se encaixam e como a bomba consegue mover as drogas através de ambas as membranas de forma coordenada.
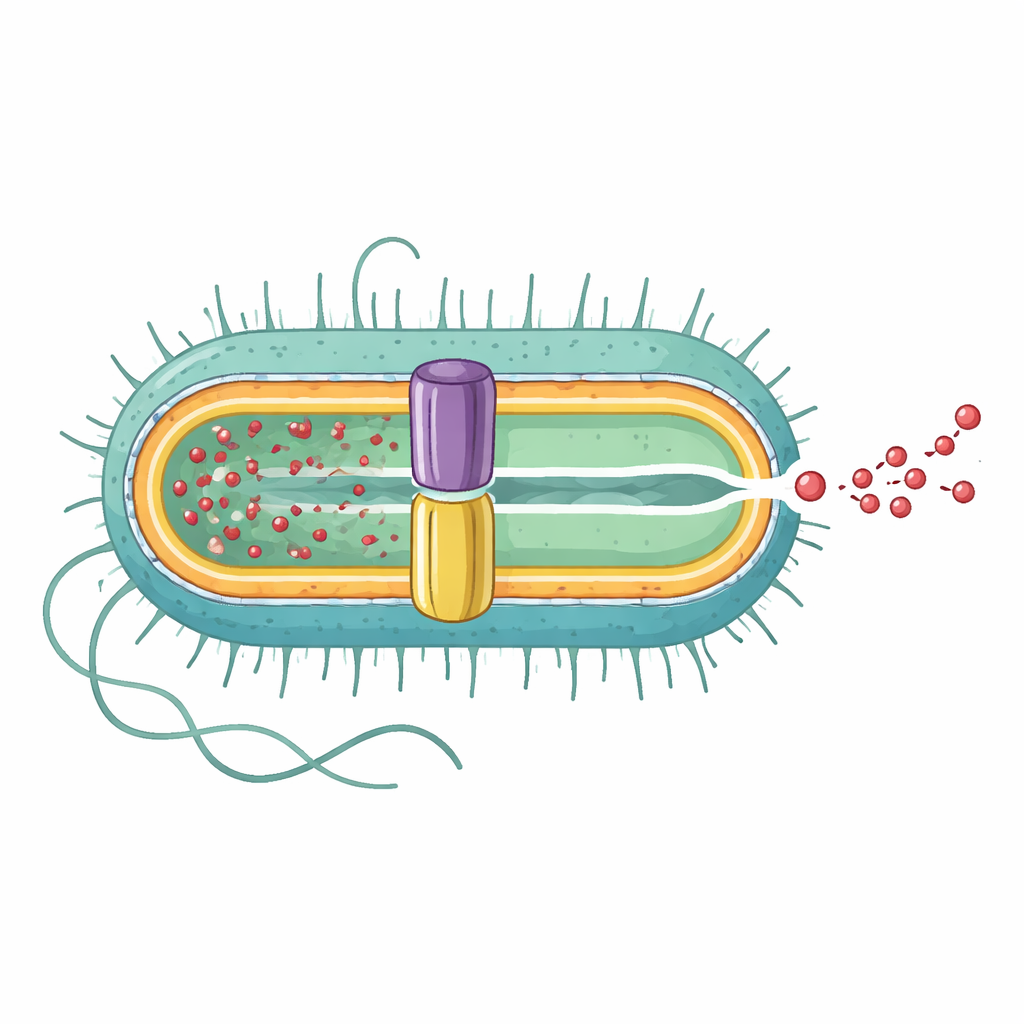
Revelando a bomba completa de dentro para fora
A equipe de pesquisa utilizou criomicroscopia eletrônica de alta resolução para determinar a estrutura tridimensional da EmrAB-TolC completa. Eles descobriram que se trata de um conjunto alongado composto por três partes principais em razão 3:6:1: três cópias do canal da membrana externa TolC, seis cópias da proteína adaptadora intermediária EmrA e uma única cópia do transportador da membrana interna EmrB. Juntas formam um túnel contínuo com cerca de 320 angström de comprimento que vai da membrana interna, através do espaço periplasmático, até o exterior. EmrA forma uma manga hexagonal entre TolC e EmrB, moldando um nano-canal central, enquanto TolC se abre amplamente onde encontra EmrA, criando uma rota de saída direta para o exterior celular.
O motor interno que alimenta a exportação de drogas
Na base do complexo está EmrB, um membro de uma grande família de transportadores que usa o fluxo de prótons — partículas carregadas que definem a acidez — para impulsionar o movimento de carga. EmrB contém 14 hélices transmembrana organizadas em dois domínios que balançam entre si. Análises estruturais e simulações computacionais mostram que um resíduo ácido chave, D29, e seus vizinhos formam uma rede sensível a prótons que pode alternar EmrB entre estados abertos para dentro e abertos para fora. Mutações em D29 e posições próximas reduzem muito a resistência da célula a vários antibióticos, ressaltando sua importância no acoplamento do movimento de prótons ao transporte de drogas, embora o fluxo de prótons também possa envolver resíduos adicionais.
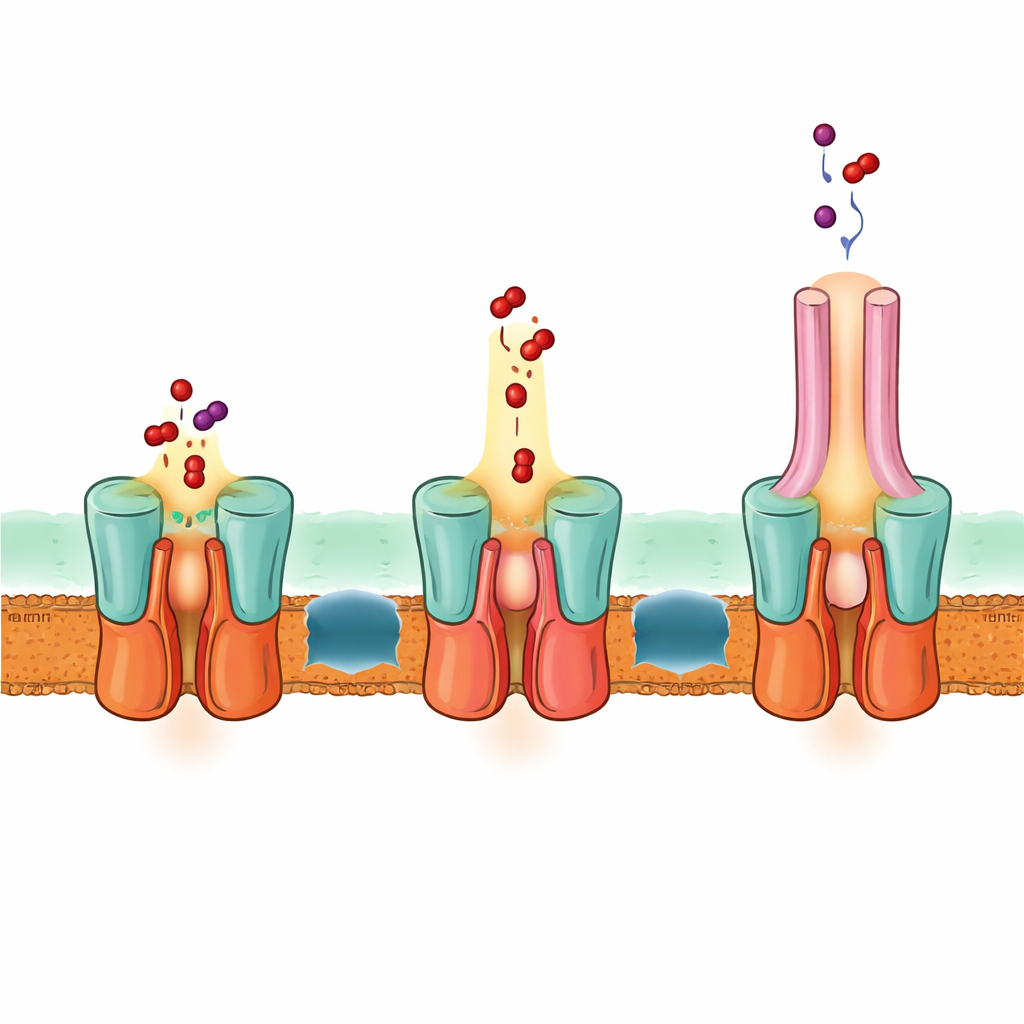
Uma rota de fuga em um passo através de ambas as membranas
A estrutura também explica como EmrA e EmrB fazem interface para formar um duto vedado. Um feixe helicoidal estendido no lado periplasmático de EmrB encaixa-se em uma região em forma de anel de EmrA, travando o transportador ao adaptador. Esse arranjo cria uma cavidade espaçosa que pode receber drogas liberadas por EmrB e guiá-las para cima, para o canal de EmrA e então para TolC. Com base na estrutura, em previsões computacionais e em testes de mutação, os autores propõem que EmrB captura drogas da membrana interna ou do citoplasma, então oscila para abrir-se em direção a EmrA e liberá-las nessa cavidade compartilhada. Uma alça flexível dentro de EmrA molda um caminho estreito que direciona as drogas para cima através do adaptador e para fora por TolC, tudo isso sem que as drogas difussem livremente no espaço entre as membranas.
O que isso significa para combater a resistência
No conjunto, o trabalho apoia um modelo no qual EmrAB-TolC realiza uma exportação verdadeira em um único passo de antibióticos diretamente do interior da célula para o exterior. A bomba usa o fluxo de prótons para impulsionar repetidas mudanças conformacionais em EmrB, que por sua vez empurram as drogas para um canal contínuo formado por EmrA e TolC. Ao identificar características estruturais essenciais para o conjunto e sua função, como anéis hidrofóbicos em EmrA e resíduos-chave em EmrB, o estudo destaca pontos fracos potenciais onde pequenas moléculas poderiam travar a bomba. Alvejar esses pontos poderia ajudar a restaurar a potência de antibióticos existentes contra patógenos Gram-negativos que hoje resistem ao tratamento.
Citação: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Palavras-chave: resistência a antibióticos, bomba de efluxo, bactérias Gram-negativas, transporte de drogas, EmrAB-TolC