Clear Sky Science · ru
Модель транспорта лекарств через две мембраны грам-отрицательных бактерий с помощью трипартитного комплекса MFS
Почему маленькие насосы в бактериях важны
Антибиотикорезистентность во многом — это микроскопическая гонка вооружений между лекарствами и защитными механизмами бактерий. Одной из мощных защит являются крошечные насосы, которые выталкивают антибиотики из клетки прежде, чем те успеют навредить. В этом исследовании раскрыта детальная структура и рабочая модель одного такого насоса, называемого EmrAB-TolC, в Escherichia coli. Показав, как этот механизм охватывает оба защитных слоя клетки и выталкивает препараты в один шаг, работа предлагает новые идеи по нейтрализации бактериальной защиты и повышению эффективности существующих лекарств.
Проблема доставки препаратов в «тяжелую» бактерию
Многие опасные бактерии окружены не одной, а двумя мембранами, с водной периплазматической пространством между ними. Эта двойная оболочка затрудняет достижение антибиотиками своих мишеней. Грам-отрицательные бактерии также собирают молекулярные машины, которые распознают вредные соединения внутри клетки и выталкивают их наружу. EmrAB-TolC — одна из таких машин, способная работать с несколькими разными антибиотиками. До недавнего времени учёные имели лишь фрагментарные представления об отдельных частях. Главными неизвестными оставались то, как эти части соединяются, и как насос координированно перемещает лекарства через обе мембраны.
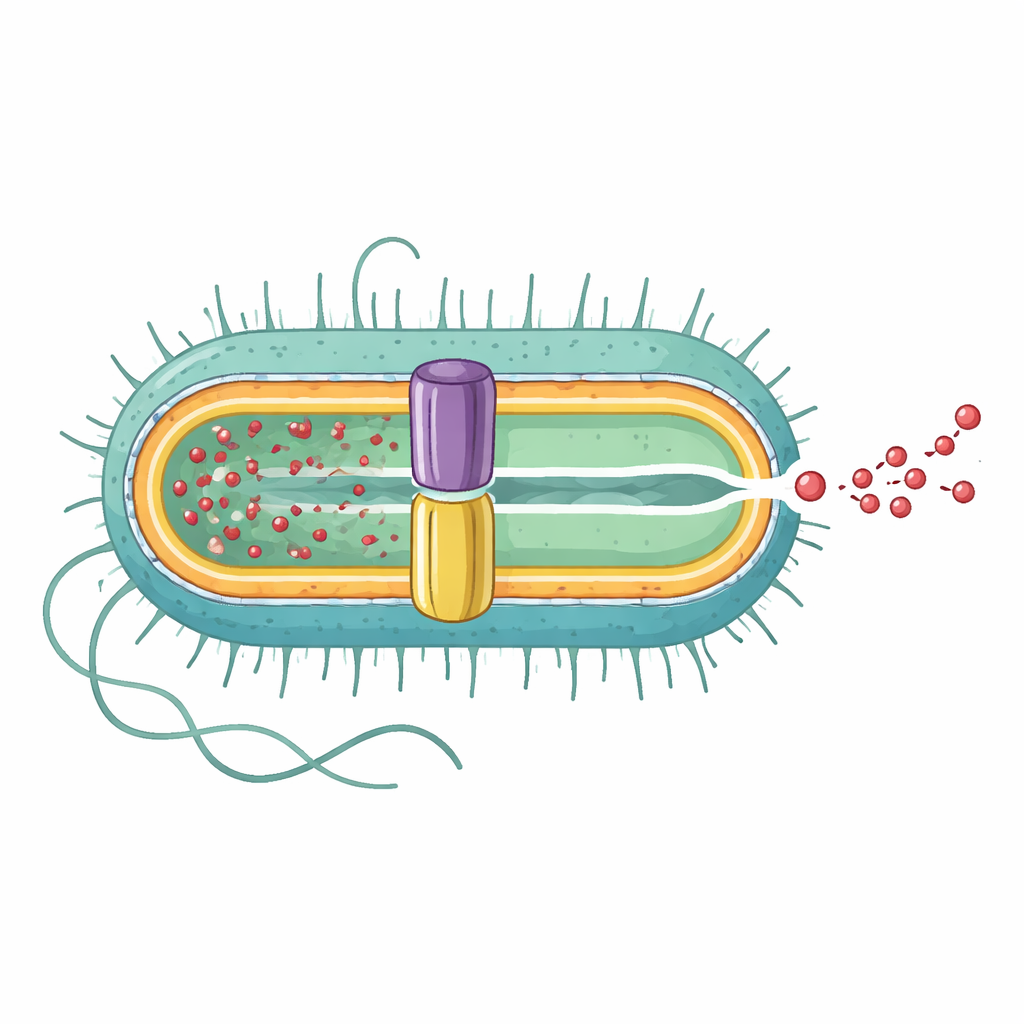
Раскрытие полного насоса от внутренней стороны к внешней
Команда использовала крио-электронную микроскопию высокого разрешения, чтобы определить трёхмерную структуру полного комплекса EmrAB-TolC. Они обнаружили, что это вытянутая сборка, состоящая из трёх основных частей в соотношении 3:6:1: три копии наружного канала TolC, шесть копий среднего адаптерного белка EmrA и одна копия внутреннего транспортёра EmrB. Вместе они образуют непрерывный туннель длиной примерно 320 ангстрем, который тянется от внутренней мембраны, через межмембранное пространство, к внешней среде. EmrA формирует шестиугольный «чехол» между TolC и EmrB, задавая форму центральному наноканалу, тогда как TolC широко раскрыт на стыке с EmrA, обеспечивая прямой выход наружу.
Внутренний двигатель, питающий экспорт препаратов
В основании комплекса находится EmrB — представитель большой семьи транспортёров, использующих поток протонов (заряженных частиц, определяющих кислотность) для приведения в движение грузов. EmrB содержит 14 мембранных спиралей, организованных в два домена, которые качаются относительно друг друга. Структурный анализ и компьютерное моделирование показывают, что ключевой кислый остаток D29 и его окружение формируют протончувствительную сеть, способную переключать EmrB между внутренне- и внешне- открытыми состояниями. Мутации в D29 и соседних позициях значительно снижают устойчивость клетки к нескольким антибиотикам, что подчёркивает их роль в связывании движения протонов с транспортом лекарств, хотя поток протонов может также вовлекать дополнительные остатки.
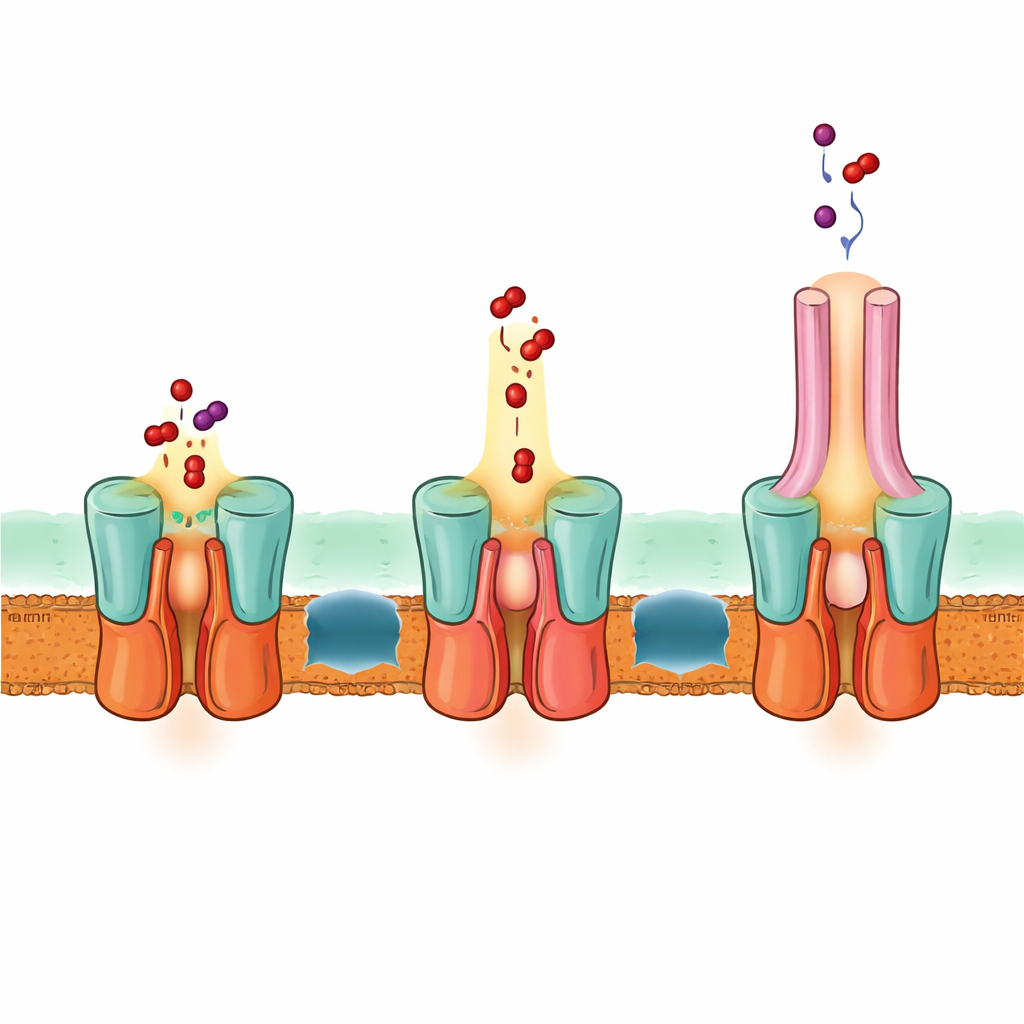
Одношаговый путь через обе мембраны
Структура также объясняет, как EmrA и EmrB взаимодействуют, образуя герметичный проводник. Особый удлинённый пучок спиралей на периплазматической стороне EmrB входит в кольцевую область EmrA, блокируя связь транспортёра с адаптером. Такая организация создаёт объёмную полость, способную принимать лекарства, высвобождаемые из EmrB, и направлять их вверх в канал EmrA, а затем в TolC. На основании структуры, компьютерных предсказаний и результатов мутаций авторы предлагают, что EmrB захватывает препараты из внутренней мембраны или цитоплазмы, затем качается, открываясь в сторону EmrA и высвобождая их в общую полость. Гибкая петля в EmrA формирует узкий канал, который воронкообразно направляет препараты вверх через адаптер и наружу через TolC, при этом препараты никогда не диффундируют свободно в периплазматическом пространстве.
Что это значит для борьбы с резистентностью
В совокупности работа поддерживает модель, в которой EmrAB-TolC выполняет истинный одношаговый экспорт антибиотиков напрямую изнутри клетки наружу. Насос использует поток протонов, чтобы приводить EmrB в повторяющиеся конформационные изменения, которые, в свою очередь, проталкивают препараты в непрерывный канал, образованный EmrA и TolC. Точная идентификация структурных элементов, важных для сборки и функции — таких как гидрофобные кольца в EmrA и ключевые остатки в EmrB — выделяет потенциальные уязвимые места, где мелкие молекулы могли бы заклинить насос. Нацеливание на эти участки может помочь восстановить эффективность существующих антибиотиков против грам-отрицательных патогенов, которые в настоящее время выдерживают лечение.
Цитирование: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Ключевые слова: антибиотикорезистентность, выкачивающий насос, грам-отрицательные бактерии, транспорт лекарств, EmrAB-TolC