Clear Sky Science · tr
Gram-negatif bakterilerin iki zarı boyunca ilaç taşınması için MFS üç parçalı bir montaj modeli
Neden bakterilerdeki küçük pompalar önemli
Antibiyotik direnci çoğunlukla ilaçlarla bakterilerin savunmaları arasındaki mikroskobik bir silahlanma yarışına dayanır. Güçlü savunmalardan biri, antibiyotikleri zarara yol açmadan önce hücre dışına atan küçük pompalardan oluşan bir settir. Bu çalışma, Escherichia coli'de EmrAB-TolC adındaki bu pompalardan birinin ayrıntılı yapısını ve çalışma modelini ortaya koyuyor. Bu makinenin hücrenin iki koruyucu katmanını nasıl kapladığını ve ilaçları tek bir adımda nasıl dışarı attığını göstererek, bakteriyel savunmaları etkisiz hale getirme ve mevcut ilaçları daha etkili kılma konusunda yeni fikirler sunuyor.
Zorlu bakterilere ilaç ulaştırmanın zorluğu
Birçok tehlikeli bakteri yalnızca tek değil iki zarla çevrilidir ve zarlar arasında bir periplazmik boşluk bulunur. Bu çift kabuk, antibiyotiklerin hedeflerine ulaşmasını zorlaştırır. Gram-negatif bakteriler ayrıca hücre içindeki zararlı bileşikleri tanıyıp dışarı atan moleküler makineler oluşturur. EmrAB-TolC bu makinelerden biridir ve birkaç farklı antibiyotiği taşıyabilir. Bugüne dek bilim insanlarının sadece bileşenlerinin kısmi görüntüleri vardı. Büyük bilinmeyenler, parçaların nasıl bir araya geldiği ve pompanın ilaçları her iki zarı koordineli bir şekilde nasıl taşıdığıydı.
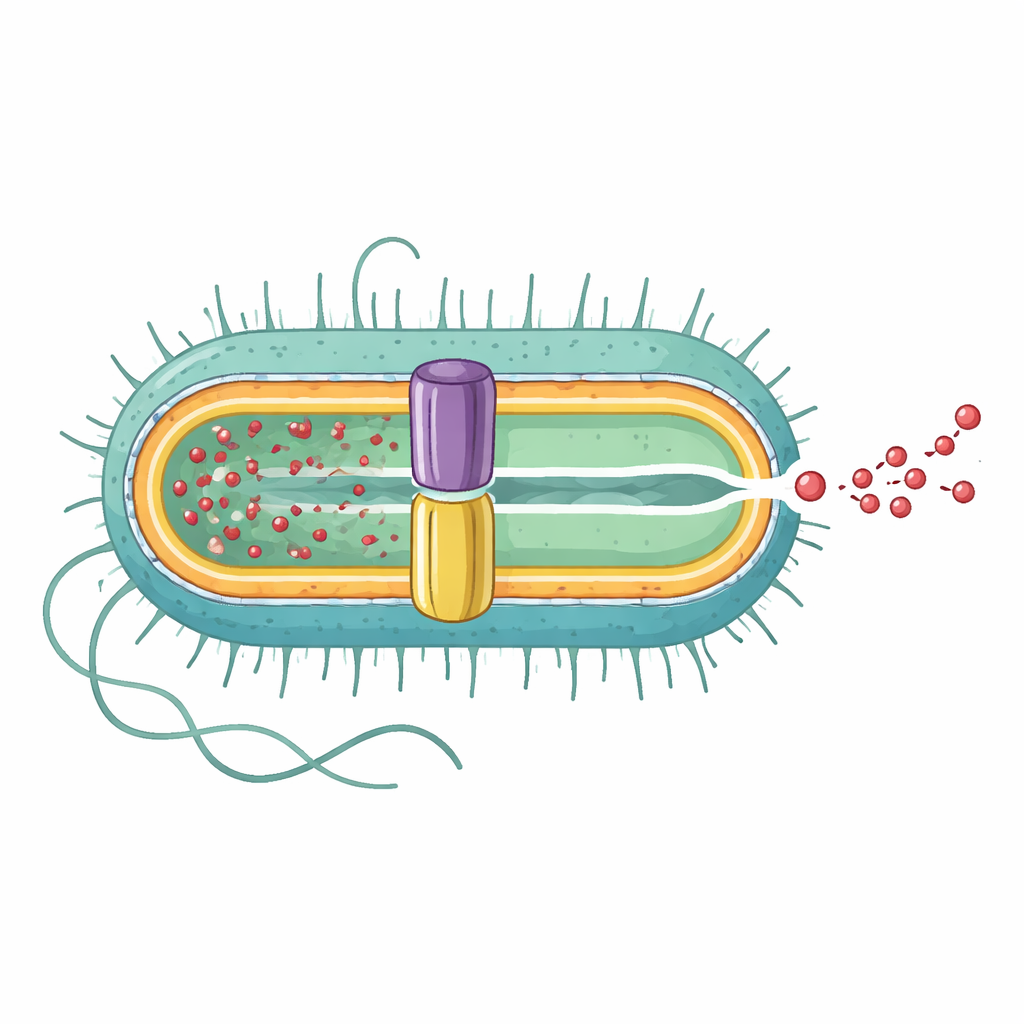
Pompayı içten dışa bütün hâliyle ortaya çıkarmak
Araştırma ekibi, tam EmrAB-TolC pompasının üç boyutlu yapısını yüksek çözünürlüklü kriyo-elektron mikroskobu ile belirledi. Yapının, 3:6:1 oranında üç ana parçadan oluşan uzamış bir montaj olduğunu buldular: dış zar kanalı TolC'den üç kopya, orta adaptör proteini EmrA'dan altı kopya ve iç zar taşıyıcısı EmrB'den tek bir kopya. Birlikte, iç zaradan başlayıp zarlar arasındaki boşluktan geçerek dışarıya ulaşan yaklaşık 320 angström uzunluğunda sürekli bir tünel oluşturuyorlar. EmrA, TolC ile EmrB arasında altıgen bir kılıf oluşturarak merkezi bir nano-kanal şekillendirirken, TolC EmrA ile buluştuğu noktada geniş açılarak hücre dışına doğrudan bir çıkış yolu yaratıyor.
İlaç ihracatını çalıştıran iç motor
Montajın tabanında, yükün hareketini proton akışını kullanarak sağlayan büyük bir taşıyıcı ailesinin üyesi EmrB bulunur. EmrB, birbirine karşı sallanan iki alana düzenlenmiş 14 zar geçirgen heliks içerir. Yapısal analiz ve bilgisayar simülasyonları, anahtar bir asidik kalıntı olan D29 ve komşularının, EmrB'yi içe ve dışa açık durumlar arasında değiştirebilen proton-duyarlı bir ağ oluşturduğunu gösteriyor. D29 ve yakınındaki pozisyonlardaki mutasyonlar, proton akışının ek kalıntıları da içerebilmesine rağmen proton hareketini ilaç taşınımına bağlamadaki önemlerini vurgulayarak hücrenin birkaç antibiyotiğe karşı direncini büyük ölçüde azaltıyor.
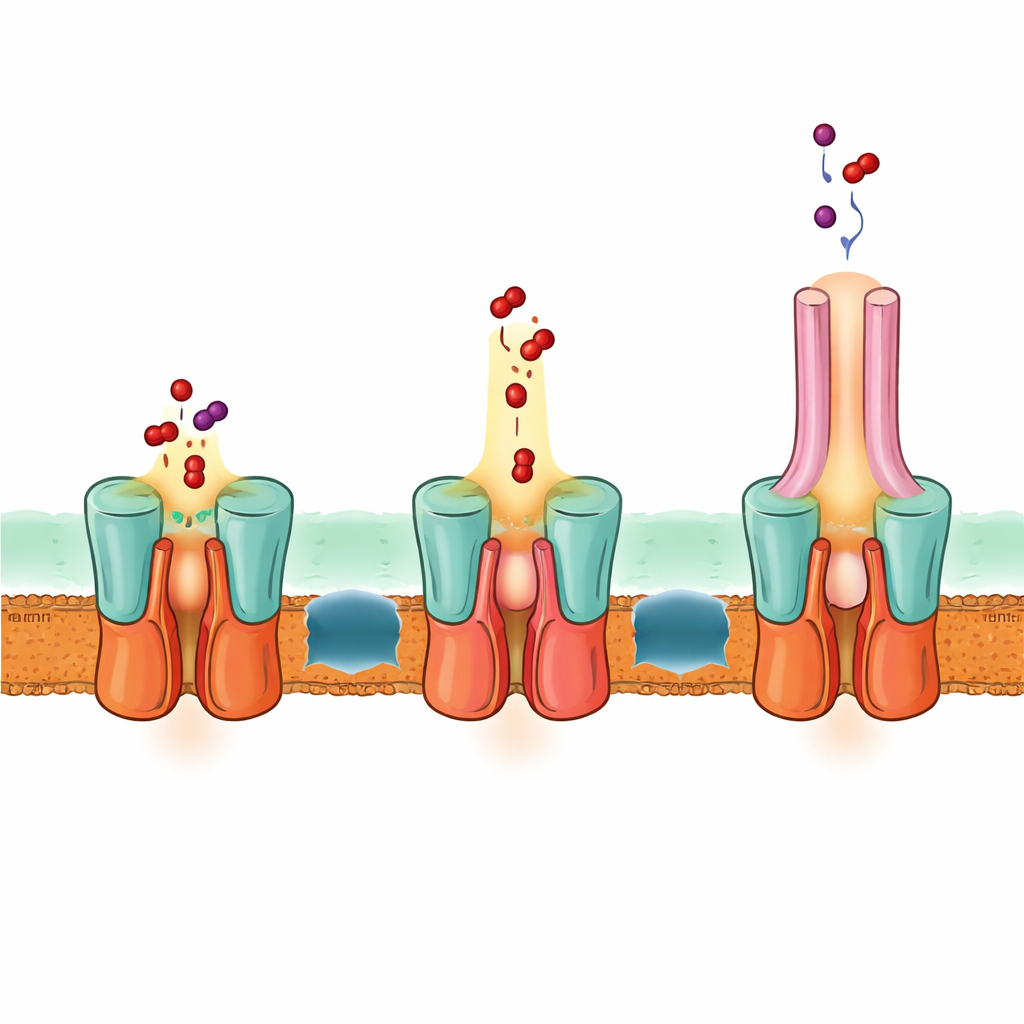
Her iki zarı aşan tek adımlık kaçış yolu
Yapı ayrıca EmrA ile EmrB'nin nasıl bir arayüz oluşturup sızdırmaz bir kanal oluşturduğunu açıklar. EmrB'nin periplazmik tarafındaki özel uzamış heliks demeti, EmrA'nın halka biçimli bir bölgesine oturarak taşıyıcıyı adaptöre kilitler. Bu düzenleme, EmrB'den salınan ilaçları alabilecek ve bunları EmrA kanalına ve sonra TolC'ye yönlendirebilecek geniş bir boşluk oluşturur. Yapıya, bilgisayar tahminlerine ve mutasyonel testlere dayanarak yazarlar, EmrB'nin ilaçları iç zar veya sitoplazmadan yakalayıp sonra EmrA'ya doğru açılacak şekilde sallanarak bunları ortak boşluğa saldığını öne sürüyorlar. EmrA içindeki esnek bir halka, ilaçları adaptör boyunca yukarı doğru daraltan bir yol şekillendirir ve böylece ilaçlar zarlar arasındaki boşlukta serbestçe difüze olmadan EmrA ve TolC tarafından oluşturulmuş sürekli kanaldan dışarı atılır.
Dirençle mücadele açısından ne anlama geliyor
Toplamda bu çalışma, EmrAB-TolC'nin antibiyotikleri hücre içinden doğrudan dışarıya gerçek bir tek aşamalı ihracat şeklinde gerçekleştirdiği modelini destekliyor. Pompa, EmrB'de tekrarlayan şekil değişikliklerini tetiklemek için proton akışını kullanır; bu değişiklikler ilaçları EmrA ve TolC tarafından oluşturulan sürekli bir kanala iter. Montaj ve işlev için hayati önemde olan hidrofobik halkalar gibi EmrA'daki ve EmrB'deki anahtar kalıntılar gibi yapısal özellikleri kesinleştirerek çalışma, küçük moleküllerin pompayı tıkayabileceği potansiyel zayıf noktaları vurguluyor. Bu noktaların hedeflenmesi, şu anda tedaviye direnç gösteren Gram-negatif patojenlere karşı mevcut antibiyotiklerin etkinliğini geri kazanmaya yardımcı olabilir.
Atıf: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Anahtar kelimeler: antibiyotik direnci, dışa atım pompası, Gram-negatif bakteriler, ilaç taşınımı, EmrAB-TolC