Clear Sky Science · fr
Un modèle de transport de médicaments à travers deux membranes des bactéries Gram-négatives par un assemblage tripartite de la superfamille MFS
Pourquoi de minuscules pompes bactériennes comptent
La résistance aux antibiotiques se joue souvent à l’échelle microscopique, dans une course aux armements entre les médicaments et les défenses bactériennes. L’un des moyens de défense les plus puissants est un ensemble de minuscules pompes qui expulsent les antibiotiques hors de la cellule avant qu’ils ne puissent nuire. Cette étude révèle la structure détaillée et le modèle de fonctionnement d’une de ces pompes, appelée EmrAB-TolC, chez Escherichia coli. En montrant comment cette machine s’étend à travers les deux couches protectrices de la cellule et expulse les médicaments en une seule étape, le travail apporte de nouvelles pistes pour neutraliser les défenses bactériennes et rendre les traitements existants plus efficaces.
Le défi d’atteindre les bactéries les plus résistantes
De nombreuses bactéries dangereuses sont enveloppées non pas d’une mais de deux membranes, avec un espace aqueux intermembranaire. Cette double enveloppe complique l’accès des antibiotiques à leurs cibles. Les bactéries Gram-négatives construisent aussi des machines moléculaires qui reconnaissent les composés nocifs à l’intérieur de la cellule et les expulsent vers l’extérieur. EmrAB-TolC est l’une de ces machines, capable de traiter plusieurs antibiotiques différents. Jusqu’ici, les scientifiques ne disposaient que de clichés partiels de ses composants individuels. Les grandes inconnues étaient la manière dont les pièces s’emboîtent et comment la pompe parvient à déplacer les médicaments à travers les deux membranes de façon coordonnée.
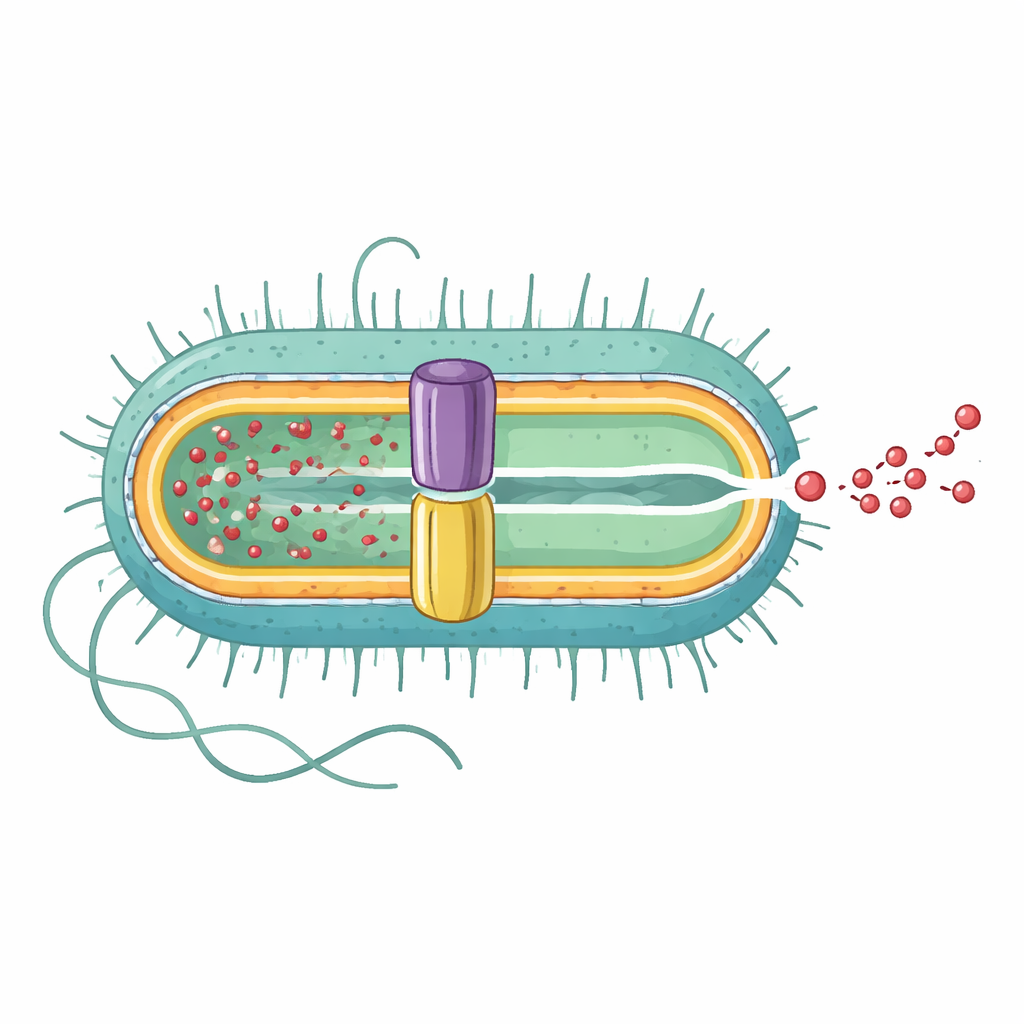
Révéler la pompe complète de l’intérieur vers l’extérieur
L’équipe a utilisé la cryo‑microscopie électronique à haute résolution pour déterminer la structure tridimensionnelle de la pompe EmrAB-TolC complète. Ils ont trouvé qu’il s’agit d’un assemblage allongé composé de trois parties principales selon un ratio 3:6:1 : trois copies du canal de la membrane externe TolC, six copies de la protéine adaptatrice intermédiaire EmrA, et une seule copie du transporteur de la membrane interne EmrB. Ensemble, elles forment un tunnel continu d’environ 320 angströms de long, allant de la membrane interne, à travers l’espace périplasmique, jusqu’à l’extérieur. EmrA forme une manche hexagonale entre TolC et EmrB, façonnant un nano‑canal central, tandis que TolC s’ouvre largement au point de rencontre avec EmrA, créant une sortie directe vers l’extérieur cellulaire.
Le moteur interne qui alimente l’exportation des médicaments
À la base de l’assemblage se trouve EmrB, membre d’une grande famille de transporteurs qui utilise le flux de protons, les particules chargées qui définissent l’acidité, pour alimenter le déplacement de cargaisons. EmrB contient 14 hélices transmembranaires organisées en deux domaines qui basculent l’un par rapport à l’autre. L’analyse structurale et les simulations informatiques montrent qu’un résidu acide clé, D29, et ses voisins forment un réseau sensible aux protons capable de basculer EmrB entre des états ouverts vers l’intérieur et vers l’extérieur. Des mutations de D29 et des positions voisines réduisent fortement la résistance cellulaire à plusieurs antibiotiques, soulignant leur rôle dans l’association du mouvement des protons au transport des médicaments, même si le flux de protons peut également impliquer d’autres résidus.
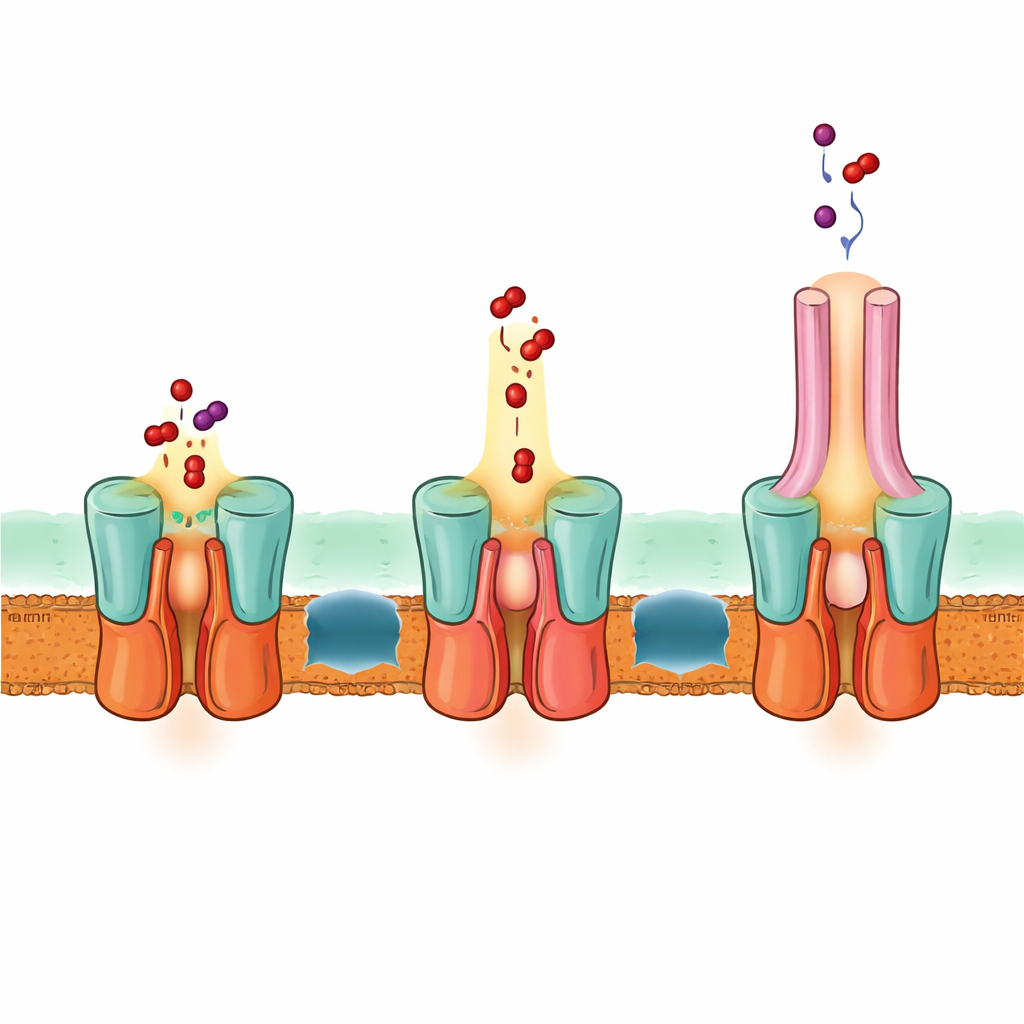
Une voie d’évasion en une seule étape à travers les deux membranes
La structure explique aussi comment EmrA et EmrB s’interface pour former un conduit étanche. Un faisceau hélicoïdal étendu du côté périplasmique d’EmrB s’emboîte dans une région en anneau d’EmrA, verrouillant le transporteur à l’adaptateur. Cet agencement crée une cavité spacieuse capable de recevoir les médicaments libérés par EmrB et de les guider vers le canal d’EmrA puis vers TolC. Sur la base de la structure, de prédictions informatiques et d’essais de mutations, les auteurs proposent qu’EmrB capte les médicaments depuis la membrane interne ou le cytoplasme, puis bascule pour s’ouvrir vers EmrA et les libérer dans cette cavité partagée. Une boucle flexible au sein d’EmrA façonne un passage étroit qui canalise les médicaments vers le haut à travers l’adaptateur et hors de TolC, le tout sans que les médicaments ne diffusent librement dans l’espace intermembranaire.
Ce que cela signifie pour lutter contre la résistance
Dans l’ensemble, le travail soutient un modèle selon lequel EmrAB-TolC réalise une véritable exportation en une seule étape des antibiotiques, directement de l’intérieur de la cellule vers l’extérieur. La pompe utilise le flux de protons pour entraîner des changements de conformation répétés d’EmrB, qui poussent à leur tour les médicaments dans un canal continu formé par EmrA et TolC. En identifiant des caractéristiques structurelles essentielles à l’assemblage et à la fonction, comme des anneaux hydrophobes dans EmrA et des résidus clés dans EmrB, l’étude met en lumière des points faibles potentiels où de petites molécules pourraient bloquer la pompe. Cibler ces points pourrait aider à restaurer l’efficacité des antibiotiques existants contre des pathogènes Gram-négatifs aujourd’hui résistants aux traitements.
Citation: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Mots-clés: résistance aux antibiotiques, pompe d’efflux, bactéries Gram-négatives, transport de médicaments, EmrAB-TolC