Clear Sky Science · nl
Een model voor medicijntransport door twee membranen van Gram-negatieve bacteriën via een MFS-tripartiete assemblage
Waarom piepkleine pompen in bacteriën ertoe doen
Antibioticaresistentie komt vaak neer op een microscopisch wapenwedloop tussen geneesmiddelen en de verdediging van bacteriën. Een krachtige verdediging is een reeks kleine pompen die antibiotica uit de cel gooien voordat ze schade kunnen aanrichten. Deze studie onthult de gedetailleerde structuur en het werkingsmodel van één van die pompen, EmrAB-TolC, in Escherichia coli. Door te tonen hoe dit mechanisme beide beschermlagen van de cel overspant en geneesmiddelen in één stap naar buiten drijft, biedt het werk nieuwe aanknopingspunten om bacteriële afweer uit te schakelen en bestaande geneesmiddelen effectiever te maken.
De uitdaging om medicijnen in harde bacteriën te krijgen
Veel gevaarlijke bacteriën zijn omgeven door niet één maar twee membranen, met een waterige ruimte ertussen. Deze dubbele schaal bemoeilijkt het bereiken van de doelen door antibiotica. Gram-negatieve bacteriën bouwen ook moleculaire machines die schadelijke verbindingen in de cel herkennen en naar buiten pompen. EmrAB-TolC is zo’n machine en kan meerdere verschillende antibiotica aan. Tot nu toe hadden wetenschappers slechts deelbeelden van de afzonderlijke onderdelen. De grote onbekenden waren hoe de delen samenkomen en hoe de pomp geneesmiddelen gecoördineerd volledig door beide membranen verplaatst.
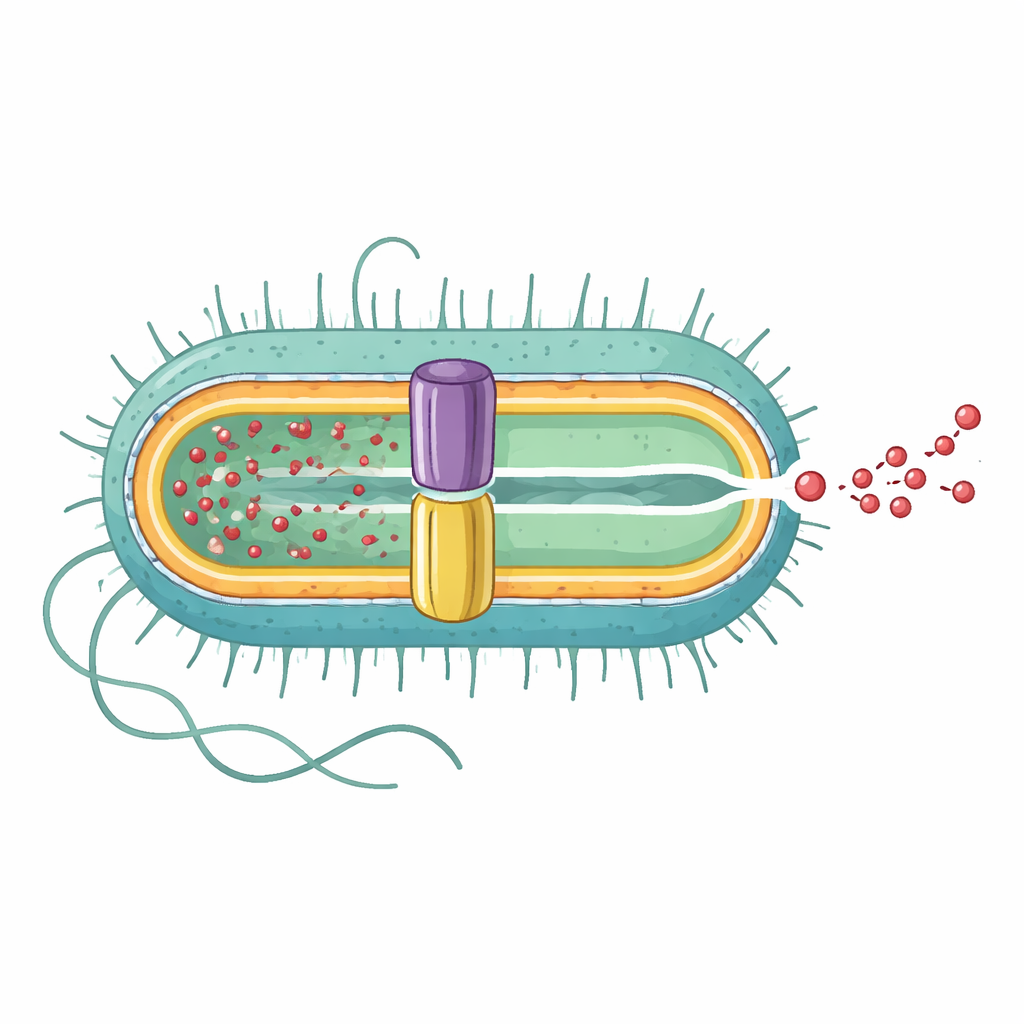
De volledige pomp van binnen naar buiten onthuld
Het onderzoeksteam gebruikte cryo-elektronenmicroscopie met hoge resolutie om de driedimensionale structuur van de complete EmrAB-TolC-pomp vast te leggen. Ze vonden dat het een langgerekte assemblage is die uit drie hoofdonderdelen bestaat in een 3:6:1-verhouding: drie kopieën van het buitenmembraankanaal TolC, zes kopieën van het intermediaire adaptor-eiwit EmrA en één kopie van de binnenmembraantransporter EmrB. Samen vormen ze een doorlopend tunnelachtig kanaal van ongeveer 320 ångström lang dat reikt van het binnenmembraan, door de ruimte tussen de membranen, naar buiten. EmrA vormt een hexagonaal mouwwerk tussen TolC en EmrB en vormt een centraal nano-kanaal, terwijl TolC breed opent waar het EmrA ontmoet, waardoor een directe uitgang naar de buitenkant van de cel ontstaat.
De interne motor die het exporteren van geneesmiddelen aandrijft
Aan de basis van de assemblage bevindt zich EmrB, lid van een grote transporterfamilie die gebruikmaakt van de stroom van protonen, de geladen deeltjes die zuurgraad bepalen, om het verplaatsen van ladingen aan te drijven. EmrB bevat 14 membraanoverspannende helices gerangschikt in twee domeinen die tegen elkaar kantelen. Structurele analyse en computersimulaties tonen aan dat een belangrijk zuur residu, D29, en zijn buren een protongevoelig netwerk vormen dat EmrB tussen naar-binnen- en naar-buiten-open toestanden kan schakelen. Mutaties in D29 en nabijgelegen posities verminderen de resistentie van de cel tegen verschillende antibiotica sterk, wat hun belang benadrukt bij het koppelen van protonbeweging aan medicijntransport, hoewel protonstroom ook aanvullende residuen kan betrekken.
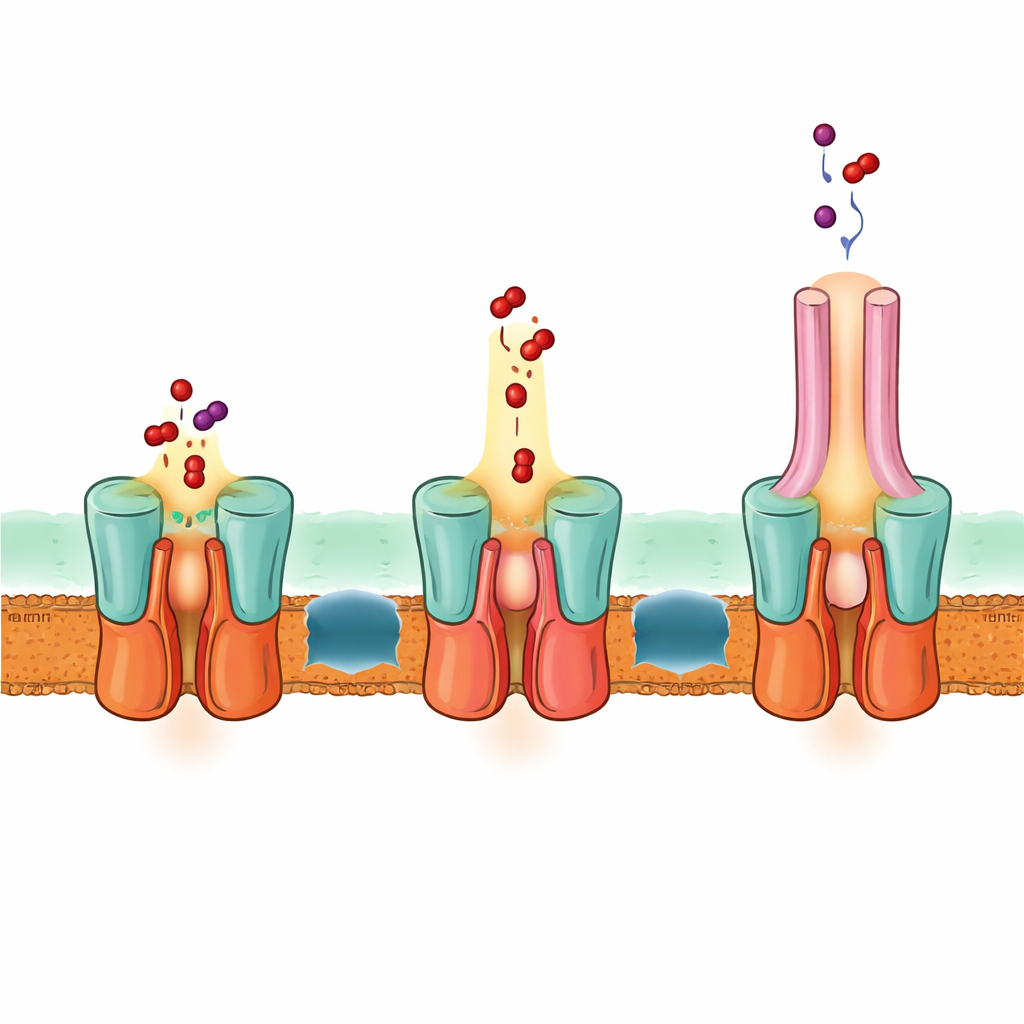
Een eentraps vluchtweg door beide membranen
De structuur verklaart ook hoe EmrA en EmrB interfacing tot een afgesloten geleider vormt. Een speciaal uitgebreid helixbundel aan de periplasmatische zijde van EmrB steekt in een ringvormig gebied van EmrA en vergrendelt de transporter aan de adaptor. Deze ordening creëert een ruime holte die geneesmiddelen kan ontvangen die door EmrB worden vrijgegeven en ze kan geleiden naar het EmrA-kanaal en vervolgens naar TolC. Op basis van de structuur, computervoorspellingen en mutatietests stellen de auteurs voor dat EmrB geneesmiddelen uit het binnenmembraan of cytoplasma grijpt, vervolgens kantelt om naar EmrA open te gaan en ze in deze gedeelde holte vrij te geven. Een flexibele lus binnen EmrA vormt een smalle baan die geneesmiddelen naar boven leidt door de adaptor en naar buiten via TolC, zonder dat de geneesmiddelen ooit vrij in de ruimte tussen de membranen diffunderen.
Wat dit betekent voor het bestrijden van resistentie
Al met al ondersteunt het werk een model waarin EmrAB-TolC een echte eentrapsexport uitvoert van antibiotica direct van binnen de cel naar de buitenwereld. De pomp gebruikt protonstroom om herhaalde vormveranderingen in EmrB aan te drijven, die op hun beurt geneesmiddelen in een continu kanaal van EmrA en TolC duwen. Door structurele kenmerken te identificeren die essentieel zijn voor assemblage en functie, zoals hydrofobe ringen in EmrA en sleutelresiduen in EmrB, belicht de studie potentiële zwakke plekken waar kleine moleculen de pomp kunnen blokkeren. Het richten op deze plekken zou kunnen helpen de werkzaamheid van bestaande antibiotica te herstellen tegen Gram-negatieve ziekteverwekkers die huidige behandelingen weerstaan.
Bronvermelding: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Trefwoorden: antibioticaresistentie, effluxpomp, Gram-negatieve bacteriën, medicijntransport, EmrAB-TolC