Clear Sky Science · es
Un modelo para el transporte de fármacos a través de dos membranas de bacterias Gramnegativas mediante un ensamblaje tripartito MFS
Por qué importan las bombas diminutas en las bacterias
La resistencia a los antibióticos a menudo se reduce a una carrera armamentística microscópica entre los fármacos y las defensas bacterianas. Una defensa poderosa es un conjunto de diminutas bombas que expulsan los antibióticos fuera de la célula antes de que puedan hacer daño. Este estudio desvela la estructura detallada y el modelo de funcionamiento de una de esas bombas, llamada EmrAB-TolC, en Escherichia coli. Al mostrar cómo esta máquina atraviesa las dos capas protectoras de la célula y expulsa fármacos en un solo paso, el trabajo ofrece nuevas ideas para desactivar las defensas bacterianas y aumentar la eficacia de los medicamentos existentes.
El reto de introducir fármacos en bacterias resistentes
Muchas bacterias peligrosas están envueltas no en una sino en dos membranas, con un espacio acuoso entre ellas. Esta doble cubierta dificulta que los antibióticos alcancen sus dianas. Las bacterias Gramnegativas también construyen máquinas moleculares que reconocen compuestos dañinos en el interior y los expulsan al exterior. EmrAB-TolC es una de estas máquinas y puede manejar varios antibióticos diferentes. Hasta ahora, los científicos sólo contaban con instantáneas parciales de sus piezas individuales. Las grandes incógnitas eran cómo encajaban las partes y cómo la bomba lograba mover los fármacos a través de ambas membranas de manera coordinada.
Revelando la bomba completa de dentro hacia fuera
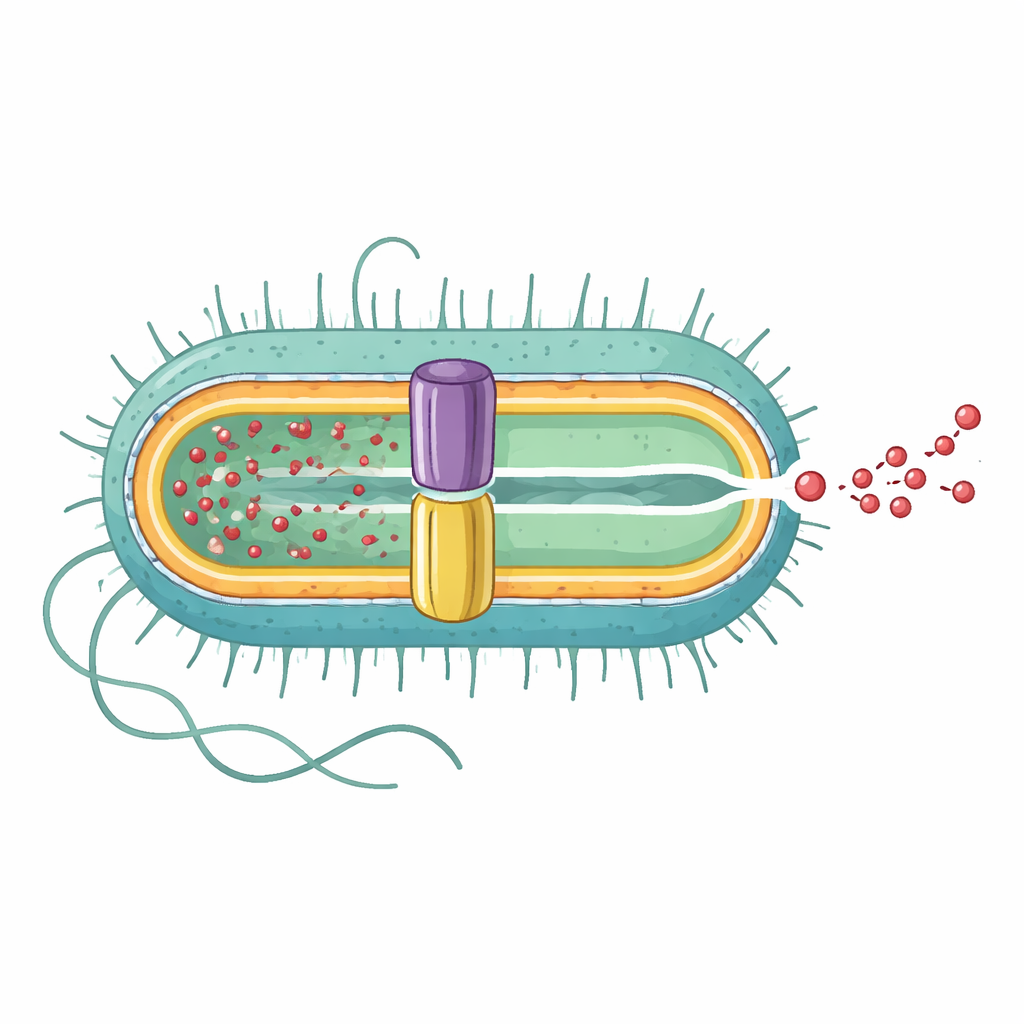
El equipo de investigación empleó microscopía crioelectrónica de alta resolución para determinar la estructura tridimensional de la bomba EmrAB-TolC completa. Encontraron que es un ensamblaje alargado compuesto por tres partes principales en una proporción 3:6:1: tres copias del canal de la membrana externa TolC, seis copias de la proteína adaptadora intermedia EmrA y una sola copia del transportador de la membrana interna EmrB. Juntos forman un túnel continuo de aproximadamente 320 angstrom que llega desde la membrana interna, a través del espacio periplásmico, hasta el exterior. EmrA forma una manga hexagonal entre TolC y EmrB, dando forma a un nanochannel central, mientras que TolC se abre ampliamente donde contacta con EmrA, creando una vía de salida directa hacia el exterior celular.
El motor interno que impulsa la exportación de fármacos
En la base del ensamblaje se encuentra EmrB, miembro de una amplia familia de transportadores que usa el flujo de protones —las partículas cargadas que definen la acidez— para impulsar el movimiento de carga. EmrB contiene 14 hélices que atraviesan la membrana organizadas en dos dominios que se balancean entre sí. El análisis estructural y simulaciones por ordenador muestran que un residuo ácido clave, D29, y sus vecinos forman una red sensible a protones que puede alternar EmrB entre estados abiertos hacia el interior y hacia el exterior. Mutaciones en D29 y posiciones cercanas reducen drásticamente la resistencia celular a varios antibióticos, subrayando su importancia en acoplar el movimiento de protones al transporte de fármacos, aunque el flujo de protones también puede implicar residuos adicionales.
Una ruta de escape en un solo paso a través de ambas membranas
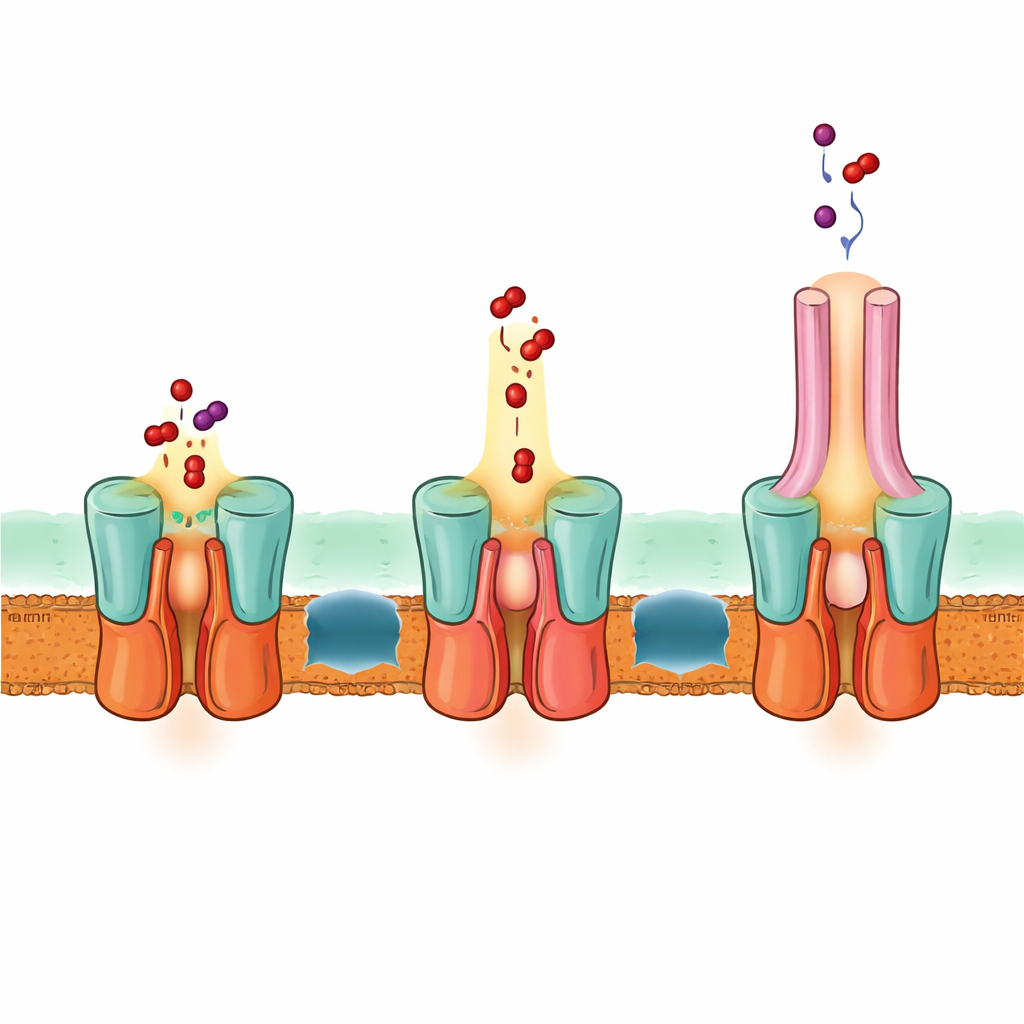
La estructura también explica cómo EmrA y EmrB se acoplan para formar un conducto sellado. Un haz de hélices extendidas en el lado periplásmico de EmrB encaja en una región anular de EmrA, bloqueando el transportador al adaptador. Esta disposición crea una cavidad espaciosa que puede recibir fármacos liberados por EmrB y guiarlos hacia el canal de EmrA y luego hacia TolC. Basándose en la estructura, predicciones computacionales y pruebas mutacionales, los autores proponen que EmrB captura fármacos de la membrana interna o del citoplasma, luego se balancea para abrirse hacia EmrA y liberarlos en esta cavidad compartida. Un bucle flexible dentro de EmrA conforma un pasaje estrecho que embudo los fármacos hacia arriba, a través del adaptador y fuera por TolC, todo ello sin que los fármacos difundan libremente en el espacio entre membranas.
Qué significa esto para combatir la resistencia
En conjunto, el trabajo respalda un modelo en el que EmrAB-TolC realiza una exportación en un solo paso de antibióticos, directamente desde el interior de la célula al exterior. La bomba usa el flujo de protones para impulsar cambios de forma repetidos en EmrB, que a su vez empujan los fármacos hacia un canal continuo formado por EmrA y TolC. Al identificar características estructurales esenciales para el ensamblaje y la función, como anillos hidrofóbicos en EmrA y residuos clave en EmrB, el estudio destaca puntos débiles potenciales donde pequeñas moléculas podrían bloquear la bomba. Dirigirse a esos puntos podría ayudar a restaurar la potencia de los antibióticos existentes contra patógenos Gramnegativos que actualmente resisten el tratamiento.
Cita: Zhong, Z., Maimaiti, T., Jackson, M.L. et al. A model for drug transport across two membranes of Gram-negative bacteria by an MFS tripartite assembly. Nat Commun 17, 4039 (2026). https://doi.org/10.1038/s41467-026-70500-5
Palabras clave: resistencia a antibióticos, bomba de expulsión, bacterias Gramnegativas, transporte de fármacos, EmrAB-TolC