Clear Sky Science · zh
使用小型支架蛋白对细胞外囊泡进行工程化
小巧的信使,巨大的医疗潜力
当今许多药物难以精确到达特定细胞而不在别处产生副作用。该研究探讨如何将体内的纳米级“信使小包”——细胞外囊泡,改造为更智能的药物与抗炎蛋白递送载体。通过发现并优化一种能将货物装入这些囊泡的小型支架蛋白,研究者构建了定制颗粒,能够抑制败血症中的危险性炎症并保护骨关节炎中受损的关节。 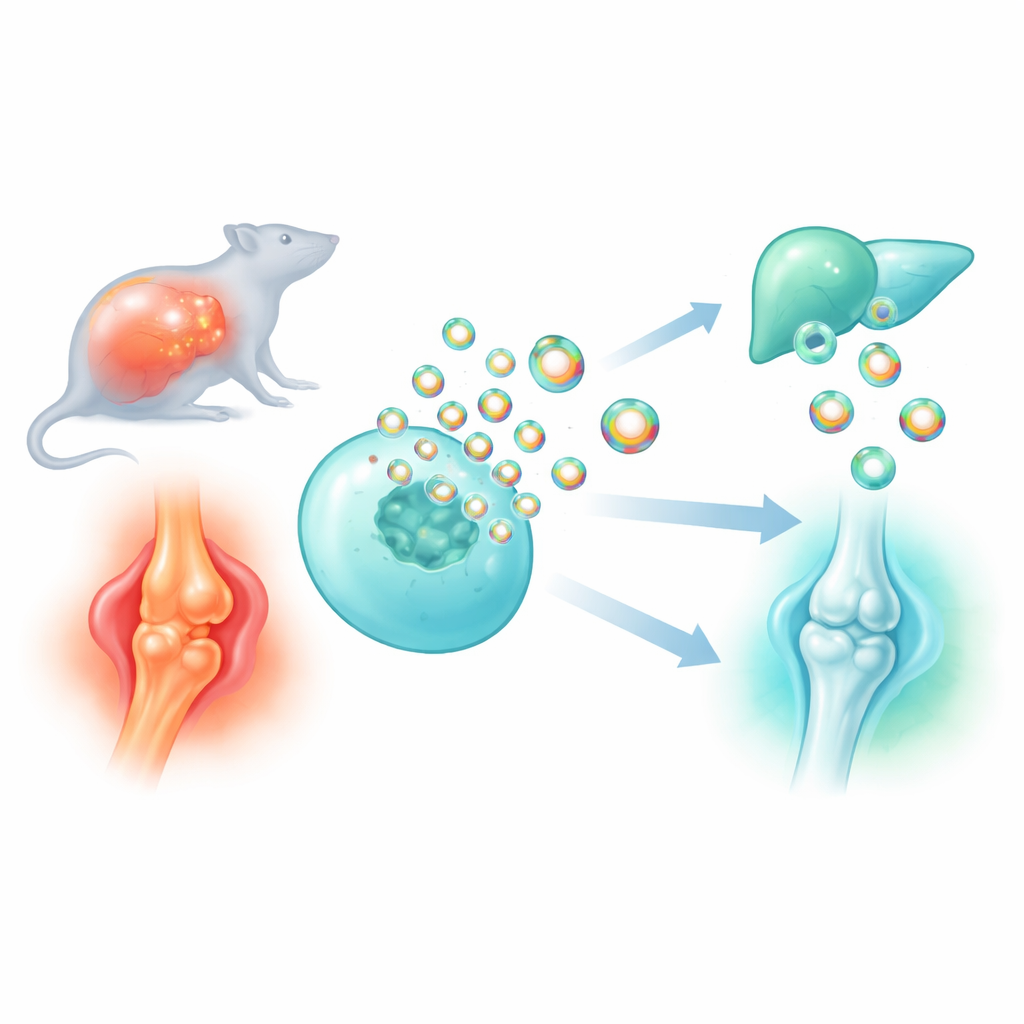
将天然包裹体转为目标化载体
细胞不断脱落称为细胞外囊泡(EVs)的小型膜泡。这些囊泡天然携带蛋白质和遗传物质在细胞间传递,并能穿过常阻挡合成纳米颗粒的生物屏障。这使得EVs成为有吸引力的“活体”递送工具,但问题在于:如何将足够多的有效货物装入它们,或在其表面展示合适的分子。现有用于将货物导入EVs的“支架”蛋白往往体积较大、结构复杂或分布不均,限制了每个囊泡可装载的治疗物质,并引发安全性顾虑。
寻找小而强大的支架
为了解决这一问题,团队系统性地筛查了常用人源细胞系产生的EVs上出现的蛋白。通过三种独立的纯化方法和质谱,他们将候选蛋白缩减为15个,并将每个蛋白与荧光报告蛋白融合以测量其被分选入囊泡的效率。其中一个脱颖而出:ENPP1,其装载货物的效率优于常用支架如PTGFRN和Lamp2b。研究者随后将ENPP1修剪为多个更短的片段,发现EN144——仅144个氨基酸的片段——能将报告蛋白装入EVs的量提升三倍,相比全长ENPP1,同时保持囊泡的大小和结构完整。 
对基因和蛋白货物都安全且多用途的载体
鉴于任何递送系统都必须安全,研究者在多种细胞类型和小鼠中测试了装饰了EN144的EVs。这些囊泡表现出典型的EV标志,尺寸在正常范围内,并且即便在高剂量或反复给药下也几乎没有毒性。注射到小鼠体内后,EN144-EVs主要在肝脏和脾脏累积,类似于标准EVs,且未对器官造成损伤或扰乱血液化学指标。随后团队展示了EN144可作为多种货物的分子对接平台:通过将其与一种趋向软骨的肽偶联,他们生成了被软骨细胞(维持关节软骨的细胞)高效摄取的EVs;通过引入RNA结合基序,他们在EVs内富集了治疗性mRNA,并证实受体细胞能将该mRNA翻译为蛋白质;他们还通过设计的蛋白—蛋白互作装载CRISPR–Cas9基因编辑复合体,并证明EV递送的编辑器能在靶细胞中激活沉默的报告基因。
吸附有害信号的诱饵囊泡
如败血症和骨关节炎等炎症性疾病部分由细胞因子白细胞介素-6(IL-6)驱动,当IL-6与可溶性受体形成复合物时,会以有害的“转信号”模式发挥作用。为了选择性阻断该有害途径而不抑制IL-6的有益功能,作者将EN144与gp130(一种关键的IL-6信号转导分子)融合,生成在表面展示gp130作为诱饵的EVs。在细胞培养中,这些诱饵囊泡显著降低了炎性细胞因子的产生。在败血症小鼠模型中,携带gp130的EVs降低了器官中的IL-6水平,抑制了下游信号通路,并显著提高了存活率,优于等量的可溶性gp130蛋白。该囊泡特异性结合IL-6–受体复合物,抑制促炎通路,同时在很大程度上保留了经典的、对正常反应重要的IL-6信号传导。
通过定位软骨保护受损关节
为了解决骨关节炎问题,团队将靶向与诱饵策略结合起来。他们在携带gp130的EN144 EVs上附加了趋向软骨的肽,产生既能归巢到软骨细胞又能中和IL-6转信号的颗粒。在暴露于炎性刺激的培养软骨细胞中,这些靶向诱饵EVs提高了细胞存活和迁移,减少了细胞死亡。在手术诱导的骨关节炎大鼠中,多次注射到关节腔后,这些EVs在软骨中的滞留显著增强,关节表面破坏减少,显微镜下软骨更健康。组织损伤标志物下降,而维持软骨的结构蛋白增加,关节衬里中免疫细胞的构成也向更有助修复、炎症较少的方向转变。
从微小支架到广泛的治疗平台
通过将EN144打造成一个最小而高效的支架,这项工作将天然存在的细胞外囊泡转化为灵活的治疗平台。同一小型锚定件既可在囊泡表面展示靶向标签和诱饵受体,又可在囊泡内部装载基因或蛋白货物,且其安全性与未修饰的囊泡相当。在动物模型中,基于EN144的“诱饵EVs”成功抑制了危及生命的炎症并保护了受损关节。对普通读者而言,这意味着我们可能正朝着用体内自身的递送包裹体构建的药物迈进——这些药物经过精确工程化,能把合适的工具送到合适的位置,并压制有害信号而不关闭身体的正常防御机制。
引用: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
关键词: 细胞外囊泡, 药物递送, 炎症, 败血症, 骨关节炎