Clear Sky Science · es
Ingeniería de vesículas extracelulares usando una pequeña proteína andamiaje
Pequeños mensajeros con gran promesa médica
Muchos de los medicamentos actuales tienen dificultades para alcanzar exactamente las células adecuadas sin provocar efectos secundarios en otras partes del cuerpo. Este estudio explora cómo convertir los “paquetes mensajeros” nanosized del propio organismo, denominados vesículas extracelulares, en vehículos de entrega más inteligentes para fármacos y proteínas antiinflamatorias. Al descubrir y refinar una proteína andamiaje muy pequeña que facilita el empaquetado de carga en estas vesículas, los investigadores construyen partículas a medida que calman la inflamación peligrosa en la sepsis y protegen las articulaciones dañadas en la artrosis. 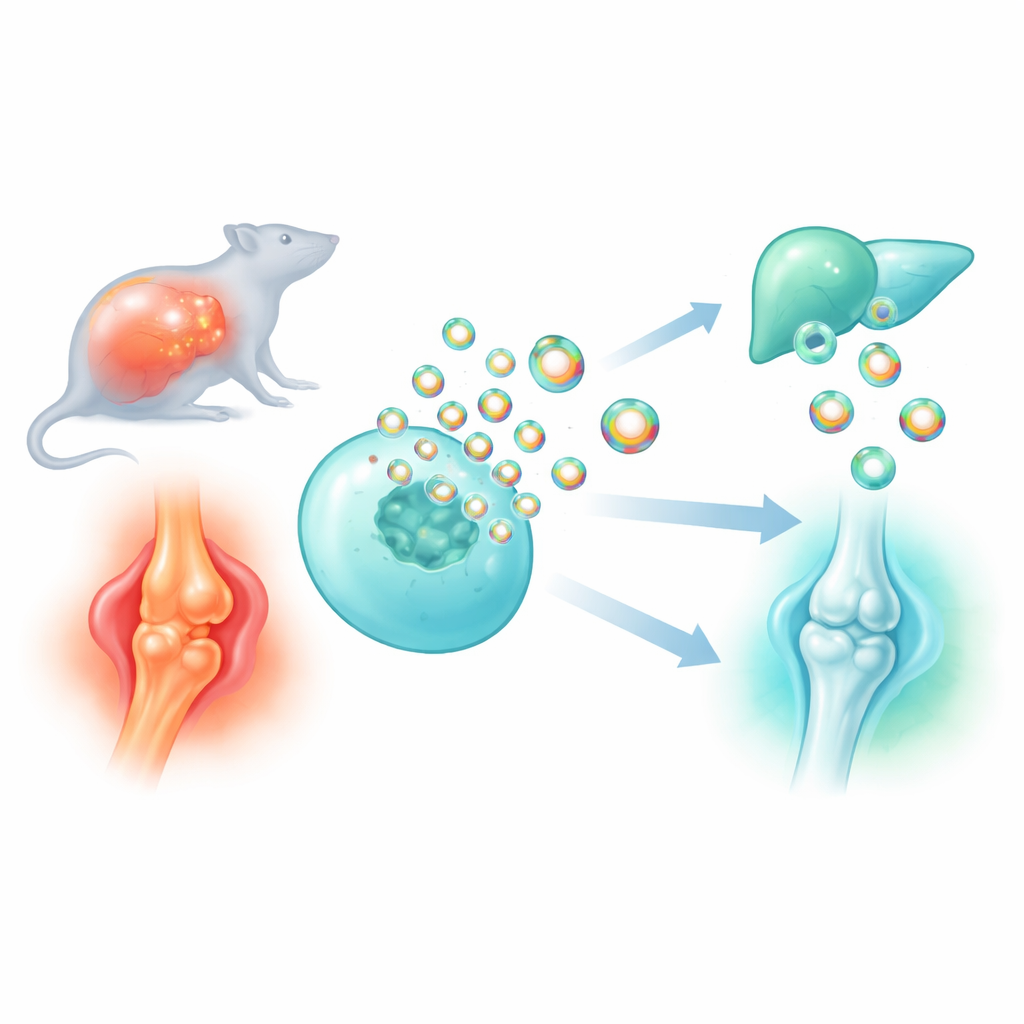
Paquetes naturales convertidos en transportadores dirigidos
Las células desprenden constantemente pequeñas burbujas de membrana conocidas como vesículas extracelulares (VE). Estos paquetes transportan de forma natural proteínas y material genético entre células y pueden atravesar barreras biológicas que a menudo bloquean a las nanopartículas sintéticas. Esto hace que las VE sean atractivas como camionetas vivas de entrega para terapias, pero hay un inconveniente: cargar suficiente material útil en su interior, o mostrar las moléculas adecuadas en su superficie, ha sido difícil. Las proteínas “andamiaje” existentes que dirigen la carga hacia las VE pueden ser voluminosas, complejas o presentarse de forma desigual, lo que limita la cantidad de material terapéutico que se puede empaquetar en cada vesícula y plantea preocupaciones de seguridad.
Encontrar un andamiaje pequeño pero poderoso
Para resolver esto, el equipo examinó sistemáticamente proteínas que aparecen en las VE producidas por una línea celular humana de uso habitual. Usando tres métodos independientes de purificación y espectrometría de masas, seleccionaron 15 candidatos y fusionaron cada uno con un reportero fluorescente para medir con qué eficiencia se ordenaba en las vesículas. Uno destacó: ENPP1, que cargó la carga más eficazmente que andamiajes ampliamente usados, como PTGFRN y Lamp2b. Los científicos recortaron entonces ENPP1 en varias versiones más cortas y descubrieron EN144, un fragmento de apenas 144 aminoácidos, que empaquetó tres veces más proteína reportera en las VE que la ENPP1 de longitud completa, manteniendo el tamaño y la estructura de las vesículas intactos. 
Vehículos seguros y versátiles para carga genética y proteica
Dado que cualquier sistema de entrega debe ser seguro, los investigadores probaron las VE decoradas con EN144 en múltiples tipos celulares y en ratones. Las vesículas mostraron marcadores típicos de VE, se mantuvieron dentro de los rangos de tamaño normales y causaron poca o ninguna toxicidad, incluso en dosis altas o repetidas. Tras la inyección en ratones, las EN144-VE se acumularon principalmente en el hígado y el bazo, de forma similar a las VE estándar, sin dañar los órganos ni alterar la química sanguínea. El equipo mostró además que EN144 puede usarse como una estación de acoplamiento molecular para muchos tipos de carga. Al acoplarla a un péptido con afinidad por el cartílago, crearon VE que fueron absorbidas eficientemente por condrocitos, las células que mantienen el cartílago articular. Usando motivos de unión a ARN, enriquecieron ARNm terapéutico dentro de las VE y confirmaron que las células receptoras tradujeron ese ARNm a proteína. También cargaron complejos de edición génica CRISPR–Cas9 mediante parejas proteicas diseñadas y demostraron que los editores entregados por VE podían activar un gen reportero silenciado en células diana.
Vesículas señuelo que absorben señales perjudiciales
Enfermedades inflamatorias como la sepsis y la artrosis están impulsadas en parte por la citocina interleucina-6 (IL-6), que puede actuar en un modo dañino de “trans-señalización” cuando forma complejos con un receptor soluble. Para bloquear selectivamente esta vía perjudicial sin apagar los roles beneficiosos de la IL-6, los autores fusionaron EN144 con gp130, un transductor clave de la señal de IL-6, creando VE que muestran gp130 como un señuelo en su superficie. En cultivo celular, estas vesículas señuelo redujeron drásticamente la producción de citocinas inflamatorias. En un modelo de sepsis en ratones, las VE portadoras de gp130 redujeron los niveles de IL-6 en los órganos, atenuaron la señalización downstream y mejoraron notablemente la supervivencia, superando dosis de proteína gp130 soluble. Las vesículas se unieron específicamente a los complejos IL-6–receptor, frenando la vía proinflamatoria mientras dejaban en gran medida intacta la señalización clásica de IL-6, importante para las respuestas normales.
Protegiendo articulaciones desgastadas al dirigirse al cartílago
Para abordar la artrosis, el equipo combinó estrategias de orientación y de señuelo. Añadieron el péptido con afinidad por el cartílago a las VE EN144 portadoras de gp130, generando partículas que tanto se dirigen a los condrocitos como neutralizan la trans-señalización de IL-6. En condrocitos cultivados expuestos a señales inflamatorias, estas VE señuelo dirigidas aumentaron la supervivencia y la migración celular mientras reducían la muerte celular. En ratas con artrosis inducida quirúrgicamente, inyecciones repetidas en la cavidad articular llevaron a una fuerte retención de las VE en el cartílago, menor degradación de la superficie articular y cartílago más sano al observarlo con el microscopio. Los marcadores de daño tisular disminuyeron, mientras que las proteínas estructurales que mantienen el cartílago aumentaron, y el equilibrio de células inmunitarias en el revestimiento articular se desplazó hacia un perfil más reparador y menos inflamatorio.
De un andamiaje minúsculo a una plataforma terapéutica amplia
Al definir EN144 como un andamiaje mínimo y de alto rendimiento, este trabajo convierte las vesículas extracelulares naturales en una plataforma terapéutica flexible. El mismo ancla pequeña puede mostrar etiquetas de direccionamiento y receptores señuelo en la superficie de la vesícula al tiempo que carga material genético o proteico en su interior, todo con un perfil de seguridad similar al de las vesículas no modificadas. En modelos animales, las “VE señuelo” basadas en EN144 lograron domar inflamaciones potencialmente mortales y proteger articulaciones dañadas. Para un público general, la implicación es que podríamos avanzar hacia medicamentos construidos a partir de los propios paquetes de entrega del cuerpo, diseñados con precisión para llevar las herramientas adecuadas al lugar correcto y silenciar señales dañinas sin anular las defensas normales del organismo.
Cita: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Palabras clave: vesículas extracelulares, administración de fármacos, inflamación, sepsis, artrosis