Clear Sky Science · ru
Инжиниринг внеклеточных везикул с использованием небольшого каркасного белка
Крошечные курьеры с большим медицинским потенциалом
Многие современные лекарства испытывают трудности с доставкой точно в нужные клетки, не вызывая побочных эффектов в других тканях. В этом исследовании изучают, как превращать собственные наноскопические «пакетики‑курьеры» организма, называемые внеклеточными везикулами, в более умные транспортные средства для лекарств и противовоспалительных белков. Открыв и оптимизировав очень небольшой каркасный белок, который помогает упаковывать полезную нагрузку в эти везикулы, исследователи создали дизайнерские частицы, которые уменьшают опасное воспаление при сепсисе и защищают изношенные суставы при остеоартрите. 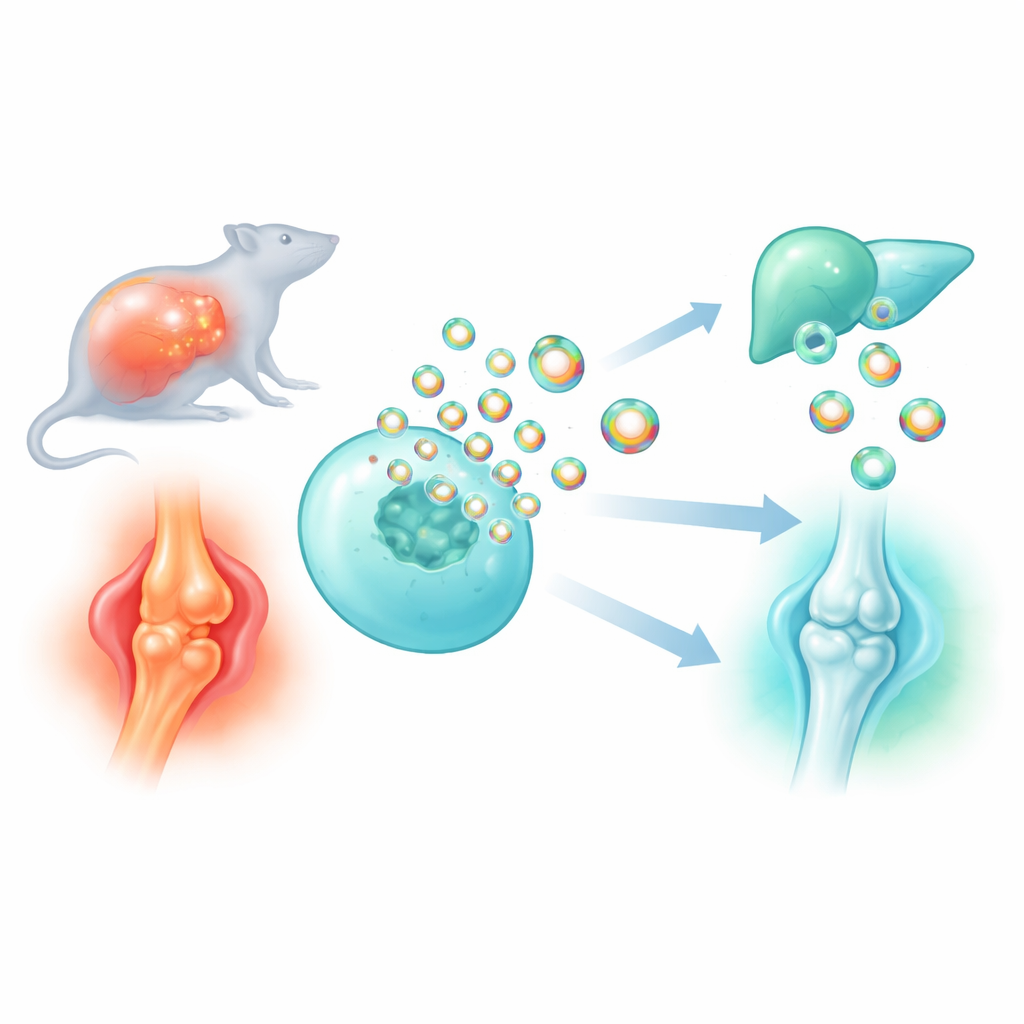
Природные упаковки, превращённые в целевые носители
Клетки постоянно сбрасывают крошечные мембранные пузырьки, известные как внеклеточные везикулы (EV). Эти пакеты естественно переносят белки и генетический материал между клетками и способны проходить через биологические барьеры, которые часто препятствуют синтетическим наночастицам. Это делает EV привлекательными как «живые» транспортные средства для терапии, но есть загвоздка: трудно загрузить в них достаточное количество полезного вещества или выставить на поверхности нужные молекулы. Существующие «каркасные» белки, направляющие груз в EV, могут быть громоздкими, сложными или присутствовать неравномерно, что ограничивает объём терапевтического материала в каждой везикуле и вызывает опасения по части безопасности.
Нахождение маленького, но мощного каркаса
Чтобы решить эту проблему, группа систематически обследовала белки, которые встречаются на EV, производимых часто используемой линией человеческих клеток. Применив три независимых метода очистки и масс‑спектрометрию, они отобрали 15 кандидатов и слили каждый из них с флуоресцентным репортером, чтобы измерить, насколько эффективно он сортируется в везикулы. Выделился один — ENPP1, который грузил полезную нагрузку эффективнее, чем широко используемые каркасы, такие как PTGFRN и Lamp2b. Ученые затем укорачивали ENPP1 до нескольких более коротких версий и обнаружили EN144 — фрагмент всего из 144 аминокислот, который упаковывал в везикулы в три раза больше репортерного белка, чем полная форма ENPP1, при этом не меняя размер и структуру везикул. 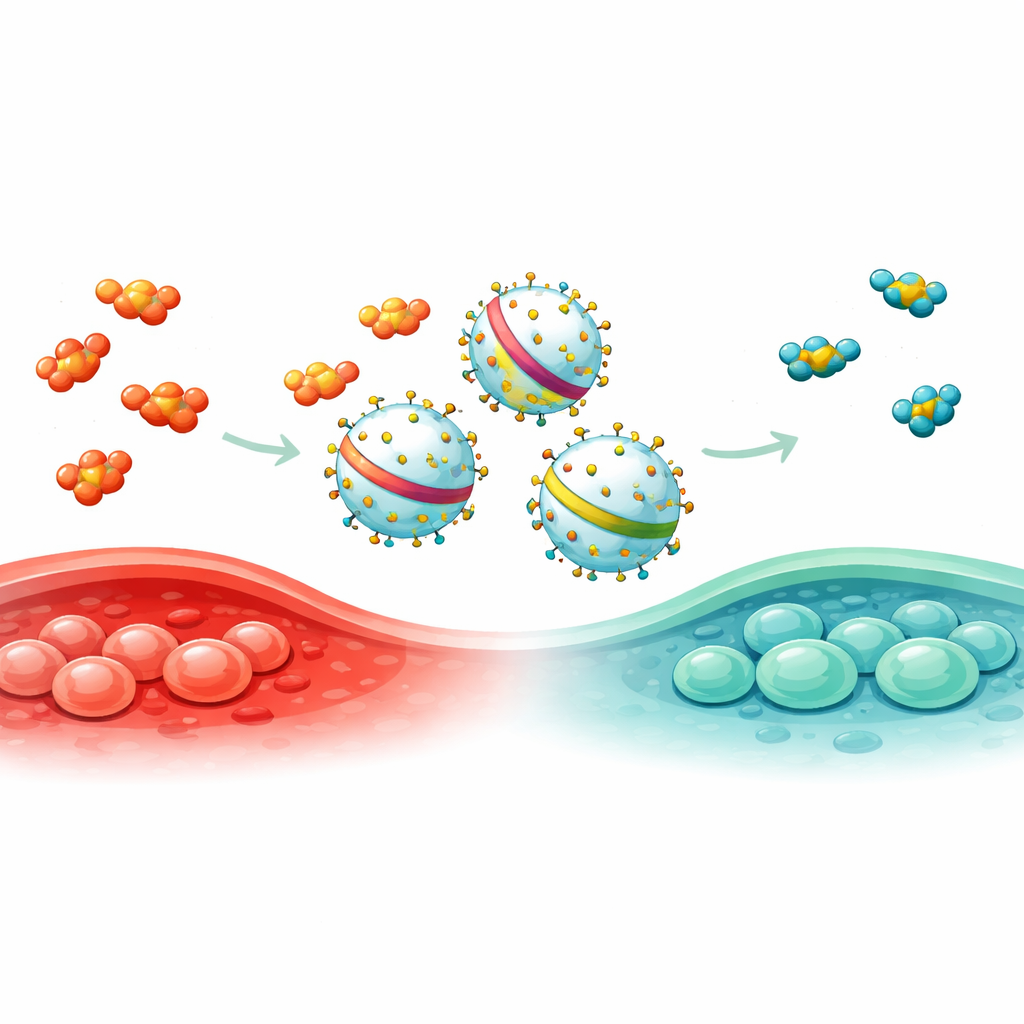
Безопасные и универсальные носители для генетического и белкового груза
Поскольку любая система доставки должна быть безопасной, исследователи протестировали EV, украшенные EN144, в нескольких типах клеток и у мышей. Везикулы демонстрировали типичные маркеры EV, оставались в пределах нормальных размеров и вызывали минимальную или нулевую токсичность даже при высоких или повторных дозах. После введения мышам EN144‑EV преимущественно накапливались в печени и селезёнке, как и стандартные EV, не повреждая органы и не нарушая показателей крови. Команда также показала, что EN144 можно использовать как молекулярную док‑станцию для разных типов груза. Соединив его с пептидом, направляющим в хрящ, они создали EV, которые эффективно поглощались хондроцитами — клетками, поддерживающими суставной хрящ. С помощью мотивов связывания РНК они обогатили терапевтическую мРНК внутри везикул и подтвердили, что принимающие клетки переводят эту мРНК в белок. Они также загрузили комплексы CRISPR–Cas9 через сконструированные пары белок–белок и показали, что доставленные EV редакторы могут активировать «молчащий» репортерный ген в целевых клетках.
Декой‑везикулы, поглощающие вредные сигналы
Воспалительные болезни, такие как сепсис и остеоартрит, частично управляются цитокином интерлейкином‑6 (IL‑6), который может действовать в повреждающем режиме «транс‑сигналинга», когда образует комплексы с растворимым рецептором. Чтобы избирательно блокировать этот вредный путь, не подавляя полезные функции IL‑6, авторы сшили EN144 с gp130, ключевым трансдьюсером сигнала IL‑6, создав EV, которые выставляют gp130 на своей поверхности в роли «приманки». В культуре клеток эти декой‑везикулы резко снизили выработку провоспалительных цитокинов. В модели сепсиса у мышей EV, несущие gp130, снижали уровни IL‑6 в органах, ослабляли последующие сигнальные каскады и заметно повышали выживаемость, превосходя по эффекту введение растворимого gp130. Везикулы специфически связывали комплексы IL‑6 с рецептором, сдерживая провоспалительный путь и при этом в основном не нарушая классическую сигнальную функцию IL‑6, важную для нормальных ответов организма.
Защита изношенных суставов за счёт нацеливания на хрящ
Для лечения остеоартрита команда объединила стратегии таргетинга и приманки. Они добавили пептид, ориентирующий в хрящ, к gp130‑несущим EN144‑EV, получив частицы, которые и направляются в хондроциты, и нейтрализуют транс‑сигналинг IL‑6. В культивируемых хондроцитах, подвергнутых воспалительным раздражителям, эти целевые декой‑везикулы повышали выживаемость и подвижность клеток, одновременно снижая клеточную гибель. У крыс с хирургически индуцированным остеоартритом повторные инъекции в полость сустава приводили к сильной ретенции EV в хряще, меньшему разрушению суставной поверхности и более здоровой структуре хряща при микроскопическом исследовании. Маркеры повреждения ткани снижались, тогда как структурные белки, поддерживающие хрящ, увеличивались, а соотношение иммунных клеток в синовиальной оболочке смещалось в сторону более восстанавливающего, менее воспалительного профиля.
От крошечного каркаса к широкой терапевтической платформе
Выделив EN144 как минимальный, высокоэффективный каркас, эта работа превращает естественные внеклеточные везикулы в гибкую терапевтическую платформу. Один и тот же маленький якорь может демонстрировать метки для нацеливания и декой‑рецепторы на поверхности везикул, одновременно загружать генетический или белковый груз внутрь, при этом обеспечивать профиль безопасности, сопоставимый с немодифицированными везикулами. В животных моделях EN144‑основанные «декой‑EV» успешно усмиряли угрожающее жизни воспаление и защищали повреждённые суставы. Для неспециалиста это означает, что мы, возможно, движемся к лекарствам, созданным из собственных «почтовых» пакетов организма, точно встроенным, чтобы доставлять нужные инструменты в нужное место и притушивать вредные сигналы, не подавляя при этом нормальные защитные функции организма.
Цитирование: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Ключевые слова: внеклеточные везикулы, доставка лекарств, воспаление, сепсис, остеоартрит