Clear Sky Science · fr
Ingénierie de vésicules extracellulaires à l’aide d’une petite protéine d’échafaudage
Petits coursiers au grand potentiel médical
De nombreux médicaments peinent aujourd’hui à atteindre précisément les cellules ciblées sans provoquer d’effets indésirables ailleurs. Cette étude explore comment transformer les « paquets » nanoscalaires naturels du corps, appelés vésicules extracellulaires, en véhicules de livraison plus intelligents pour des médicaments et des protéines anti-inflammatoires. En découvrant et en raffinant une très petite protéine d’échafaudage qui aide à empaqueter la cargaison dans ces vésicules, les chercheurs conçoivent des particules sur mesure qui apaisent l’inflammation dangereuse de la septicémie et protègent les articulations usées dans l’ostéoarthrite. 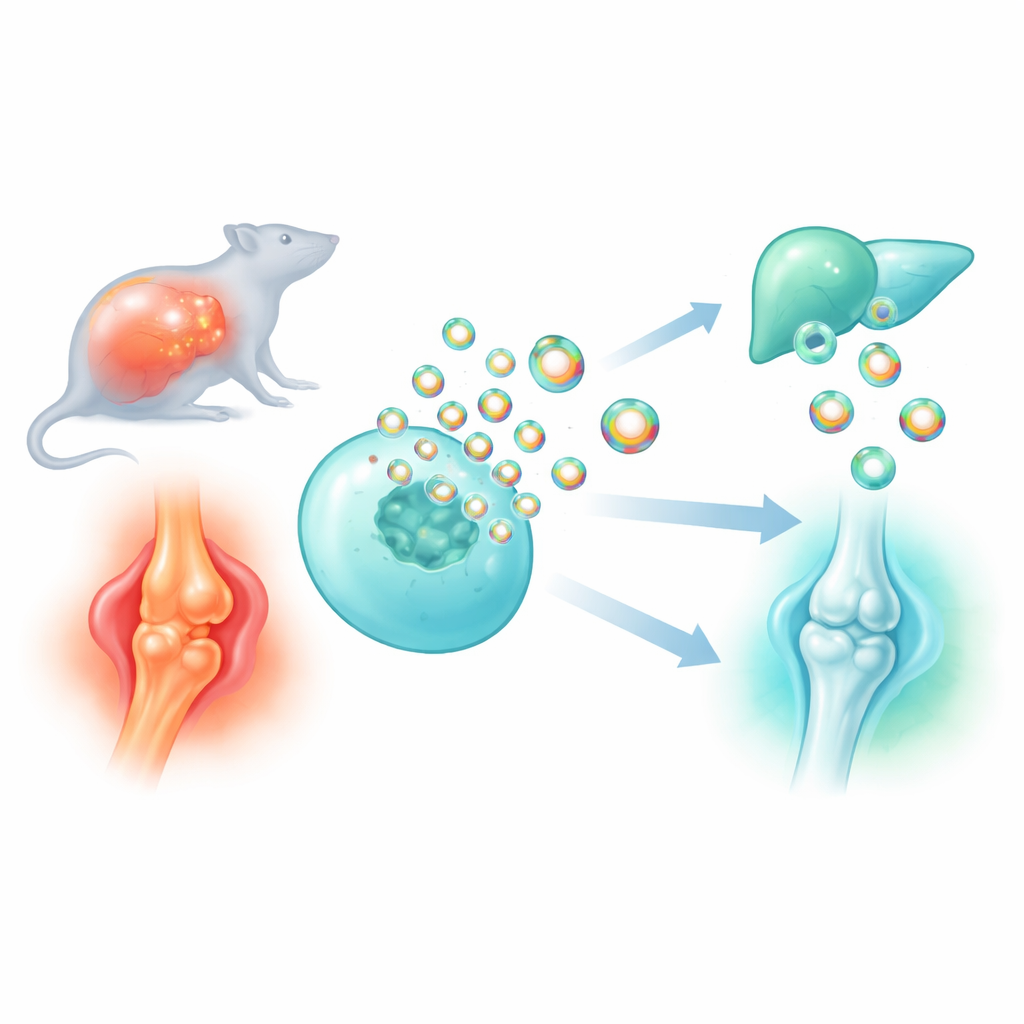
Des enveloppes naturelles transformées en vecteurs ciblés
Les cellules libèrent en permanence de minuscules bulles membranaires appelées vésicules extracellulaires (VE). Ces paquets transportent naturellement des protéines et du matériel génétique entre les cellules et peuvent franchir des barrières biologiques qui bloquent souvent les nanoparticules synthétiques. Cela rend les VE intéressantes comme « camions » vivants pour la thérapie, mais il y a un bémol : il est difficile d’y charger suffisamment de cargaison utile ou d’exposer les bonnes molécules à leur surface. Les protéines d’« échafaudage » existantes qui dirigent la cargaison vers les VE peuvent être volumineuses, complexes ou présentes de manière inégale, ce qui limite la quantité de matériel thérapeutique pouvant être embarquée dans chaque vésicule et soulève des problèmes de sécurité.
Trouver un échafaudage petit mais performant
Pour résoudre ce problème, l’équipe a passé en revue systématiquement les protéines présentes sur les VE produits par une lignée cellulaire humaine couramment utilisée. Employant trois méthodes de purification indépendantes et la spectrométrie de masse, ils ont présélectionné 15 candidats et ont fusionné chacun à un marqueur fluorescent pour mesurer l’efficacité de leur tri vers les vésicules. Un candidat s’est distingué : ENPP1, qui a chargé la cargaison plus efficacement que des échafaudages largement utilisés tels que PTGFRN et Lamp2b. Les scientifiques ont ensuite tronqué ENPP1 en plusieurs versions plus courtes et découvert EN144, un fragment de seulement 144 acides aminés, qui a empaqueté trois fois plus de protéine marqueuse dans les VE que l’ENPP1 en pleine longueur, tout en conservant la taille et la structure des vésicules. 
Véhicules sûrs et polyvalents pour cargaisons génétiques et protéiques
Parce qu’un système de livraison doit être sûr, les chercheurs ont testé les VE décorés par EN144 sur plusieurs types cellulaires et chez la souris. Les vésicules affichaient des marqueurs typiques de VE, restaient dans des plages de taille normales et causaient peu ou pas de toxicité, même à doses élevées ou répétées. Après injection chez la souris, les EN144-VE s’accumulaient principalement dans le foie et la rate, comme les VE standards, sans endommager les organes ni perturber la chimie sanguine. L’équipe a ensuite montré qu’EN144 peut servir de point d’ancrage moléculaire pour de nombreux types de cargaison. En le couplant à un peptide ciblant le cartilage, ils ont créé des VE efficacement internalisés par les chondrocytes, les cellules qui entretiennent le cartilage articulaire. En utilisant des motifs liant l’ARN, ils ont enrichi l’ARNm thérapeutique à l’intérieur des VE et confirmé que les cellules réceptrices traduisaient cet ARNm en protéine. Ils ont aussi chargé des complexes CRISPR–Cas9 via des paires protéine–protéine ingénierées et démontré que les éditeurs délivrés par VE pouvaient activer un gène rapporteur silencieux dans les cellules cibles.
Vésicules leurres qui absorbent les signaux nocifs
Les maladies inflammatoires comme la septicémie et l’ostéoarthrite sont en partie pilotées par la cytokine interleukine-6 (IL-6), qui peut agir de manière dommageable par un mode de « trans‑signalisation » lorsqu’elle forme des complexes avec un récepteur soluble. Pour bloquer sélectivement cette voie néfaste sans supprimer les rôles bénéfiques de l’IL-6, les auteurs ont fusionné EN144 au gp130, un transducteur clé du signal IL-6, créant des VE qui exposent gp130 comme leurre à leur surface. En culture cellulaire, ces vésicules leurres ont fortement réduit la production de cytokines inflammatoires. Dans un modèle murin de septicémie, les VE portant gp130 ont abaissé les niveaux d’IL-6 dans les organes, atténué la signalisation en aval et grandement amélioré la survie, surpassant des doses de protéine gp130 soluble. Les vésicules se lient spécifiquement aux complexes IL-6–récepteur, limitant la voie pro-inflammatoire tout en laissant en grande partie intacte la signalisation classique de l’IL-6, importante pour les réponses physiologiques normales.
Protéger les articulations usées en visant le cartilage
Pour traiter l’ostéoarthrite, l’équipe a combiné stratégies de ciblage et de leurre. Ils ont ajouté le peptide homing du cartilage aux VE EN144 portant gp130, générant des particules à la fois ciblées vers les chondrocytes et capables de neutraliser la trans‑signalisation de l’IL-6. Dans des chondrocytes en culture exposés à des signaux inflammatoires, ces VE leurres ciblés ont amélioré la survie et la mobilité cellulaire tout en réduisant la mort cellulaire. Chez des rats présentant une ostéoarthrite induite chirurgicalement, des injections répétées dans la cavité articulaire ont entraîné une forte rétention des VE dans le cartilage, une moindre dégradation de la surface articulaire et un cartilage mieux préservé à l’examen histologique. Les marqueurs de dommage tissulaire ont diminué, tandis que les protéines structurales maintenant le cartilage ont augmenté, et l’équilibre des cellules immunitaires dans la membrane synoviale a évolué vers un profil plus réparateur et moins inflammatoire.
Du petit échafaudage à une plateforme thérapeutique large
En isolant EN144 comme un échafaudage minimal et performant, ce travail transforme les vésicules extracellulaires naturelles en une plateforme thérapeutique flexible. Le même petit ancrage peut afficher des étiquettes de ciblage et des récepteurs leurres à la surface des vésicules tout en chargeant de la cargaison génétique ou protéique à l’intérieur, le tout avec un profil de sécurité similaire à celui des vésicules non modifiées. Dans des modèles animaux, des « VE leurres » basés sur EN144 ont réussi à maîtriser une inflammation potentiellement mortelle et à protéger des articulations endommagées. Pour le grand public, l’idée est que nous pourrions nous diriger vers des médicaments construits à partir des propres paquets de livraison du corps, précisément conçus pour apporter les bons outils au bon endroit et étouffer les signaux nuisibles sans neutraliser les défenses normales de l’organisme.
Citation: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Mots-clés: vésicules extracellulaires, vectorisation de médicaments, inflammation, septicémie, ostéoarthrite