Clear Sky Science · pl
Inżynieria pęcherzyków zewnątrzkomórkowych przy użyciu małego białka rusztowaniowego
Maleńcy kurierzy o wielkiej nadziei medycznej
Wiele współczesnych leków ma trudność z dotarciem dokładnie do odpowiednich komórek bez wywoływania skutków ubocznych gdzie indziej. W tym badaniu analizuje się, jak przekształcić naturalne nanorpaczki organizmu — zwane pęcherzykami zewnątrzkomórkowymi — w bardziej inteligentne nośniki leków i białek przeciwzapalnych. Odkrywając i udoskonalając bardzo małe białko rusztowaniowe, które pomaga załadowywać ładunek do tych pęcherzyków, badacze zbudowali zaprojektowane cząstki, które łagodzą niebezpieczne zapalenie w sepsie i chronią zużyte stawy w chorobie zwyrodnieniowej stawów. 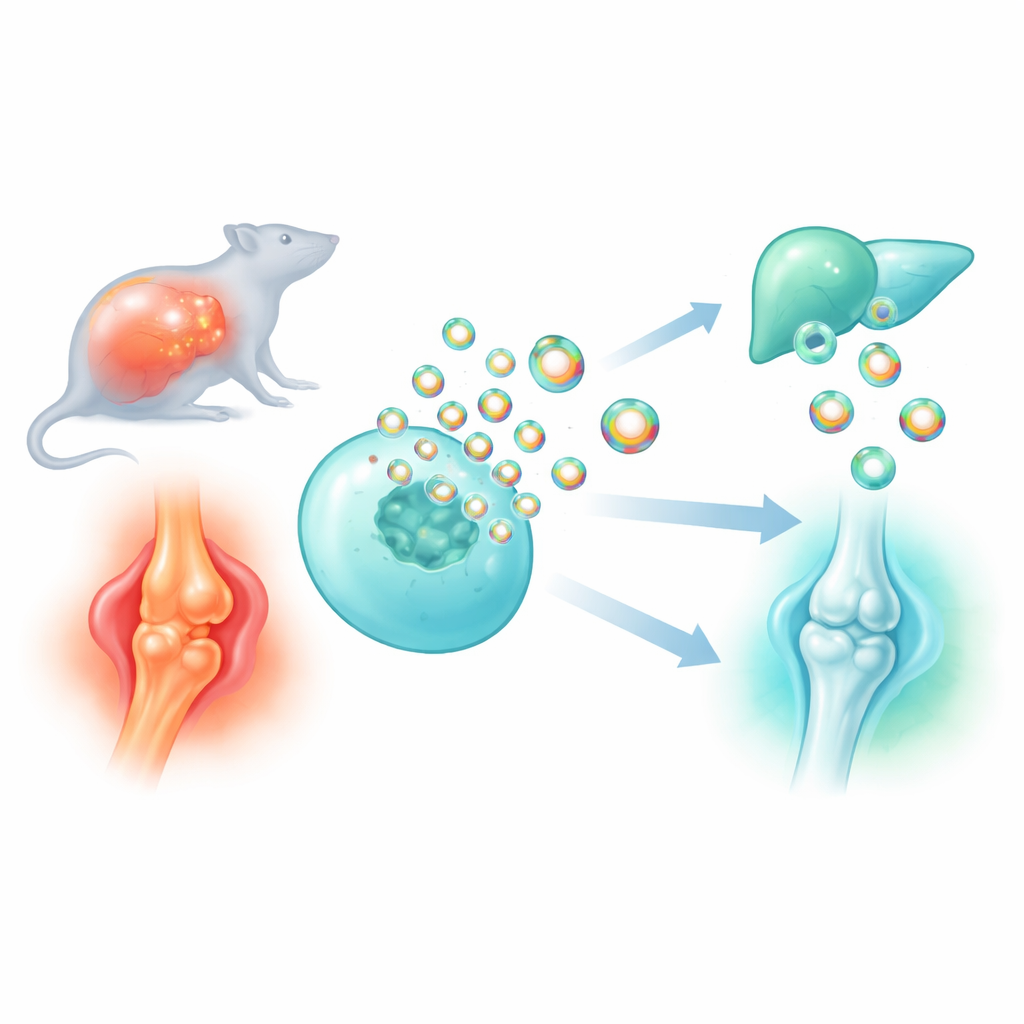
Naturalne opakowania przerobione na ukierunkowane nośniki
Komórki nieustannie zrzucają małe błonowe pęcherzyki znane jako pęcherzyki zewnątrzkomórkowe (EV). Te pakiety naturalnie przenoszą białka i materiał genetyczny między komórkami i potrafią przenikać bariery biologiczne, które często blokują syntetyczne nanocząstki. To sprawia, że EV są atrakcyjnymi, „żywymi” ciężarówkami do terapii, ale istnieje problem: załadowanie wystarczającej ilości użytecznego ładunku wewnątrz nich lub umieszczenie odpowiednich cząsteczek na ich powierzchni bywa trudne. Istniejące białka „rusztowaniowe”, które kierują ładunek do EV, mogą być obszerne, złożone lub występować nieregularnie, co ogranicza ilość terapeutycznych substancji mieszczących się w każdym pęcherzyku i rodzi obawy dotyczące bezpieczeństwa.
Małe, ale potężne rusztowanie
Aby to rozwiązać, zespół systematycznie przeszukał białka pojawiające się na EV produkowanych przez powszechnie stosowaną ludzką linię komórkową. Korzystając z trzech niezależnych metod oczyszczania i spektrometrii mas, sporządzili listę 15 kandydatów i połączyli każdy z raportorem fluorescencyjnym, by zmierzyć, jak efektywnie jest sortowany do pęcherzyków. Jeden kandydat wyróżnił się: ENPP1, który załadowywał ładunek efektywniej niż szeroko stosowane rusztowania, takie jak PTGFRN i Lamp2b. Naukowcy następnie skrócili ENPP1 do kilku krótszych wersji i odkryli EN144, fragment liczący zaledwie 144 aminokwasy, który pakował trzykrotnie więcej białka-raportera do EV niż pełnej długości ENPP1, przy zachowaniu rozmiaru i struktury pęcherzyków. 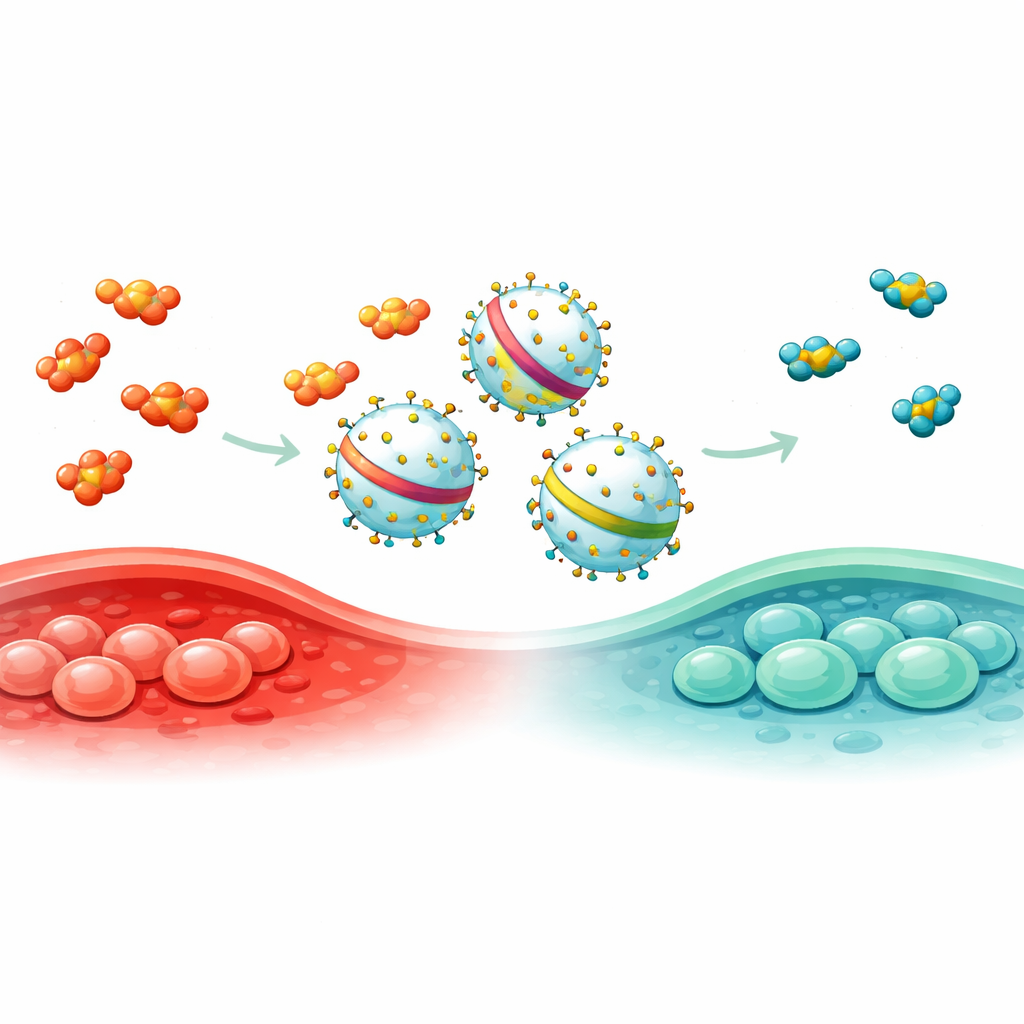
Bezpieczne, wszechstronne nośniki dla ładunku genetycznego i białkowego
Ponieważ każdy system dostarczania musi być bezpieczny, badacze przetestowali EV ozdobione EN144 w różnych typach komórek i u myszy. Pęcherzyki wykazywały typowe markery EV, mieściły się w normalnych zakresach rozmiarów i powodowały niewielką lub żadną toksyczność, nawet przy wysokich lub powtarzanych dawkach. Po wstrzyknięciu do myszy EN144-EV gromadziły się głównie w wątrobie i śledzionie, podobnie jak standardowe EV, nie uszkadzając organów ani nie zaburzając parametrów krwi. Zespół pokazał, że EN144 może służyć jak stacja dokująca dla różnych typów ładunku. Poprzez sprzężenie z peptydem kierującym do chrząstki stworzyli EV, które były efektywnie pobierane przez chondrocyty, komórki utrzymujące chrząstkę stawową. Używając motywów wiążących RNA, wzbogacili terapeutyczne mRNA w EV i potwierdzili, że komórki biorcze tłumaczą to mRNA na białko. Załadowali także kompleksy do edycji genów CRISPR–Cas9 za pomocą zaprojektowanych par białko–białko i wykazali, że edytory dostarczone przez EV mogą aktywować uśpiony gen raportera w komórkach docelowych.
Przynęty w formie pęcherzyków, które pochłaniają szkodliwe sygnały
Choroby zapalne, takie jak sepsa i choroba zwyrodnieniowa stawów, są częściowo napędzane przez cytokinę interleukinę-6 (IL-6), która może działać w szkodliwym trybie „trans-sygnałowania”, gdy tworzy kompleksy z rozpuszczalnym receptorem. Aby selektywnie zablokować tę szkodliwą drogę bez wyłączania korzystnych funkcji IL-6, autorzy połączyli EN144 z gp130, kluczowym transduktorem sygnału IL-6, tworząc EV, które eksponują gp130 jako przynętę na swojej powierzchni. W hodowlach komórkowych te przynętowe pęcherzyki wyraźnie zmniejszyły produkcję cytokin zapalnych. W modelu myszy z sepsą EV z gp130 obniżyły poziomy IL-6 w narządach, stłumiły dalsze sygnalizowanie i znacznie poprawiły przeżywalność, przewyższając podania rozpuszczalnego białka gp130. Pęcherzyki specyficznie wiązały kompleksy IL-6–receptor, ograniczając prozapalną ścieżkę przy jednoczesnym zachowaniu klasycznego sygnalizowania IL-6, ważnego dla normalnych reakcji.
Ochrona zużytych stawów poprzez ukierunkowanie na chrząstkę
Aby przeciwdziałać chorobie zwyrodnieniowej stawów, zespół połączył strategie ukierunkowania i przynęty. Dodali peptyd kierujący do chrząstki do EV z gp130 opartych na EN144, generując cząstki, które zarówno trafiają do chondrocytów, jak i neutralizują trans-sygnałowanie IL-6. W hodowlach chondrocytów narażonych na bodźce zapalne te ukierunkowane przynętowe EV poprawiły przeżywalność i migrację komórek przy jednoczesnym zmniejszeniu ich śmierci. U szczurów z chirurgicznie wywołaną chorobą zwyrodnieniową stawów powtarzane iniekcje do jamy stawowej prowadziły do silnego zatrzymania EV w chrząstce, mniejszego rozpadu powierzchni stawu oraz zdrowszej chrząstki w badaniu mikroskopowym. Markery uszkodzenia tkanki spadły, podczas gdy białka strukturalne utrzymujące chrząstkę wzrosły, a skład komórek układu odpornościowego w wyściółce stawowej przesunął się w kierunku bardziej gojącego, mniej zapalnego profilu.
Od maleńkiego rusztowania do szerokiej platformy terapeutycznej
Wyodrębniając EN144 jako minimalne, wysokowydajne rusztowanie, ta praca przekształca naturalnie występujące pęcherzyki zewnątrzkomórkowe w elastyczną platformę terapeutyczną. Ten sam mały kotwiczący fragment może eksponować znaczniki ukierunkowujące i receptory-przynęty na powierzchni pęcherzyka, jednocześnie ładując materiał genetyczny lub białkowy wewnątrz, przy profilu bezpieczeństwa podobnym do niemodyfikowanych EV. W modelach zwierzęcych „przynętowe EV” oparte na EN144 skutecznie ujarzmiły zagrażające życiu zapalenie i chroniły uszkodzone stawy. Dla laika implikacją jest to, że możemy zmierzać w kierunku leków zbudowanych z naturalnych pakietów dostarczających organizmu, precyzyjnie zaprojektowanych, by nieść odpowiednie narzędzia we właściwe miejsce i tłumić szkodliwe sygnały, nie wyłączając przy tym normalnej obrony organizmu.
Cytowanie: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Słowa kluczowe: pęcherzyki zewnątrzkomórkowe, dostarczanie leków, zapalanie, sepsa, choroba zwyrodnieniowa stawów