Clear Sky Science · he
הנדסת וסקולות חוץ-תאיות באמצעות חלבון שלד קטן
שליחים זעירים עם הבטחה רפואית גדולה
תרופות רבות של היום מתקשות להגיע בדיוק לתאים הנכונים מבלי לגרום לתופעות לוואי באזורים אחרים. המחקר הזה בוחן כיצד להפוך את "חבילי השליח" הננומטריים של הגוף, המכונים וגסקולות חוץ-תאיות, לכלי נשיאה חכמים יותר לתרופות וחלבונים אנטי‑דלקתיים. על ידי גילוי וטיוב חלבון שלד קטן שמסייע לארוז מטען לתוך הווסקולות הללו, החוקרים בנו חלקיקים מתוכננים שמרגיעים דלקת מסוכנת בספסיס ומגנים על מפרקים שחוקים באוסטאוארתריטיס. 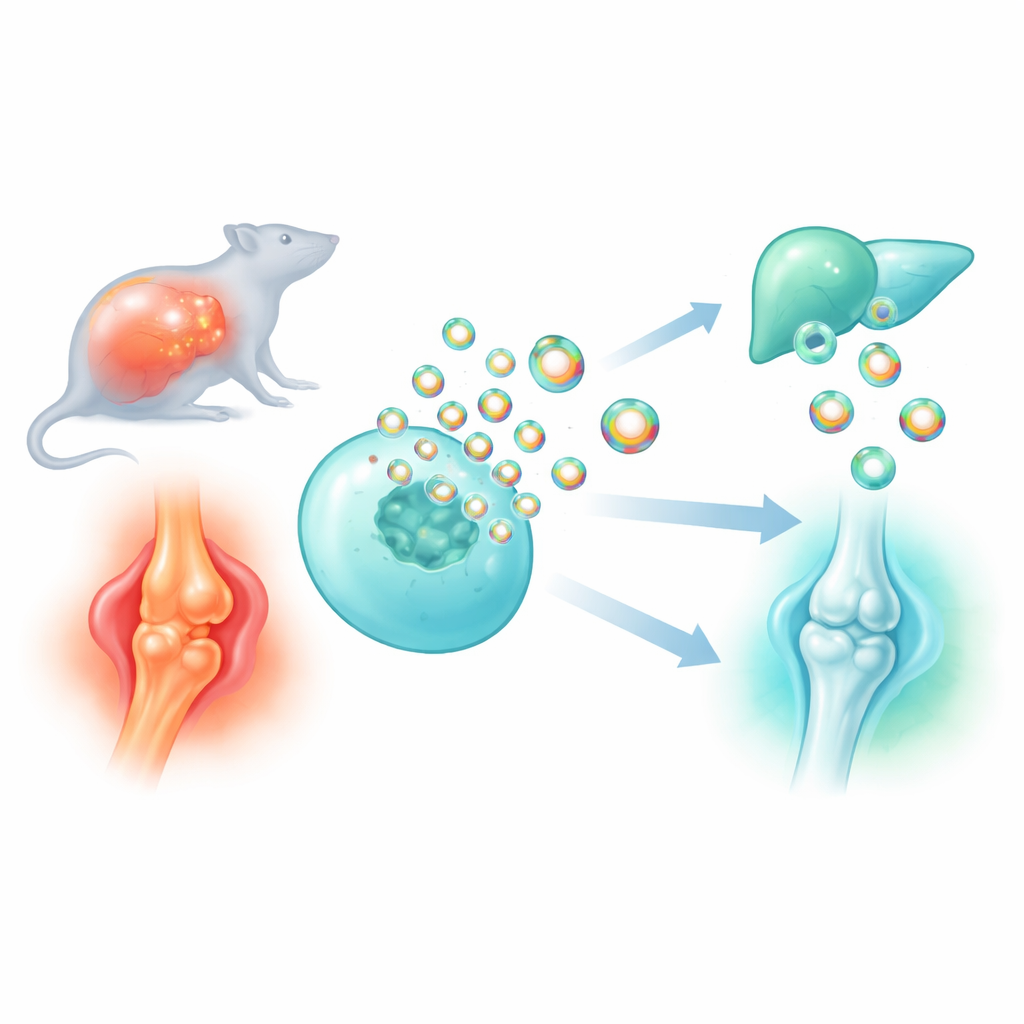
חבילות טבעיות שהופכו לנושאות ממוקדות
תאים משילים באופן קבוע בועיות ממברנה זעירות הידועות כווסקולות חוץ-תאיות (EVs). חבילות אלה מעבירות באופן טבעי חלבונים וחומר גנטי בין תאים ויכולות לחדור מחסומים ביולוגיים שלעתים חוסמים חלקיקים סינתטיים. זה עושה את ה‑EVs לאטרקטיביים כרכבי הובלה ביולוגיים לטיפול, אך קיימת בעיה: הטענת כמות מספקת של מטען שימושי בתוכן, או הצגת המולקולות הנכונות על פני השטח, הייתה קשה. חלבוני "שלד" קיימים שמנחים מטען ל‑EVs עלולים להיות מגושמים, מורכבים או מופיעים באופן לא אחיד, מה שמגביל כמה חומר טיפולי ניתן לארוז בכל וגסקולה ומעורר חששות בטיחותיים.
למצוא שלד קטן אך עוצמתי
כדי לפתור זאת, הצוות ערך סקר שיטתי של חלבונים הנראים על EVs המיוצרים על‑ידי קו תאים אנושי בשימוש שכיח. באמצעות שלוש שיטות טיהור עצמאיות ומסטרומטריה של מסה, הם קיבצו 15 מועמדים וחיברו כל אחד לדיו פלורסנטי למדידת היעילות שבה ממוינים לווסקולות. אחד בלט: ENPP1, שטען מטען ביעילות גבוהה יותר מאשר שלדי מוכרים כמו PTGFRN ו‑Lamp2b. המדענים קיצצו לאחר מכן את ENPP1 למספר גרסאות קצרות וגילו את EN144, שבריר של 144 חומצות אמינו בלבד, שאיפסן פי שלוש יותר חלבון מדווח בתוך EVs מאשר ENPP1 המלא, תוך שמירה על גודל והמבנה של הווסקולות.
כלי בטוחים וגמישים למטען גנטי וחלבוני
מכיוון שכל מערכת הובלה חייבת להיות בטוחה, החוקרים בדקו EVs מקושטים ב‑EN144 למספר סוגי תאים ולחולדות. הווסקולות הראו סמני EV אופייניים, נשארו בטווחי גודל רגילים וגרמו למעט או ללא רעילות, גם במנות גבוהות או בחזרות מנות. לאחר הזרקה בעכברים, EN144‑EVs הצטברו בעיקר בכבד ובטחול, בדומה ל‑EVs סטנדרטיים, ללא פגיעה באיברים או הפרת פרמטרים בדם. הצוות הראה גם ש‑EN144 יכול לשמש כעמדה עגינה מולקולרית למגוון מטענים. כאשר קישרו אותו לפפטיד המכוון לסחוס, יצרו EVs שנבלעו ביעילות על ידי כונדרוציטים, התאים השומרים על רקמת הסחוס. באמצעות מוטיבים קשירת RNA העשירו mRNA טיפולי בתוך הווסקולות ואישרו שהתאים המקבלים תרגמו את ה‑mRNA לחלבון. הם גם טעינו קומפלקס עריכת גנים CRISPR–Cas9 דרך זוגות חלבון‑חלבון מהנדסים והראו שעורכי גנים מסופקים ב‑EVs יכולים להפעיל גן מדווח שקט בתאים מטרה.
ווסקולות דמויי פתיון שסופחות אותות מזיקים
מחלות דלקתיות כמו ספסיס ואוסטאוארתריטיס מונעות בחלקן על‑ידי הציטוקין אינטרליאוקין‑6 (IL‑6), שיכול לפעול במנגנון "טרנס‑סיגנלינג" מזיק כשהוא יוצר קומפלקסים עם קולטן מסיס. כדי לחסום באופן סלקטיבי את המסלול המזיק הזה מבלי להשבית תפקידים מועילים של IL‑6, המחברים חיברו את EN144 ל‑gp130, מעביר אות מרכזי של IL‑6, ויצרו EVs שמציגים gp130 כפתיון על פני השטח. בתרביות תאים, הווסקולות‑פתיון הקטינו בצורה ניכרת את ייצור הציטוקינים הדלקתיים. במודל עכבר של ספסיס, EVs עם gp130 הקטינו רמות IL‑6 באיברים, ריככו איתות מטה ושיפרו באופן ניכר את ההישרדות, כשהם עולים על מינונים של חלבון gp130 מסיס. הווסקולות נקשרו באופן ספציפי לקומפלקסים של IL‑6‑קולטן, עיכבו את המסלול הפרו‑דלקתי והשאירו את איתות IL‑6 הקלאסי, החשוב לתגובות נורמליות, ברובו ללא פגיעה.
הגנה על מפרקים שחוקים באמצעות כיוון לסחוס
כדי לטפל באוסטאוארתריטיס, הצוות שילב אסטרטגיות מיקוד ופיתיון. הם הוסיפו את הפפטיד המכוון לסחוס ל‑EN144 EVs הנושאים gp130, ויצרו חלקיקים שגם נמשכים לכונדרוציטים וגם מנטרלים את ה‑IL‑6 טרנס‑סיגנלינג. בכונדרוציטים בתרבית שנחשפו לאיתותים דלקתיים, EVs הפתיון הממוקדים האלה שיפרו את השרידות והתנועה של התאים תוך שהם מצמצמים את המוות התאי. בחולדות עם אוסטאוארתריטיס שנגרמה ניתוחית, הזרקות חוזרות לחלל המפרק הביאו לשימור חזק של הווסקולות בסחוס, לפירוק משטח המפרק מופחת ולסחוס בריא יותר תחת המיקרוסקופ. סמנים של נזק רקמתי ירדו, בעוד חלבוני מבנה השומרים על הסחוס עלו, והאיזון של תאי חיסון ברקמת הרירית של המפרק התוזמן לכיוון מרפא ופחות דלקתי.
מ‑שלד זעיר לפלטפורמת טיפולית רחבה
על‑ידי חיתוך EN144 כשלד מינימלי וביצועי, עבודה זו הופכת ווסקולות חוץ‑תאיות טבעיות לפלטפורמת טיפולית גמישה. העוגן הקטן הזה יכול להציג תגיות מטרה וקולטנים‑פתיון על פני הווסקולה ובו‑זמנית לטעון מטען גנטי או חלבוני בפנים, הכל עם פרופיל בטיחות בדומה לווסקולות לא‑משונעות. במודלים חייים, "ווסקולות פתיון" מבוססות EN144 ריסנו בהצלחה דלקת מסכנת חיים והגנו על מפרקים פגועים. עבור הקורא הרחב, המשמעות היא שאנו מתקרבים לתרופות המבוססות על חבילות ההובלה של הגוף עצמו, מהונדסות בדיוק כדי לשאת את הכלים הנכונים למקום הנכון ולרגיע אותות מזיקים מבלי להשתיק את ההגנות הטבעיות של הגוף.
ציטוט: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
מילות מפתח: ווסקולות חוץ-תאיות, הובלת תרופות, דלקת, ספסיס, אוסטאוארתריטיס