Clear Sky Science · de
Extrazelluläre Vesikel-Engineering mit einem kleinen Gerüstprotein
Winzige Kuriere mit großem medizinischem Potenzial
Viele der heute verwendeten Medikamente haben Schwierigkeiten, genau die richtigen Zellen zu erreichen, ohne anderswo Nebenwirkungen zu verursachen. Diese Studie untersucht, wie sich die körpereigenen nanoskaligen „Päckchen“, sogenannte extrazelluläre Vesikel, in intelligentere Transportvehikel für Wirkstoffe und entzündungshemmende Proteine verwandeln lassen. Durch die Entdeckung und Verfeinerung eines sehr kleinen Gerüstproteins, das beim Verpacken von Fracht in diese Vesikel hilft, bauen die Forschenden maßgeschneiderte Partikel, die gefährliche Entzündungen bei Sepsis dämpfen und verschlissene Gelenke bei Osteoarthritis schützen. 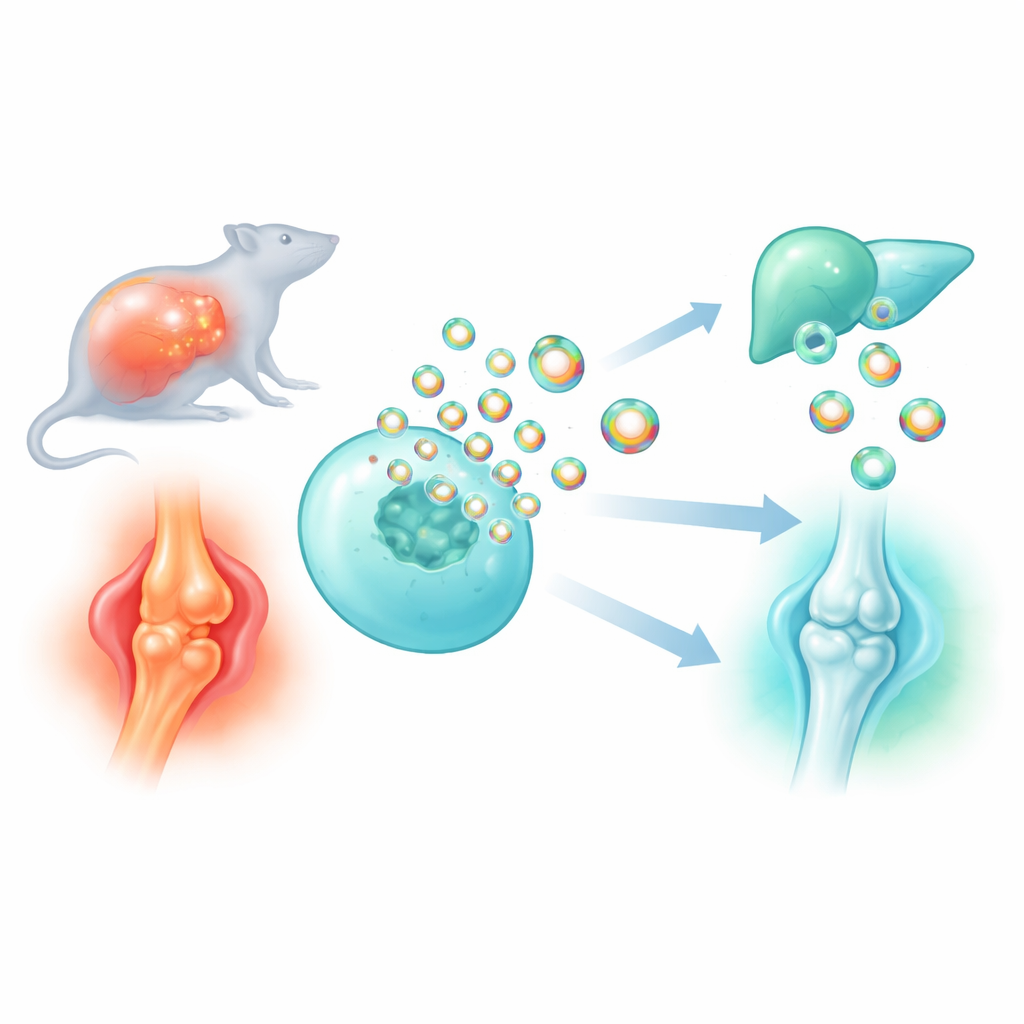
Natürliche Pakete als zielgerichtete Träger
Zellen stoßen ständig winzige Membranbläschen aus, die als extrazelluläre Vesikel (EVs) bekannt sind. Diese Päckchen transportieren natürlich Proteine und genetisches Material zwischen Zellen und können biologische Barrieren passieren, die synthetische Nanopartikel oft blockieren. Das macht EVs als lebende Transporter für Therapien attraktiv, doch es gibt einen Haken: Es ist schwierig, genügend hilfreiche Fracht in sie hineinzuladen oder die richtigen Moleküle auf ihrer Oberfläche darzustellen. Bestehende „Gerüst“-Proteine, die Fracht in EVs lenken, können sperrig, komplex oder ungleichmäßig vorhanden sein, was die Menge therapeutischen Materials pro Vesikel begrenzt und Sicherheitsbedenken aufwirft.
Ein kleines, aber kraftvolles Gerüst finden
Um dieses Problem zu lösen, untersuchte das Team systematisch Proteine, die auf EVs einer häufig verwendeten humanen Zelllinie vorkommen. Mit drei unabhängigen Aufreinigungsmethoden und Massenspektrometrie kürzten sie die Kandidatenliste auf 15 ein und fusionierten jedes Protein mit einem fluoreszenten Reporter, um zu messen, wie effizient es in Vesikel sortiert wurde. Ein Protein stach hervor: ENPP1, das Fracht wirksamer lud als weitverbreitete Gerüste wie PTGFRN und Lamp2b. Die Forschenden schnitten ENPP1 dann in mehrere kürzere Versionen und entdeckten EN144, ein Fragment von nur 144 Aminosäuren, das dreimal mehr Reporterprotein in EVs verpackte als das vollstängige ENPP1, während Größe und Struktur der Vesikel erhalten blieben. 
Sichere, vielseitige Vehikel für genetische und proteinbasierte Fracht
Da jedes Liefersystem sicher sein muss, testeten die Forschenden EN144-dekorierte EVs in mehreren Zelltypen und in Mäusen. Die Vesikel zeigten typische EV-Marker, blieben innerhalb normaler Größenspannen und verursachten kaum oder keine Toxizität, selbst bei hohen oder wiederholten Dosen. Nach Injektion in Mäuse akkumulierten EN144-EVs überwiegend in Leber und Milz, ähnlich wie Standard-EVs, ohne Organschäden oder Störungen der Blutchemie. Das Team zeigte außerdem, dass EN144 als molekulare Andockstation für viele Frachtarten genutzt werden kann. Durch die Kopplung an ein knorpel-spezifisches Peptid entstanden EVs, die effizient von Chondrozyten, den Zellen, die Gelenkknorpel erhalten, aufgenommen wurden. Mit RNA-bindenden Motiven reicherte man therapeutische mRNA in EVs an und bestätigte, dass Empfängerzellen diese mRNA in Protein übersetzten. Sie luden auch CRISPR–Cas9-Geneditierkomplexe über konstruierte Protein‑Protein‑Paare in die Vesikel und zeigten, dass EV-vermittelte Editoren ein stilles Reportergen in Zielzellen aktivieren konnten.
Fang-Vesikel, die schädliche Signale aufsaugen
Entzündliche Erkrankungen wie Sepsis und Osteoarthritis werden teilweise durch das Zytokin Interleukin-6 (IL-6) vorangetrieben, das in einer schädlichen „Trans-Signal“-Form wirken kann, wenn es Komplexe mit einem löslichen Rezeptor bildet. Um diesen schädlichen Weg gezielt zu blockieren, ohne IL-6s nützliche Funktionen abzuschalten, fusionierten die Autor:innen EN144 mit gp130, einem Schlüsseltransduktor der IL-6-Signalgebung, und schufen EVs, die gp130 als Köder auf ihrer Oberfläche darstellen. In Zellkulturen reduzierten diese Köder-Vesikel die Produktion entzündlicher Zytokine deutlich. In einem Mausmodell der Sepsis senkten gp130-tragende EVs die IL-6-Spiegel in Organen, dämpften nachgeschaltete Signalwege und verbesserten das Überleben stark — und zwar besser als Dosen des löslichen gp130-Proteins. Die Vesikel banden spezifisch IL-6–Rezeptor-Komplexe und bremsten den proinflammatorischen Pfad, während die klassische IL-6-Signalgebung, wichtig für normale Reaktionen, weitgehend intakt blieb.
Geschädigte Gelenke schützen durch gezielte Knorpelansprache
Um Osteoarthritis anzugehen, kombinierten die Forschenden Targeting- und Köder-Strategien. Sie fügten dem gp130-tragenden EN144-EVs das knorpel-ansprechende Peptid hinzu und erzeugten Partikel, die sowohl Chondrozyten ansteuern als auch IL-6-Trans-Signalgebung neutralisieren. In kultivierten Chondrozyten, die entzündlichen Reizen ausgesetzt waren, förderten diese zielgerichteten Köder-EVs Überleben und Migration der Zellen und reduzierten zugleich Zelltod. In Ratten mit chirurgisch induzierter Osteoarthritis führten wiederholte Injektionen in die Gelenkhöhle zu starker Retention der EVs im Knorpel, weniger Abbau der Gelenkoberfläche und gesünderem Knorpel im Mikroskop. Marker für Gewebeschädigung sanken, während Strukturproteine, die den Knorpel erhalten, zunahmen, und das Gleichgewicht der Immunzellen in der Gelenkschleimhaut verschob sich zu einem heilungsfördernden, weniger entzündlichen Profil.
Vom winzigen Gerüst zur breiten therapeutischen Plattform
Durch die Herausarbeitung von EN144 als minimales, leistungsstarkes Gerüst verwandelt diese Arbeit natürlich vorkommende extrazelluläre Vesikel in eine flexible therapeutische Plattform. Dieselbe kleine Verankerung kann Zielanhänge und Köderrezeptoren auf der Vesikeloberfläche darstellen und gleichzeitig genetische oder proteinbasierte Fracht im Inneren laden — und das mit einem Sicherheitsprofil, das dem unmodifizierter Vesikel ähnelt. In Tiermodellen zähmten EN144-basierte „Köder-EVs“ lebensbedrohliche Entzündungen erfolgreich und schützten geschädigte Gelenke. Für Laien bedeutet das: Wir bewegen uns möglicherweise auf Medikamente zu, die aus körpereigenen Transportpäckchen gebaut sind, präzise so konstruiert, dass sie die richtigen Werkzeuge an den richtigen Ort bringen und schädliche Signale dämpfen, ohne die normalen Abwehrfunktionen des Körpers zu unterdrücken.
Zitation: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Schlüsselwörter: extrazelluläre Vesikel, Arzneimitteltransport, Entzündung, Sepsis, Osteoarthritis