Clear Sky Science · ar
هندسة الحويصلات خارج الخلوية باستخدام بروتين هيكلي صغير
سعاة صغار بوعد طبي كبير
تواجه العديد من الأدوية الحالية صعوبة في الوصول إلى الخلايا المستهدفة بدقة من دون التسبب في آثار جانبية في أماكن أخرى. تستكشف هذه الدراسة كيفية تحويل «حزم النقل» النانوية الطبيعية في الجسم، المسماة الحويصلات خارج الخلوية، إلى ناقلات أكثر ذكاءً للأدوية والبروتينات المضادة للالتهاب. من خلال اكتشاف وتعديل بروتين هيكلي صغير يساعد على تعبئة الحمولة داخل هذه الحويصلات، بنى الباحثون جسيمات مصممة تهدئ الالتهاب الخطير في الإنتان وتحمي المفاصل المتآكلة في التهاب المفاصل التنكسي. 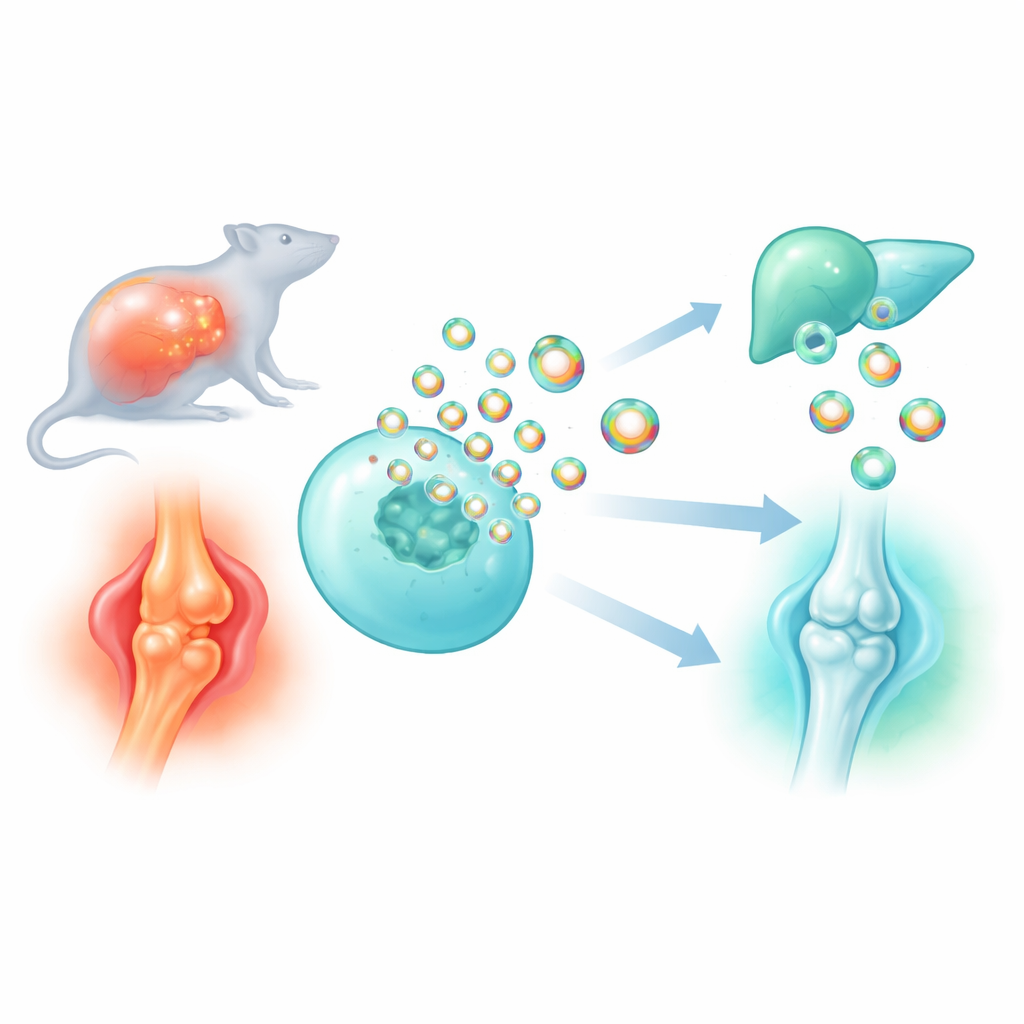
حزم طبيعية تتحول إلى ناقلات موجهة
تتخلص الخلايا باستمرار من فقاعات غشائية صغيرة تعرف باسم الحويصلات خارج الخلوية (EVs). تحمل هذه الحزم طبيعيًا بروتينات ومادة وراثية بين الخلايا ويمكنها اجتياز الحواجز البيولوجية التي غالبًا ما تعيق الجسيمات النانوية الاصطناعية. وهذا يجعل الحويصلات خارج الخلوية جذابة كسيارات نقل حية للعلاج، لكن هناك عقبة: صعب تحميل كمية كافية من الحمولة المفيدة بداخلها، أو عرض الجزيئات المناسبة على سطحها. البروتينات «الهيكلية» الحالية التي توجه الحمولة إلى الحويصلات قد تكون ضخمة أو معقدة أو متواجدة بشكل غير متساوٍ، مما يحد من كمية المادة العلاجية التي يمكن تعبئتها في كل حويصلة ويثير مخاوف تتعلق بالسلامة.
البحث عن هيكل صغير لكنه قوي
لحل هذه المشكلة، استعرض الفريق منهجيًا البروتينات التي تظهر على الحويصلات خارج الخلوية المنتجة من سلالة خلوية بشرية مستخدمة على نطاق واسع. باستخدام ثلاث طرق تنقية مستقلة والتحليل الطيفي الكتلي، اختصروا قائمة المرشحين إلى 15 بروتينًا ووصلوا كل واحد بمؤشر فلوري لقياس كفاءة فرزه إلى الحويصلات. برز واحد منها: ENPP1، الذي حمّل الحمولة بفعالية أكبر من الهياكل الشائعة مثل PTGFRN وLamp2b. ثم قام العلماء بتقطيع ENPP1 إلى نسخ أقصر واكتشفوا EN144، قطعة بطول 144 حمضًا أمينيًا فقط، وأنها حزمت ثلاثة أضعاف بروتين المؤشر داخل الحويصلات مقارنةً بالبروتين الكامل، مع الحفاظ على حجم الحويصلة وبنيتها.
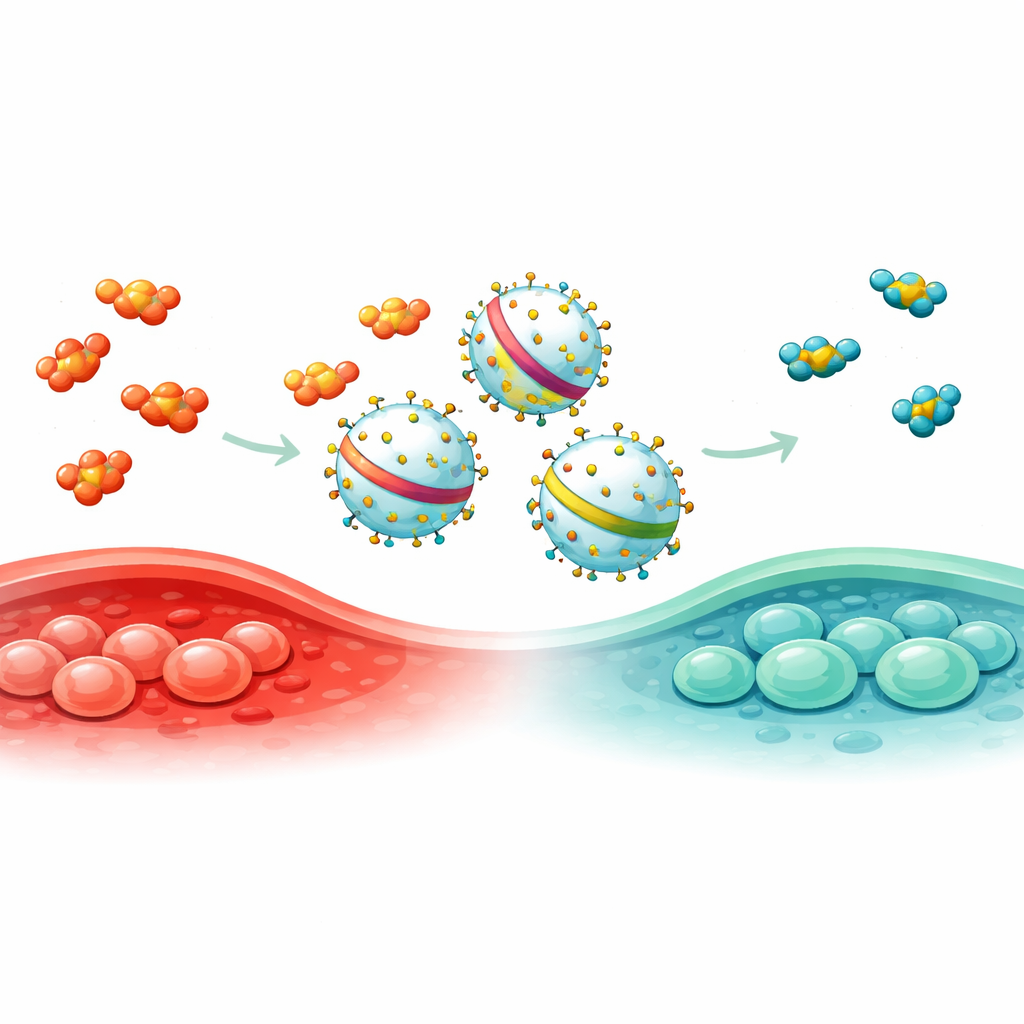
ناقلات آمنة ومتعددة الاستخدامات للحمولات الجينية والبروتينية
نظرًا لأن أي نظام توصيل يجب أن يكون آمنًا، اختبر الباحثون الحويصلات المزينة بـEN144 في عدة أنواع خلوية وفي الفئران. عرضت الحويصلات علامات نمطية للحويصلات خارج الخلوية، وبقيت ضمن نطاقات الحجم الطبيعية، ولم تسبب سمية تذكر حتى بجرعات عالية أو متكررة. بعد الحقن في الفئران، تراكمت حويصلات EN144 بشكل رئيسي في الكبد والطحال، على نحو مماثل للحويصلات القياسية، دون إلحاق ضرر بالأعضاء أو إحداث اضطراب في كيمياء الدم. ثم أظهر الفريق أن EN144 يمكن استخدامه كمحطة ارتكاز جزيئية لأنواع متعددة من الحمولة. بربطه بببتيد يتوجه إلى الغضروف، صنعوا حويصلات تمتصها الخلايا الغضروفية بفعالية. باستخدام أنماط ربط للـRNA، قاموا بتخصيب mRNA علاجي داخل الحويصلات وتأكدوا من ترجمة الخلايا المستقبلة لذلك الـmRNA إلى بروتين. كما حملوا مجمعات تحرير الجينات CRISPR–Cas9 عبر أزواج بروتينية مهندسة وأظهروا أن المحررات الموصولة بالحويصلات يمكن أن تنشط جين مؤشر صامت في الخلايا المستهدفة.
حويصلات طُعم تمتص الإشارات الضارة
تُقود الأمراض الالتهابية مثل الإنتان والتهاب المفاصل التنكسي جزئيًا السيتوكين إنترلوكين-6 (IL-6)، الذي يمكن أن يعمل في وضع «الإشارة المتقاطعة» الضار عندما يشكل مركبات مع مستقبل قابل للذوبان. لوقف هذا المسار الضار انتقائيًا دون تعطيل أدوار IL-6 المفيدة، أضاف المؤلفون EN144 إلى gp130، وهو ناقل رئيسي لإشارات IL-6، فأنشأوا حويصلات تعرض gp130 كطُعم على سطحها. في الثقافة الخلوية، قللت هذه الحويصلات الطُعمية بشدة إنتاج السيتوكينات الالتهابية. في نموذج فأري للإنتان، خفضت الحويصلات الحاملة لـgp130 مستويات IL-6 في الأعضاء، وكبتت الإشارات اللاحقة، وحسنت البقاء بشكل كبير، متفوقة على جرعات من بروتين gp130 القابل للذوبان. ارتبطت الحويصلات بشكل انتقائي بمركبات IL-6–المستقبل، فكبَحت المسار المؤيد للالتهاب بينما تركت إشارة IL-6 الكلاسيكية، المهمة للاستجابات الطبيعية، سليمة إلى حد كبير.
حماية المفاصل المتآكلة بالاستهداف للغضروف
لمعالجة التهاب المفاصل التنكسي، جمع الفريق استراتيجيات الاستهداف والطُعم. أضافوا الببتيد المتجه إلى الغضروف إلى حويصلات EN144 الحاملة لـgp130، فأنشأوا جسيمات تتوجه إلى الخلايا الغضروفية وتحيد إشارات IL-6 المتقاطعة. في الخلايا الغضروفية المزروعة المعرضة لمحفزات التهابية، عززت هذه الحويصلات الطُعمية المستهدفة بقاء الخلايا وحركتها بينما قللت من موت الخلايا. في جرذان أُحدثت لها إصابات جراحية تسببت في التهاب مفاصل تنكسي، أدت الحقن المتكررة داخل تجويف المفصل إلى بقاء قوي للحويصلات في الغضروف، وتقليل تفكك سطح المفصل، وغضروف أنسب تحت المجهر. انخفضت مؤشرات تلف الأنسجة، بينما زادت البروتينات التركيبية التي تحافظ على الغضروف، وتحول توازن الخلايا المناعية في بطانة المفصل نحو حالة أكثر شفاءً وأقل التهابية.
من هيكل صغير إلى منصّة علاجية واسعة
من خلال تقليم EN144 ليصبح هيكلًا صغيرًا عالي الأداء، يحول هذا العمل الحويصلات خارج الخلوية الطبيعية إلى منصة علاجية مرنة. يمكن للمرساة الصغيرة نفسها عرض علامات استهداف ومستقبلات طُعمية على سطح الحويصلة أثناء تحميل حمولات جينية أو بروتينية بالداخل، كل ذلك مع ملف سلامة مشابه للحويصلات غير المعدلة. في نماذج حيوانية، نجحت «الحويصلات الطُعمية» المعتمدة على EN144 في تهدئة التهاب مهدد للحياة وحماية المفاصل التالفة. للقراء غير المتخصصين، الاثار المحتملة هى أننا قد نكون نتقدم نحو أدوية مبنية من حزم النقل الطبيعية في الجسم، مُهندَسة بدقة لحمل الأدوات المناسبة إلى المكان المناسب، ولقمع الإشارات الضارة دون إسكات دفاعات الجسم الطبيعية.
الاستشهاد: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
الكلمات المفتاحية: الحويصلات خارج الخلوية, توصيل الأدوية, الالتهاب, الإنتان, التهاب المفاصل التنكسي