Clear Sky Science · sv
Extracellulära vesiklar konstruerade med ett litet scaffold-protein
Små budbärare med stor medicinsk potential
Många av dagens läkemedel har svårt att nå exakt rätt celler utan att orsaka biverkningar på andra ställen. Denna studie undersöker hur kroppens egna nanoskaliga ”budkappar”, kallade extracellulära vesiklar, kan göras till smartare leveransfordon för läkemedel och antiinflammatoriska proteiner. Genom att upptäcka och finslipa ett mycket litet scaffold-protein som hjälper till att packa last i dessa vesiklar bygger forskarna skräddarsydda partiklar som dämpar farlig inflammation vid sepsis och skyddar slitna leder vid artros. 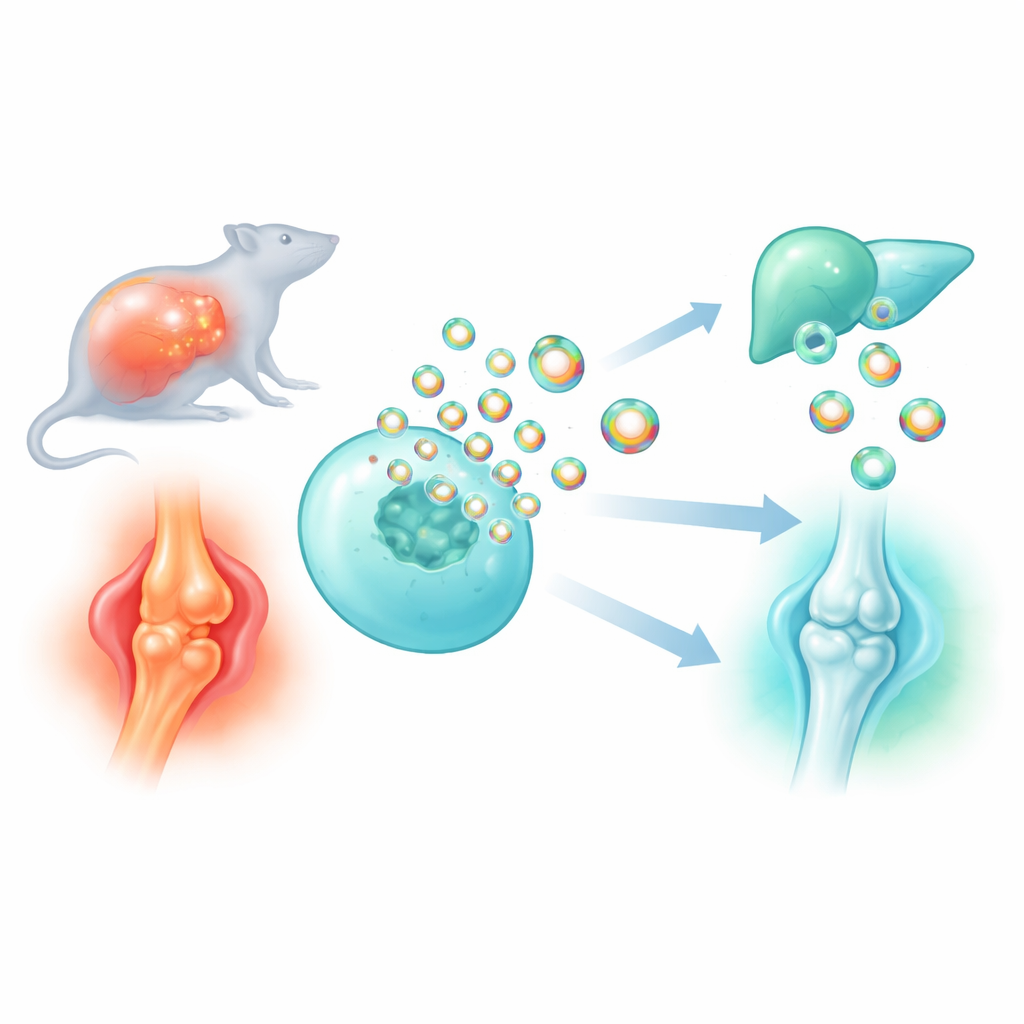
Naturens paket blir målsökande bärare
Celler avger ständigt små membranblåsor som kallas extracellulära vesiklar (EV). Dessa paket transporterar naturligt proteiner och genetiskt material mellan celler och kan passera biologiska barriärer som ofta stoppar syntetiska nanopartiklar. Det gör EV till attraktiva levande leveransfordon för terapi, men det finns en utmaning: att ladda tillräckligt med användbar last inuti dem, eller att visa rätt molekyler på deras yta, har varit svårt. Befintliga ”scaffold”-proteiner som riktar last till EV kan vara otympliga, komplexa eller ojämnt förekommande, vilket begränsar hur mycket terapeutiskt material som kan packas i varje vesikel och väcker säkerhetsfrågor.
Att hitta ett litet men kraftfullt scaffold
För att lösa detta genomsökte teamet systematiskt proteiner som finns på EV från en vanligt använd mänsklig cellinje. Med tre oberoende reningsmetoder och masspektrometri kortlistade de 15 kandidater och fäste var och en vid en fluorescerande markör för att mäta hur effektivt de sorterades in i vesiklarna. En stack ut: ENPP1, som laddade last mer effektivt än ofta använda scaffolds som PTGFRN och Lamp2b. Forskarna trimmade sedan ner ENPP1 till flera kortare versioner och upptäckte EN144, ett fragment på bara 144 aminosyror, som packade tre gånger mer rapporterande protein i EV än fullängds-ENPP1, samtidigt som vesiklarnas storlek och struktur bibehölls. 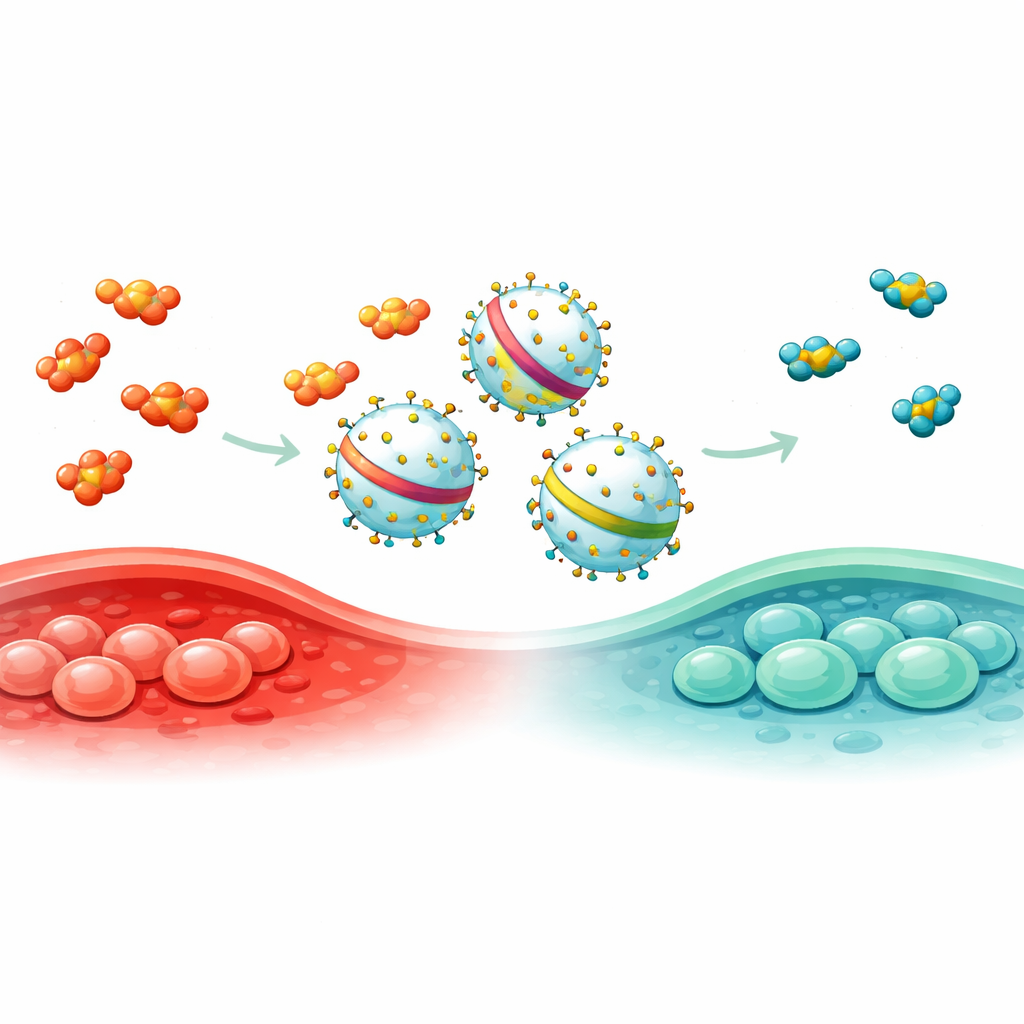
Säkra, mångsidiga fordon för genetisk och proteinkargo
Ett leveranssystem måste vara säkert, så forskarna testade EN144-dekorerade EV i flera celltyper och hos möss. Vesiklarna visade typiska EV-markörer, höll sig inom normala storleksintervall och gav liten till ingen toxicitet, även vid höga eller upprepade doser. Efter injektion i möss ackumulerades EN144-EV främst i lever och mjälte, likt standard-EV, utan att skada organ eller rubba blodkemin. Teamet visade också att EN144 kan fungera som en molekylär dokningsstation för många typer av last. Genom att koppla det till en broskorts‑homerande peptid skapade de EV som togs upp effektivt av kondrocyter, cellerna som upprätthåller ledbrosk. Med RNA-bindande motiv berikade de terapeutisk mRNA i EV och bekräftade att mottagarceller översatte detta mRNA till protein. De lastade också CRISPR–Cas9-genredigeringskomplex via konstruerade protein–protein‑par och visade att EV‑levererade redigerare kunde aktivera en tyst rapportörgen i målceller.
Lock‑vesiklar som fångar skadliga signaler
Inflammatoriska sjukdomar som sepsis och artros drivs delvis av cytokinern interleukin‑6 (IL‑6), som kan verka i ett skadligt ”trans‑signalering”-läge när den bildar komplex med en löslig receptor. För att selektivt blockera denna skadliga väg utan att slå ut IL‑6:s fördelaktiga roller, fäste författarna EN144 vid gp130, en nyckeltransduktor för IL‑6‑signalering, och skapade EV som visar gp130 som en lock på ytan. I cellkultur minskade dessa lock‑vesiklar kraftigt produktionen av inflammatoriska cytokiner. I en musemodell av sepsis sänkte gp130‑bärande EV nivåerna av IL‑6 i organen, dämpade nedströms signalering och förbättrade överlevnaden avsevärt, bättre än doser av lösligt gp130‑protein. Vesiklarna band specifikt IL‑6–receptor‑komplex, vilket hejdade den proinflammatoriska vägen samtidigt som klassisk IL‑6‑signalering, viktig för normala svar, till stor del lämnades intakt.
Skydda slitna leder genom riktning mot brosk
För att angripa artros kombinerade teamet riktning och lock‑strategier. De lade till broskhomerande peptiden till gp130‑bärande EN144‑EV och genererade partiklar som både söker upp kondrocyter och neutraliserar IL‑6 trans‑signalering. I odlade kondrocyter exponerade för inflammatoriska signaler ökade dessa riktade lock‑EV cellöverlevnad och rörlighet samtidigt som celldöd minskade. I råttor med kirurgiskt inducerad artros ledde upprepade injektioner i ledhålan till stark kvarhållning av EV i brosket, mindre nedbrytning av ledytan och friskare brosk vid mikroskopisk analys. Markörer för vävnadsskada sjönk, medan strukturella proteiner som upprätthåller brosk ökade, och balansen av immunceller i ledhinnan försköts mot en mer läkande, mindre inflammatorisk profil.
Från litet scaffold till bred terapeutisk plattform
Genom att utforma EN144 som ett minimalt, högpresterande scaffold förvandlar detta arbete naturligt förekommande extracellulära vesiklar till en flexibel terapeutisk plattform. Samma lilla ankare kan visa upp riktningstaggar och lockreceptorer på vesikelns yta samtidigt som genetisk eller proteinkargo lastas inuti, allt med ett säkerhetsprofil liknande omodifierade vesiklar. I djurmodeller lyckades EN144‑baserade ”lock‑EV” tämja livshotande inflammation och skydda skadade leder. För en lekman innebär det att vi kanske är på väg mot läkemedel byggda av kroppens egna leveranspaket, precist konstruerade för att bära rätt verktyg till rätt plats och dämpa skadliga signaler utan att tysta kroppens normala försvar.
Citering: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Nyckelord: extracellulära vesiklar, läkemedelsleverans, inflammation, sepsis, artros