Clear Sky Science · ja
小さな足場タンパク質を用いた細胞外小胞のエンジニアリング
小さな運び手、大きな医療的可能性
現在の多くの薬は、標的となる細胞に正確に到達することが難しく、他の部位で副作用を引き起こすことがあります。本研究は、細胞がもつナノサイズの“運び袋”である細胞外小胞(extracellular vesicles, EV)を、薬剤や抗炎症タンパク質を運ぶより賢い輸送体に変える方法を探ります。貨物を小胞に詰めるのを助ける非常に小さな足場(スキャフォールド)タンパク質を発見・改良することで、研究者たちは敗血症の危険な炎症を鎮め、変形性関節症で損なわれた関節を保護するデザイナー粒子を作り上げました。 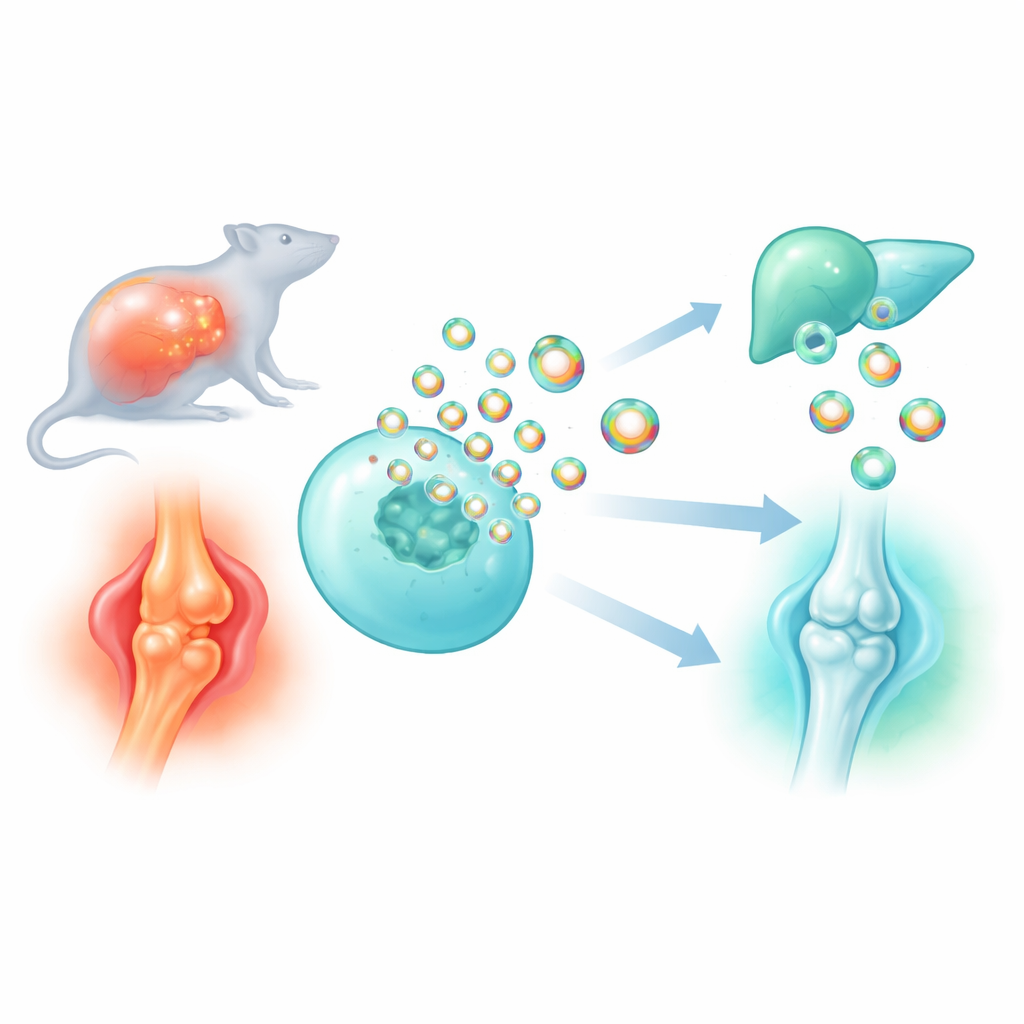
天然のパッケージを標的輸送体へ
細胞は絶えず細胞膜の小さな泡、すなわち細胞外小胞(EV)を放出します。これらの小袋は自然にタンパク質や遺伝物質を細胞間で運び、合成ナノ粒子がよく遮られる生体バリアを通り抜けることができます。そのためEVは生体由来の治療輸送体として有望ですが、問題もあります:十分な有用貨物を内部に積むこと、あるいは表面に適切な分子を表示することが困難でした。貨物をEVに取り込ませる既存の“スキャフォールド”タンパク質は大きく複雑であったり発現が不均一であったりし、各小胞に詰められる治療物質の量を制限し、安全性の懸念を生じさせます。
小さくとも強力な足場の発見
この課題を解決するため、研究チームは一般的に用いられるヒト細胞株が産生するEV上に現れるタンパク質を系統的に調べました。3つの独立した精製法と質量分析を用いて15の候補を絞り、各候補を蛍光レポーターと融合させて小胞への取り込み効率を測定しました。最も優れたものはENPP1で、PTGFRNやLamp2bなど広く用いられるスキャフォールドよりも貨物の取り込みが効率的でした。研究者らはさらにENPP1をいくつかの短い断片に切り詰め、その中でEN144と呼ばれるわずか144アミノ酸長の断片が、全長ENPP1よりも3倍多くのレポータープロテインをEVに詰め込みつつ、小胞のサイズや構造を保つことを発見しました。 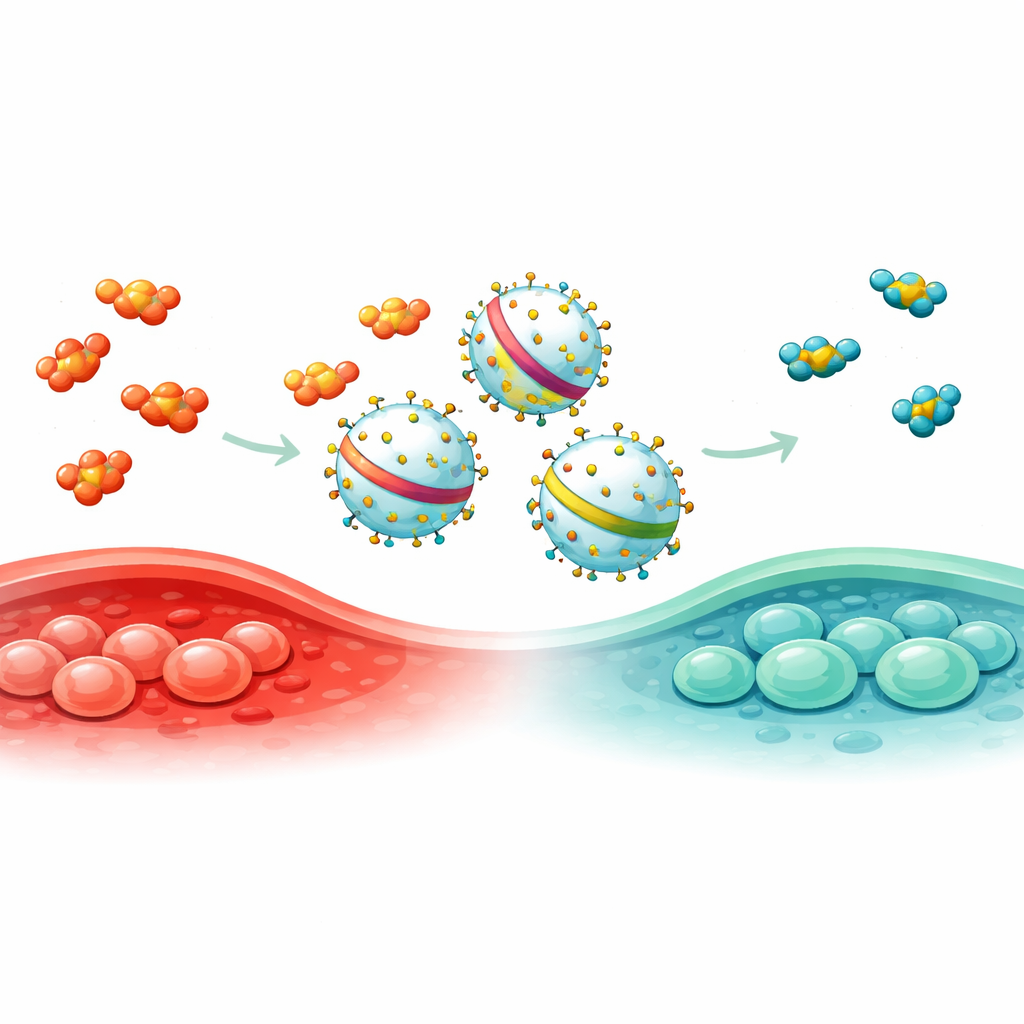
遺伝子とタンパク質を運ぶ安全で多用途な輸送体
どのデリバリーシステムでも安全性が不可欠であるため、研究者たちはEN144を装飾したEVを複数の細胞型とマウスで試験しました。これらの小胞は典型的なEVマーカーを示し、通常のサイズ範囲にあり、高用量や反復投与でもほとんど毒性を示しませんでした。マウスへ注入すると、EN144-EVは標準的なEVと同様に主に肝臓や脾臓に集積し、臓器を損なったり血液化学を乱したりすることはありませんでした。次にEN144が多様な貨物のための分子ドッキングステーションとして機能することを示しました。軟骨へ向かうペプチドを結合することで、軟骨細胞(関節軟骨を維持する細胞)に効率よく取り込まれるEVを作製しました。RNA結合モチーフを使って治療用mRNAをEV内に濃縮し、受容細胞がそのmRNAをタンパク質に翻訳することを確認しました。さらに、遺伝子編集複合体CRISPR–Cas9を設計したタンパク質間相互作用を介して搭載し、EV経由で運ばれた編集酵素が標的細胞でサイレントなリポーター遺伝子を活性化できることを実証しました。
有害なシグナルを吸着するデコイ小胞
敗血症や変形性関節症のような炎症性疾患は、サイトカインであるインターロイキン‑6(IL‑6)によって部分的に駆動されます。IL‑6は可溶性受容体と複合体を形成すると有害な“トランスシグナル”経路で作用することがあります。この有害な経路を選択的に遮断しつつ、IL‑6の有益な役割を維持するために、著者らはEN144をIL‑6の主要なシグナル伝達子であるgp130に融合し、表面にgp130をデコイとして表示するEVを作製しました。培養細胞では、これらのデコイ小胞は炎症性サイトカインの産生を大幅に減らしました。敗血症マウスモデルでは、gp130を持つEVは臓器中のIL‑6レベルを低下させ、下流のシグナル伝達を抑え、生存率を大きく改善し、可溶性gp130タンパク質の投与より優れた効果を示しました。これらの小胞はIL‑6–受容体複合体に特異的に結合し、炎症促進経路を抑える一方で、正常な生体応答に重要な古典的なIL‑6シグナルは概ね維持しました。
軟骨を狙って摩耗した関節を保護
変形性関節症に対処するため、チームは標的化戦略とデコイ戦略を組み合わせました。軟骨ホーミングペプチドをgp130を表示するEN144 EVに付加することで、軟骨細胞へ向かいつつIL‑6トランスシグナルを中和する粒子を作りました。炎症刺激にさらされた培養軟骨細胞では、これらの標的化されたデコイEVが細胞の生存と運動性を高め、細胞死を減少させました。外科的に誘発した変形性関節症ラットでは、関節腔内への繰り返し注射によりEVの軟骨内保持が強くなり、関節表面の分解が少なくなり、顕微鏡下でより健康的な軟骨が観察されました。組織損傷のマーカーは低下し、軟骨を維持する構造タンパク質は増加し、関節膜内の免疫細胞バランスはより修復的で炎症の少ないプロファイルへと変化しました。
小さな足場から広範な治療プラットフォームへ
EN144を最小で高性能なスキャフォールドとして確立することで、この研究は天然の細胞外小胞を柔軟な治療プラットフォームへと変えました。同じ小さなアンカーは、小胞表面に標的タグやデコイ受容体を表示しつつ、内部に遺伝子やタンパク質の貨物を搭載でき、いずれも改変していない小胞と類似した安全性プロファイルを示します。動物モデルでは、EN144ベースの“デコイEV”が生命を脅かす炎症を抑え、損傷した関節を保護しました。一般の読み手にとっての含意は、体内の天然の輸送袋を出発点とし、正しい道具を正しい場所へ正確に運び、有害なシグナルは抑えつつも生体の通常の防御を過度に消さないよう設計された医薬が近づいている可能性がある、ということです。
引用: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
キーワード: 細胞外小胞, ドラッグデリバリー, 炎症, 敗血症, 変形性関節症