Clear Sky Science · nl
Extracellulaire vesikel-engineering met een klein scaffold-eiwit
Kleine koeriers met grote medische belofte
Veel hedendaagse geneesmiddelen hebben moeite om precies de juiste cellen te bereiken zonder elders bijwerkingen te veroorzaken. Deze studie onderzoekt hoe de eigen nanogrote "koerierpakketjes" van het lichaam, extracellulaire vesikels genoemd, kunnen worden omgevormd tot slimmere vervoerders voor medicijnen en ontstekingsremmende eiwitten. Door een zeer klein scaffold-eiwit te ontdekken en te verfijnen dat helpt cargo in deze vesikels te laden, bouwen de onderzoekers designpartikels die gevaarlijke ontsteking bij sepsis dempen en versleten gewrichten bij artrose beschermen. 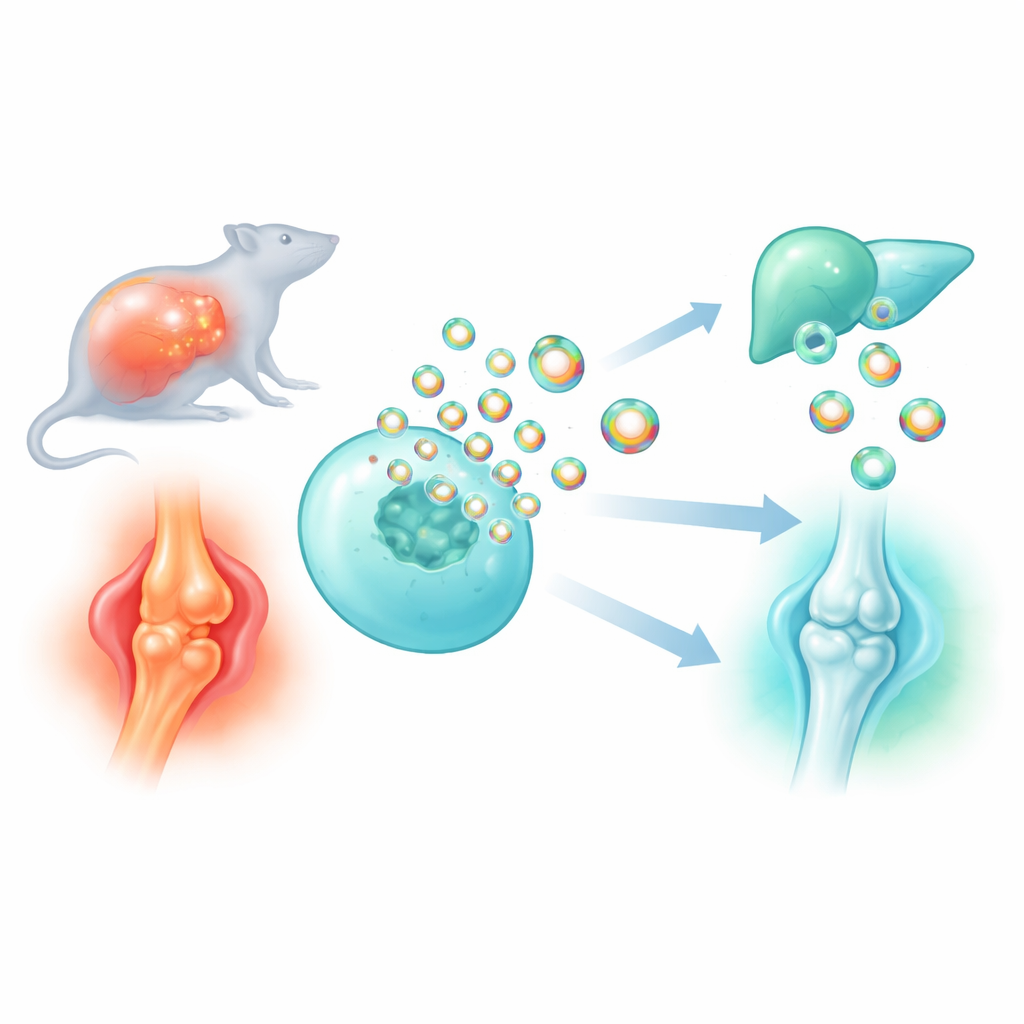
Natuurlijke pakketjes getransformeerd tot gerichte dragers
Cellen stoten voortdurend kleine membraanblaasjes af die bekendstaan als extracellulaire vesikels (EVs). Deze pakketjes dragen van nature eiwitten en genetisch materiaal tussen cellen en kunnen biologische barrières passeren die synthetische nanodeeltjes vaak blokkeren. Dat maakt EVs aantrekkelijk als levende bezorgtrucks voor therapie, maar er is een probleem: het is moeilijk om voldoende bruikbare lading in ze te laden of de juiste moleculen op hun oppervlak te tonen. Bestaande "scaffold"-eiwitten die cargo naar EVs sturen kunnen omvangrijk, complex of ongelijkmatig aanwezig zijn, waardoor de hoeveelheid therapeutisch materiaal per vesikel beperkt wordt en zorgen over veiligheid ontstaan.
Een klein maar krachtig scaffold vinden
Om dit op te lossen onderzocht het team systematisch eiwitten die voorkomen op EVs geproduceerd door een vaak gebruikte humane cellijn. Met drie onafhankelijke zuiveringsmethoden en massaspectrometrie selecteerden ze 15 kandidaten en fuseerden elk met een fluorescerende reporter om te meten hoe efficiënt het in vesikels werd gesorteerd. Eén viel op: ENPP1, dat cargo effectiever laadde dan veelgebruikte scaffolds zoals PTGFRN en Lamp2b. De wetenschappers snoeiden ENPP1 vervolgens terug tot meerdere kortere versies en ontdekten EN144, een fragment van slechts 144 aminozuren, dat drie keer meer reporter-eiwit in EVs verpakte dan de volledige ENPP1, terwijl grootte en structuur van de vesikels intact bleven. 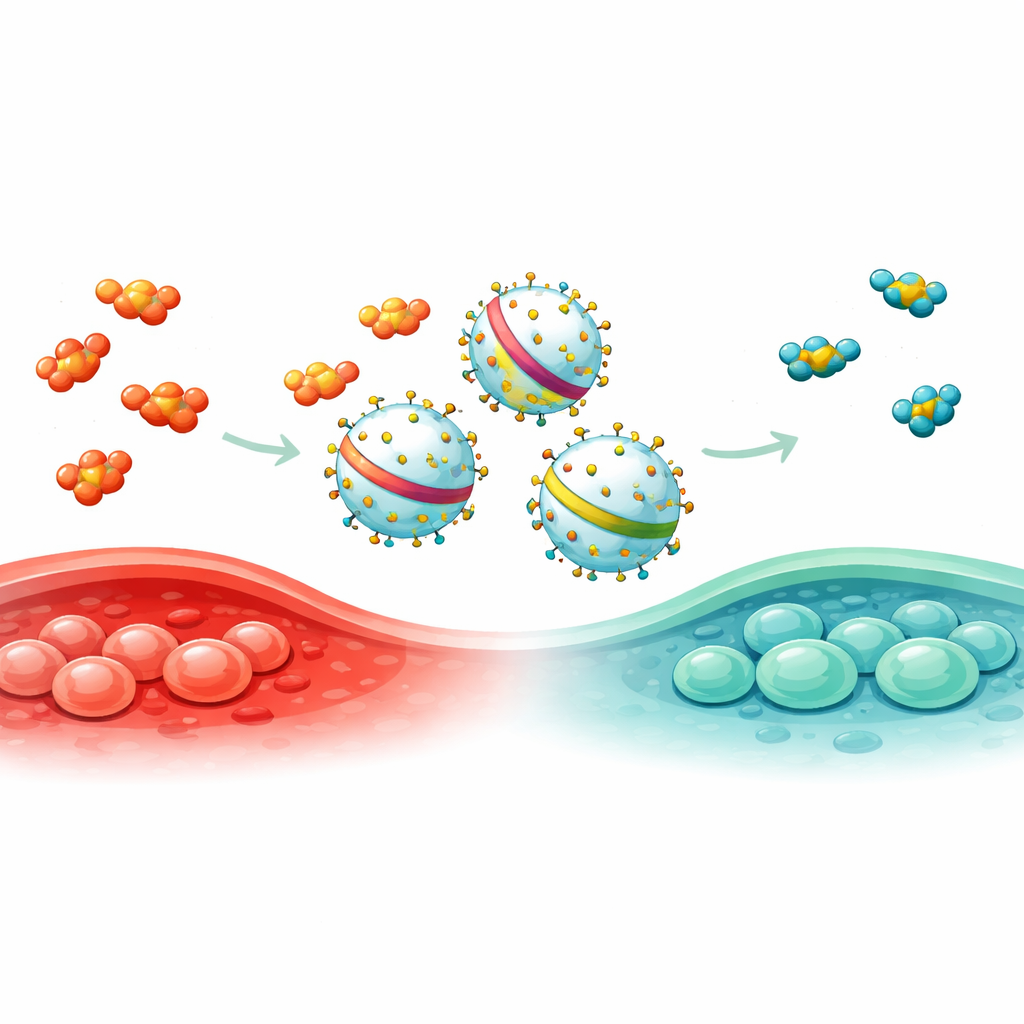
Veilige, veelzijdige vervoerders voor genetische en proteïne-lading
Aangezien elk afleveringssysteem veilig moet zijn, testten de onderzoekers EN144-versierde EVs in meerdere celtypen en in muizen. De vesikels toonden typische EV-markers, bleven binnen normale formaten en veroorzaakten weinig tot geen toxiciteit, zelfs bij hoge of herhaalde doses. Na injectie in muizen stapelden EN144-EVs zich voornamelijk op in de lever en milt, vergelijkbaar met standaard EVs, zonder organen te beschadigen of de bloedwaarden te verstoren. Het team toonde vervolgens dat EN144 kan fungeren als een moleculair dockingstation voor vele soorten lading. Door het te koppelen aan een kraakbeen-homing peptide maakten ze EVs die efficiënt werden opgenomen door chondrocyten, de cellen die het gewrichtskraakbeen onderhouden. Met RNA-bindende motieven verrijkten ze therapeutische mRNA in EVs en bevestigden dat ontvankelijke cellen dat mRNA vertaalden naar eiwit. Ze laadden ook CRISPR–Cas9-genbewerkingcomplexen via ontworpen proteïne–proteïneparen en toonden aan dat EV-afgeleverde editors een stil reporter-gen in doelcellen konden activeren.
Decoy-vesikels die schadelijke signalen opslorpen
Ontstekingsziekten zoals sepsis en artrose worden deels gedreven door het cytokine interleukine-6 (IL-6), dat een schadelijke "trans-signalerings"-modus kan aannemen wanneer het complexes vormt met een oplosbare receptor. Om deze schadelijke route selectief te blokkeren zonder IL-6’s nuttige rollen uit te schakelen, fuseerden de auteurs EN144 met gp130, een belangrijke IL-6-signaaltransducer, en creëerden EVs die gp130 als decoy op hun oppervlak tonen. In celculturen verminderden deze decoy-vesikels scherp de productie van ontstekingsbevorderende cytokinen. In een muismodel van sepsis verlaagden gp130-dragende EVs IL-6-niveaus in organen, dempten ze downstream-signaalgeving en verbeterden ze het overleven sterk, en deden dit beter dan doses oplosbaar gp130-eiwit. De vesikels bonden specifiek aan IL-6–receptorcomplexen, waardoor de pro-inflammatoire route werd afgeremd terwijl klassieke IL-6-signalisatie, belangrijk voor normale responsen, grotendeels intact bleef.
Bescherming van versleten gewrichten door gericht op kraakbeen
Om artrose aan te pakken combineerde het team target- en decoy-strategieën. Ze voegden het kraakbeen-homing peptide toe aan gp130-dragende EN144-EVs, waardoor deeltjes ontstonden die zowel naar chondrocyten toehomen als IL-6 trans-signaleringscomplexen neutraliseren. In gekweekte chondrocyten blootgesteld aan ontstekingssignalen verhoogden deze gerichte decoy-EVs de overleving en migratie van cellen en verminderden ze celdood. In ratten met chirurgisch geïnduceerde artrose leidden herhaalde injecties in het gewrichtsvocht tot sterke retentie van de EVs in het kraakbeen, minder afbraak van het gewrichtsoppervlak en gezonder kraakbeen onder de microscoop. Markers van weefselschade daalden, terwijl structurele eiwitten die kraakbeen behouden toenamen, en de balans van immuuncellen in het gewrichtsvlies verschoof naar een meer herstellend, minder ontstekingsbevorderend profiel.
Van klein scaffold naar breed therapeutisch platform
Door EN144 te isoleren als een minimaal, hoogpresterend scaffold verandert dit werk van nature voorkomende extracellulaire vesikels in een flexibel therapeutisch platform. Dezelfde kleine ankerplaats kan target-tags en decoy-receptoren op het vesikeloppervlak tonen terwijl genetische of proteïne-lading binnenin wordt geladen, allemaal met een veiligheidsprofiel vergelijkbaar met ongewijzigde vesikels. In diermodellen tamed EN144-gebaseerde "decoy EVs" levensbedreigende ontsteking en beschermden ze beschadigde gewrichten. Voor een leek impliceert dit dat we mogelijk op weg zijn naar geneesmiddelen opgebouwd uit de eigen afleverpakketjes van het lichaam, nauwkeurig ontworpen om de juiste werktuigen op de juiste plek te brengen en schadelijke signalen te dempen zonder de normale verdedigingen van het lichaam te stilzitten.
Bronvermelding: Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun 17, 3726 (2026). https://doi.org/10.1038/s41467-026-70451-x
Trefwoorden: extracellulaire vesikels, geneesmiddelbezorging, ontsteking, sepsis, artrose