Clear Sky Science · zh
坎地沙坦西雷替尔破坏耐甲氧西林金黄色葡萄球菌膜并增强庆大霉素与多粘菌素 B 的活性
把降压药变成对抗病菌的盟友
耐甲氧西林金黄色葡萄球菌(MRSA)是在医院和社区都很棘手的病原体,它能抵抗我们许多最有效的抗生素。本研究提出了一个出人意料的问题:常用的降压药坎地沙坦西雷替尔能否被重新利用来削弱 MRSA,使常规抗生素更有效?通过从化学、遗传、成像到动物模型的多角度研究,作者展示了这种药片如何削弱细菌防御并重振陈旧药物的效能。
为什么耐药性葡萄球菌如此难以治疗
MRSA 每年导致数十万例严重感染并造成数千人死亡。它难治的一个原因是其外膜和细胞壁充当了智能盾牌。构成该盾牌的脂类分子可以被重排,使其更坚硬、通透性更低并对常规抗生素更具抵抗性。一些 MRSA 细胞还会进入生长缓慢的“顽固态”或藏匿于黏性生物膜中,从而耐受通常能杀死活跃细菌的药物。这些特征强调了从细菌表面入手寻找新攻击方式的重要性,而不是再从头设计另一种传统抗生素。
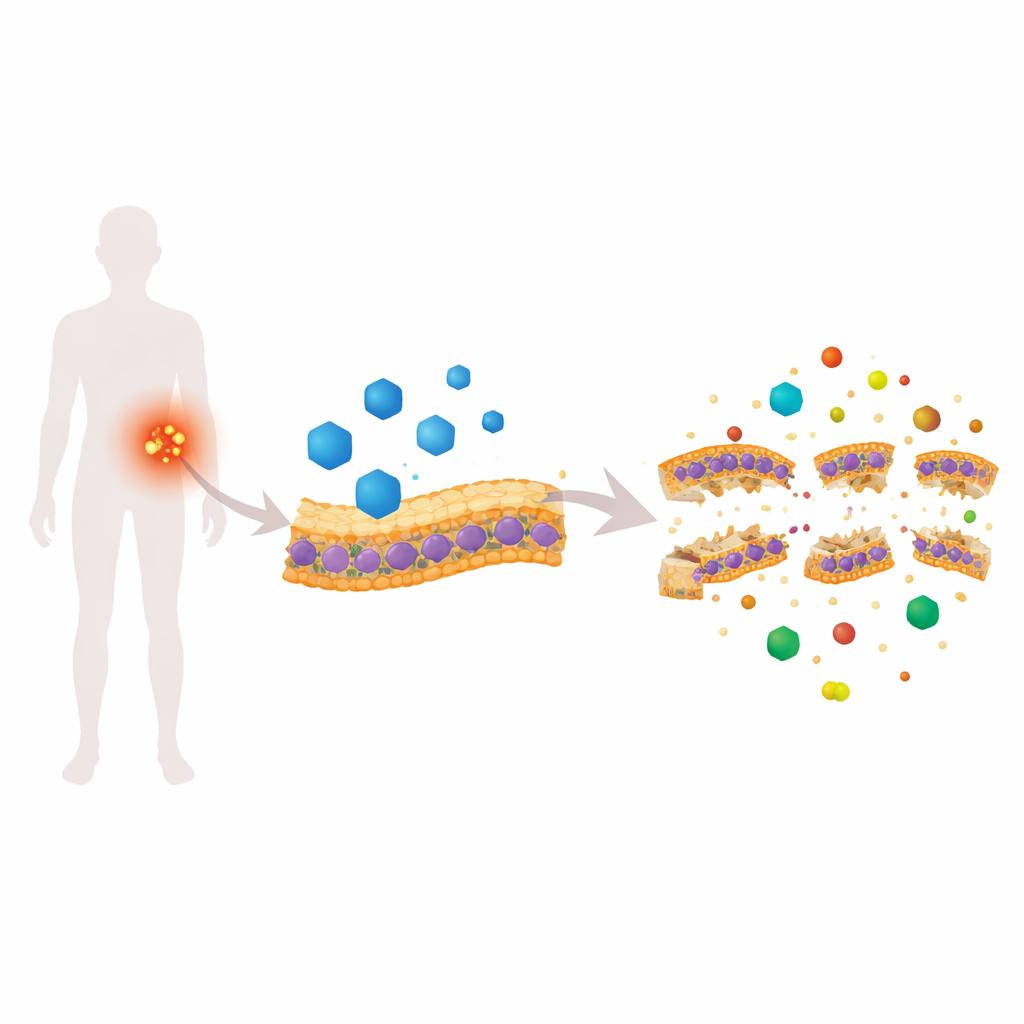
一种心血管药物攻击细菌“皮肤”
坎地沙坦西雷替尔(CC)获批用于治疗高血压,但在基于线虫的药物筛选中意外显示出对 MRSA 的强烈活性。在体外测试中,CC 能杀死处于分裂期的 MRSA 和更难对付的静止期细胞,并能减少生物膜的形成与存活率。用荧光染料进行的细致实验证明,CC 能快速使 MRSA 膜变得渗漏、破坏膜两侧的电化学梯度,并使细胞内环境变得异常碱性。高分辨成像——扫描电子显微镜、原子力显微镜、透射电子显微镜和三维冷冻断层显微——显示出鼓胀的表面、膜变薄以及可见的裂隙,均表明细菌“皮肤”在物理上受损。
重塑细菌的化学与脂质外衣
为理解 CC 在分子层面的作用,研究团队结合了 RNA 测序、代谢物分析和脂质谱分析。他们发现与细胞壁构建、膜脂合成和能量生成相关的基因与小分子在接触 CC 后总体下调,甚至在低于杀菌剂量的情况下也出现改变。若干关键磷脂——有助于维持膜完整性的分子——含量下降。一个显著变化涉及一类特定的长链 20 个碳原子的脂肪酸(称为 C20:0)。研究者用另一种化合物角鲨烯酰肼(cerulenin)耗竭这些脂肪酸后,MRSA 对 CC 的敏感性下降。补充回 C20:0 脂肪酸可恢复药物的大部分效能,独立的结合实验也显示 CC 可直接与 C20:0 相关的脂质及相关表面成分相互作用。膜“流动性”的测量表明,CC 实际上使 MRSA 膜变僵硬,将脂质锁定在更刚性的状态,最终破坏其功能。
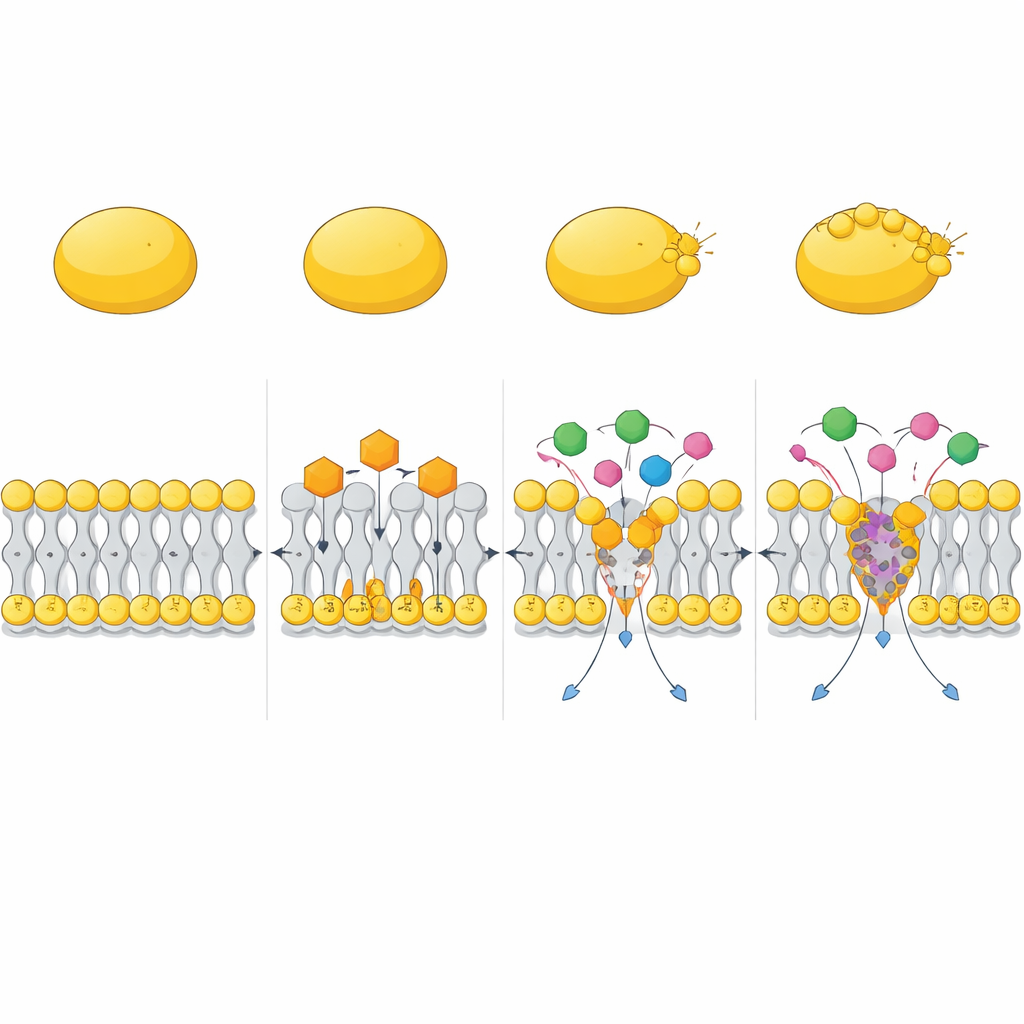
与现有抗生素携手作战
研究还测试了 CC 与现有药物的联用效果。在棋盘法和时间杀灭实验中,CC 显著增强了氨基糖苷类抗生素(如庆大霉素)以及多粘菌素 B 的活性。这些组合能迅速消灭既有增殖的 MRSA 也包括难以杀死的顽固细胞,而单药往往留下幸存者。计算机模拟提出了一个可能的机制:CC 可与多粘菌素 B 形成紧密复合体,更容易插入膜并比单独分子更强烈地扭曲膜结构,造成脂质层更深更广的变形。这有助于其他抗生素跨越膜屏障,更高效地到达其靶点。
从培养皿到活体动物
令人鼓舞的是,CC 的抗菌及助效作用并不限于试管内。在被 MRSA 感染的小型线虫和蜡蛾幼虫模型中,CC 提高了存活率。在使用高毒性 MRSA 菌株的小鼠大腿感染模型中,单独使用 CC 即能降低细菌计数,而其与庆大霉素联用相比未处理对照降低了约一千倍的细菌负荷。血液测定显示,在实验期间,小鼠体内可达到与体外有效剂量相似的药物水平,且未见明显的肝、肾或心脏组织损伤。
这对未来治疗意味着什么
简单来说,这项工作表明一种长期使用的降压药可以作为针对 MRSA 的膜靶向武器。通过结合细菌包膜中的特定脂肪构件、使膜变僵并在其上打孔,坎地沙坦西雷替尔既能直接杀死 MRSA,又能为老抗生素重获作用打开通道。尽管仍需更多关于安全性和剂量的研究——特别是因为该药也作用于人体血管——这些发现提示了一个有前景的捷径:与其完全发明新抗生素,不如重新利用现有药物来削弱细菌防御,恢复现有治疗手段的效力。
引用: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
关键词: MRSA, 抗生素耐药, 药物再利用, 细菌膜, 坎地沙坦西雷替尔