Clear Sky Science · sv
Candesartan cilexetil stör meticillinresistenta Staphylococcus aureus membran och förstärker aktivitet hos gentamicin och polymyxin B
Att förvandla en blodtrycksmedicin till en bakteriekämpe
Meticillinresistenta Staphylococcus aureus (MRSA) är en tålig vård- och samhällsrelaterad bakterie som står emot många av våra bästa antibiotika. Denna studie ställer en överraskande fråga: kan ett vanligt blodtrycksmedel, candesartan cilexetil, återanvändas för att försvaga MRSA och göra vanliga antibiotika mer effektiva? Genom att undersöka MRSA-celler från flera håll — kemi, genetik, avbildning och djurmodeller — visar forskarna hur detta läkemedel kan slå hål i bakteriernas försvar och återuppliva äldre läkemedel.
Varför läkemedelsresistent stafylokock är så svårbehandlad
MRSA orsakar hundratusentals allvarliga infektioner och tusentals dödsfall varje år. En anledning till att den är svår att behandla är att bakterien har ett yttre membran och en cellvägg som fungerar som en effektiv sköld. De fettmolekyler som bygger upp denna sköld kan omfördelas för att bli hårdare, mindre genomträngliga och mer motståndskraftiga mot vanliga antibiotika. Vissa MRSA-celler går även in i långsamväxande ”persister”-tillstånd eller gömmer sig i klibbiga biofilmer, där de tolererar läkemedel som normalt dödar aktiva bakterier. Dessa egenskaper gör det avgörande att hitta nya sätt att angripa bakterieytan snarare än att konstruera ännu ett traditionellt antibiotikum från grunden.
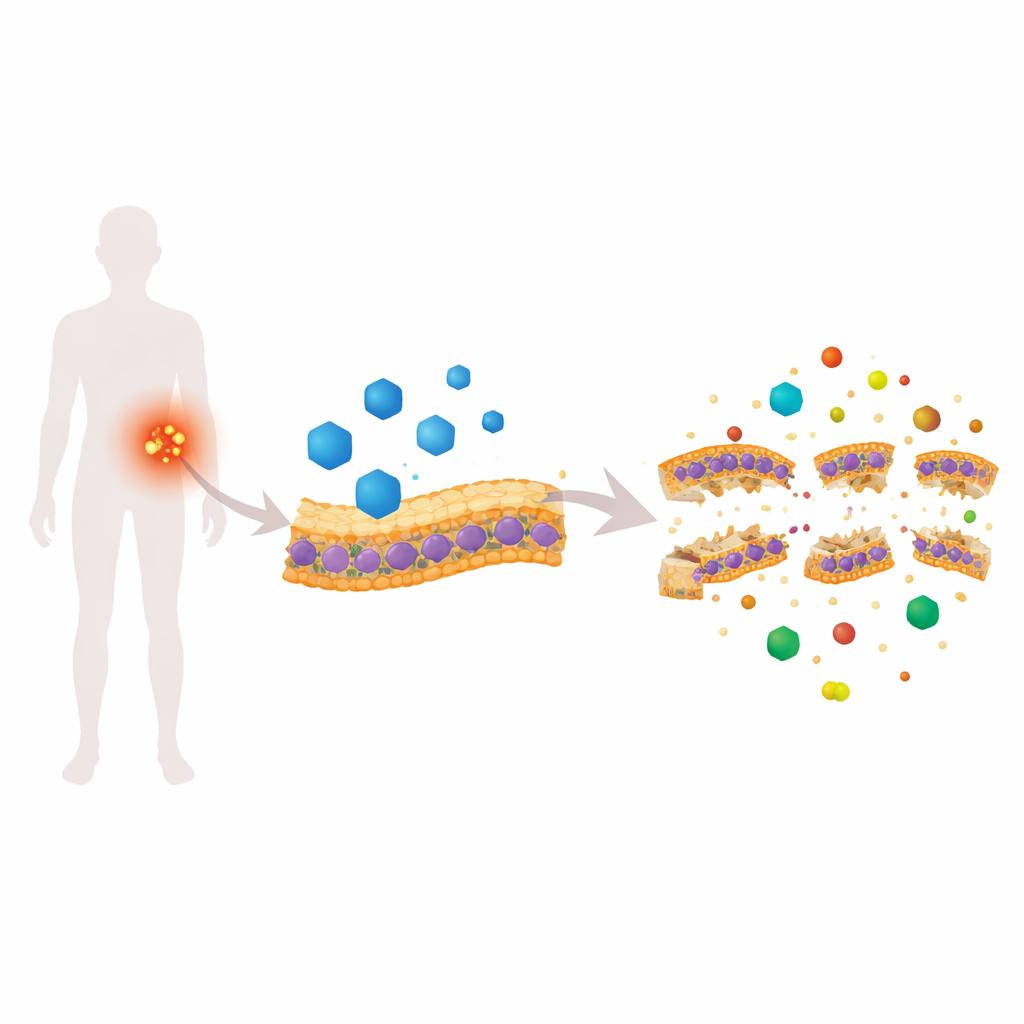
En hjärtmedicin som angriper bakteriehud
Candesartan cilexetil (CC) är godkänt för att behandla högt blodtryck, men i ett maskbaserat läkemedelsscreening visade det oväntat stark aktivitet mot MRSA. I laboratorietester dödade CC både aktivt delande MRSA och de mer envisa stationära cellerna, och det minskade bildningen och livsdugligheten hos biofilmer. Detaljerade experiment med fluorescerande färgämnen avslöjade att CC snabbt gör MRSA-membranet läckande, kollapsar den elektriska gradienten över det och gör insidan av cellen ovanligt alkalisk. Högupplöst avbildning — svepelektronmikroskopi, atomkraftmikroskopi, transmissionselektronmikroskopi och 3D-kryo-tomografi — visade blåsbildade ytor, förtunning av membranet och synliga sprickor, alla tecken på att bakterie"huden" är fysiskt komprometterad.
Omläggning av bakteriens kemi och fettlager
För att förstå vad CC gör under huven kombinerade teamet RNA-sekvensering, metabolitprofilering och lipidanalys. De fann att gener och småmolekyler som är involverade i uppbyggnad av cellvägg, syntes av membranlipider och energiproduktion i stort var nedreglerade efter CC-exponering, även vid doser för låga för att direkt döda. Flera nyckelfosfolipider som hjälper till att hålla membranet intakt minskade i mängd. En iögonfallande förändring gällde en särskild grupp långa 20-koliga fettsyror (kallade C20:0). När forskarna använde en annan förening, cerulenin, för att tömma dessa fettsyror blev MRSA mindre känslig för CC. Återföring av C20:0-fettsyror återställde mycket av läkemedlets effekt, och separata bindningsanalyser visade att CC direkt interagerar med C20:0-bundna lipider och relaterade ytkomponenter. Mätningar av membranets ”fluiditet” indikerade att CC faktiskt stelnar MRSA-membranet, låser lipider i ett mer stelt tillstånd som till slut underminerar dess funktion.
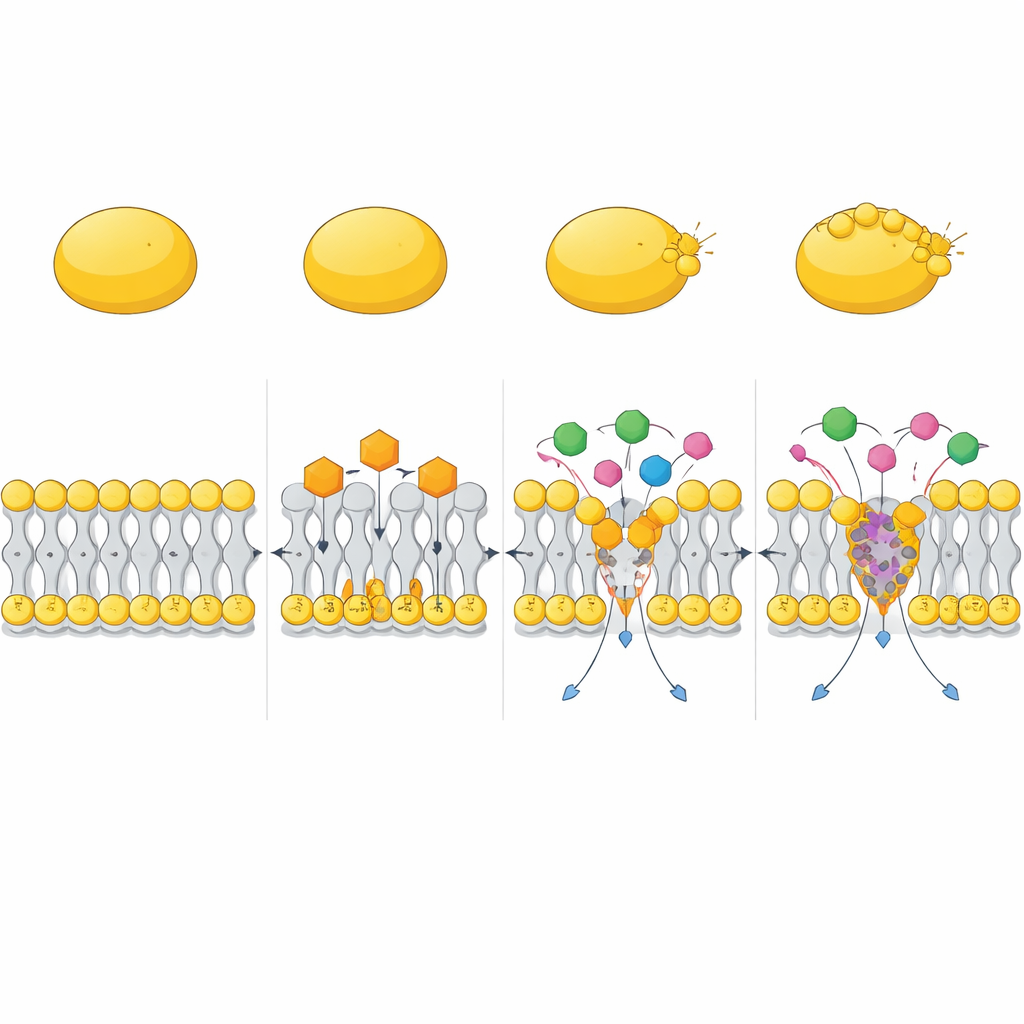
Samarbete med befintliga antibiotika
Studien testade också hur CC fungerar i kombination med befintliga läkemedel. I checkerboard- och time-kill-experiment förstärkte CC dramatiskt aktiviteten hos aminoglykosidantibiotika som gentamicin, liksom polymyxin B. Dessa kombinationer utplånade snabbt både aktivt växande MRSA och svårbehandlade persister-celler, medan de enskilda läkemedlen ofta lämnade kvar överlevare. Datorsimuleringar föreslog en förklaring: CC kan bilda kompakt komplex med polymyxin B som införlivas i membranet och deformerar det kraftfullare än någon av molekylerna för sig, vilket skapar djupa, långtgående deformationer i lipidlagret. Detta hjälper andra antibiotika att korsa membranbarriären och nå sina mål mer effektivt.
Från petriskål till levande djur
Lovande nog sträckte sig CC:s antibakteriella och hjälpande effekter bortom provröret. I små maskar och vaxmottlarver infekterade med MRSA förbättrade CC överlevnaden. I en mössmodell för lårinfektion med en virulent MRSA-stam minskade CC ensam bakteriemängden, och i kombination med gentamicin reducerade den bakteriebördan med ungefär tusen gånger jämfört med obehandlade kontroller. Blodmätningar visade att läkemedelsnivåer liknande de som var effektiva i laboratoriet kunde uppnås i möss utan uppenbara skador på lever, njure eller hjärta under experimentets gång.
Vad detta kan innebära för framtida behandlingar
Enkelt uttryckt visar detta arbete att ett länge använt blodtrycksmedel kan fungera som ett membranstyrt vapen mot MRSA. Genom att fästa vid specifika fettbyggstenar i bakterieomslaget, stelna membranet och slå hål på det, dödar candesartan cilexetil både MRSA direkt och öppnar dörren för att äldre antibiotika ska fungera igen. Även om fler säkerhets- och doseringsstudier behövs — särskilt eftersom detta läkemedel också verkar på människans blodkärl — tyder resultaten på en lovande genväg: istället för att uppfinna helt nya antibiotika kan vi omdisponera befintliga läkemedel för att försvaga bakteriers försvar och återställa kraften hos de behandlingar vi redan har.
Citering: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Nyckelord: MRSA, antibiotikaresistens, omprövning av läkemedel, bakteriellt membran, candesartan cilexetil