Clear Sky Science · nl
Candesartan cilexetil verstoort het membraan van methicilline-resistente Staphylococcus aureus en versterkt de werking van gentamicine en polymyxine B
Een bloeddrukpil als bondgenoot tegen ziektekiemen
Methicilline-resistente Staphylococcus aureus (MRSA) is een hardnekkige ziekenhuis- en gemeenschapsbacterie die veel van onze beste antibiotica negeert. Deze studie stelt een verrassende vraag: kan een veelgebruikt bloeddrukmiddel, candesartan cilexetil, worden hergebruikt om MRSA te verzwakken en standaardantibiotica effectiever te maken? Door MRSA-cellen van meerdere kanten te onderzoeken — chemisch, genetisch, met beeldvorming en in diermodellen — laten de onderzoekers zien hoe dit middel gaten kan slaan in bacteriële verdedigingslinies en oudere geneesmiddelen nieuw leven kan inblazen.
Waarom resistente stafylokokken zo moeilijk te bestrijden zijn
MRSA veroorzaakt jaarlijks honderden duizenden ernstige infecties en duizenden doden. Een reden dat behandeling zo lastig is, is dat de buitenmembraan en celwand van de bacterie fungeren als een slimme schild. De vettige moleculen in dit schild kunnen worden herschikt zodat ze harder, minder doorlaatbaar en resistenter tegen standaardantibiotica worden. Sommige MRSA-cellen gaan ook in langzaam groeiende “persister”-toestanden of verstoppen zich in kleverige biofilms, waar ze geneesmiddelen tolereren die normaal actieve bacteriën doden. Deze eigenschappen maken het cruciaal om nieuwe manieren te vinden om het bacteriële oppervlak aan te vallen in plaats van opnieuw een traditioneel antibioticum te ontwerpen.
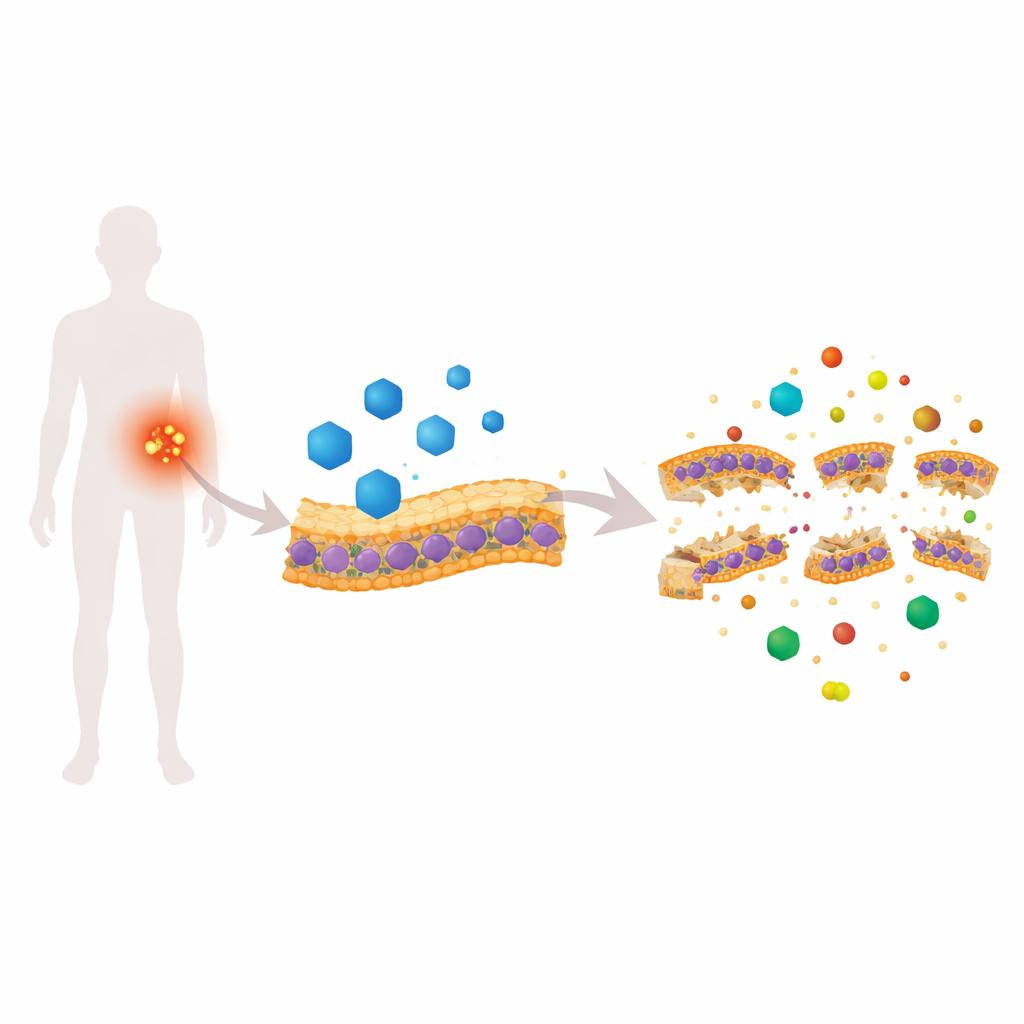
Een hartmedicijn dat bacteriële huidlagen aanvalt
Candesartan cilexetil (CC) is goedgekeurd voor de behandeling van hoge bloeddruk, maar in een wormgebaseerde medicijnscreening toonde het onverwacht sterke activiteit tegen MRSA. In laboratoriumtests doodde CC zowel actief delende MRSA als de moeilijkere stationaire-fasecellen, en verminderde het de vorming en levensvatbaarheid van biofilms. Gedetailleerde experimenten met fluorescente kleurstoffen toonden aan dat CC snel het MRSA-membraan lek maakt, de elektrische gradiënt erover doet instorten en het binnenste van de cel abnormaal alkalisch maakt. Hoge-resolutiebeeldvorming — scanning elektronenmicroscopie, atomaire krachtmicroscopie, transmissie-elektronenmicroscopie en 3D cryo-tomografie — toonde geblisterde oppervlakken, verdunning van het membraan en zichtbare gaten, allemaal tekenen dat de bacteriële “huid” fysiek is aangetast.
De biochemie en vetlaag van de bacterie herbedraden
Om te begrijpen wat CC onder de motorkap doet, combineerde het team RNA-sequencing, metabolietprofielen en lipidenanalyse. Ze vonden dat genen en kleine moleculen die betrokken zijn bij de opbouw van de celwand, de aanmaak van membraanfosfolipiden en het genereren van energie over het algemeen werden teruggeschroefd na blootstelling aan CC, zelfs bij doses te laag om direct te doden. Verscheidene belangrijke fosfolipiden die bijdragen aan membraanintegriteit namen in hoeveelheid af. Een opvallende verandering betrof een specifieke groep lange, 20-koolstofvetzuren (genoemd C20:0). Toen de onderzoekers een ander verbinding, cerulenin, gebruikten om deze vetzuren uit te putten, werd MRSA minder gevoelig voor CC. Het toevoegen van C20:0-vetzuren herstelde veel van de werking van het middel, en afzonderlijke bindingsassays toonden aan dat CC direct interageert met C20:0-gebonden lipiden en gerelateerde oppervlaktecomponenten. Metingen van membraan“fluiditeit” wezen uit dat CC het MRSA-membraan juist verstijft, lipiden in een stijverer stadium vergrendelt en zodoende uiteindelijk de functie ondermijnt.
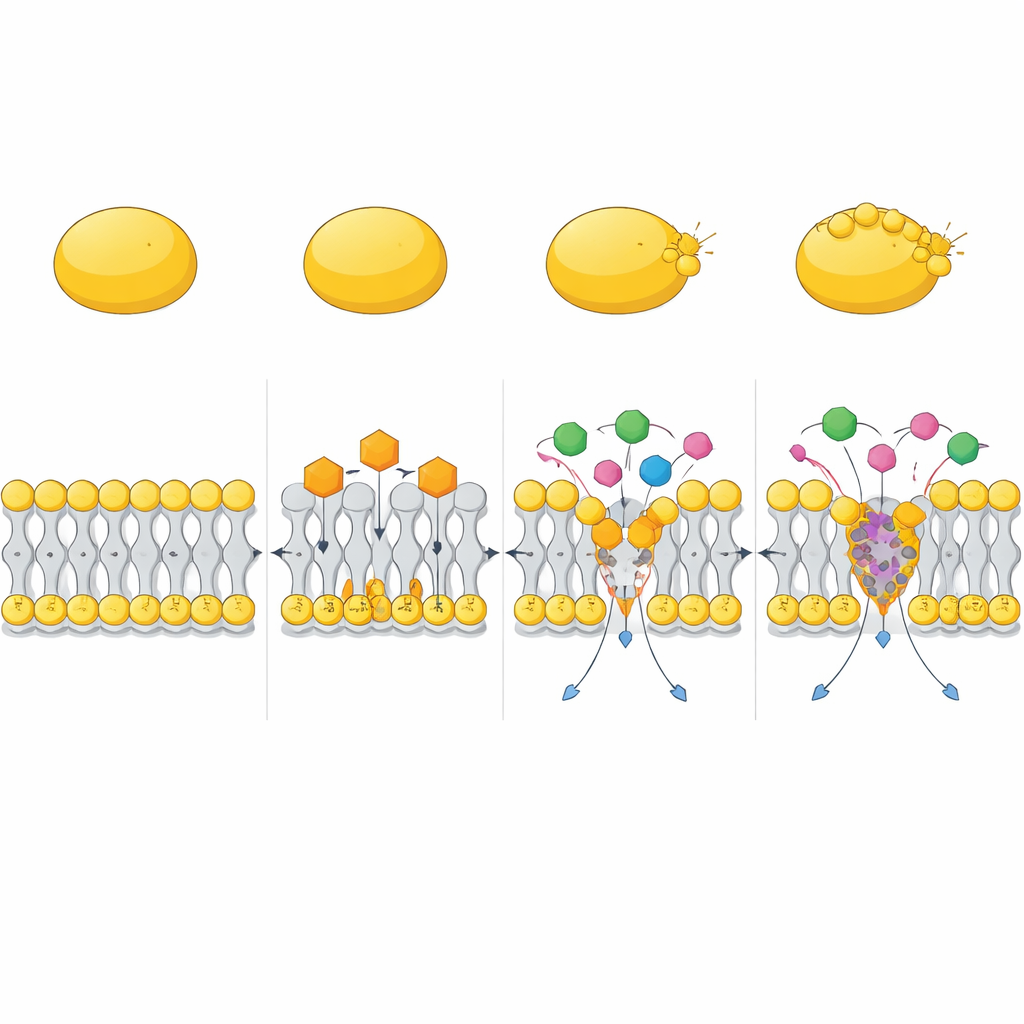
Samenwerken met bestaande antibiotica
De studie testte ook hoe CC zich gedraagt in combinatie met bestaande geneesmiddelen. In checkerboard- en time-kill-experimenten versterkte CC de werking van aminoglycoside-antibiotica zoals gentamicine en ook van polymyxine B aanzienlijk. Deze combinaties wisten zowel actief groeiende MRSA als moeilijk te doden persistercellen snel uit te roeien, terwijl de individuele middelen vaak overlevenden lieten. Computersimulaties suggereerden een verklaring: CC kan compacte complexen vormen met polymyxine B die in het membraan inserteren en het krachtiger vervormen dan elk molecuul afzonderlijk, waardoor diepe, ver reikende deformaties in de lipidenlaag ontstaan. Dit helpt andere antibiotica om de membraanbarrière te passeren en hun doelwitten efficiënter te bereiken.
Van petrischaal naar levende dieren
Veelbelovend reikten de antibacteriële en hulpgevende effecten van CC verder dan het reageerbuisje. In kleine wormen en wasmotlarven geïnfecteerd met MRSA verbeterde CC de overleving. In een muismodel van dijbeeninfectie met een virulent MRSA-stam verminderde CC alleen de bacteriële aantallen, en de combinatie met gentamicine verlaagde de bacteriële last ongeveer duizendvoudig vergeleken met niet-behandelde controles. Bloedmetingen toonden aan dat medicijnniveaus vergelijkbaar met die effectief in het lab in muizen konden worden bereikt zonder duidelijke schade aan lever-, nier- of hartweefsel gedurende het experiment.
Wat dit kan betekenen voor toekomstige behandelingen
In gewone bewoordingen laat dit werk zien dat een langgebruikt bloeddrukmiddel ook dienst kan doen als een membraan-gerichte wapen tegen MRSA. Door zich te hechten aan specifieke vettige bouwstenen in de bacteriële omhulling, het membraan te verstijven en er gaten in te prikken, doodt candesartan cilexetil MRSA zowel rechtstreeks als helpt het oudere antibiotica weer effectief te maken. Hoewel meer veiligheids- en doseringsonderzoek nodig is — vooral omdat dit middel ook op menselijke bloedvaten werkt — wijzen de bevindingen op een veelbelovende kortere weg: in plaats van volledig nieuwe antibiotica uit te vinden, kunnen we bestaande middelen herinzetten om bacteriële verdedigingslinies te verzwakken en de werking van bestaande behandelingen te herstellen.
Bronvermelding: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Trefwoorden: MRSA, antibioticaresistentie, herbestemming van geneesmiddelen, bacterieel membraan, candesartan cilexetil