Clear Sky Science · ru
Цилексетил кандесартана нарушает мембрану метициллин-резистентного Staphylococcus aureus и усиливает активность гентамицина и полимиксина B
Переосмысление лекарства от давления как союзника в борьбе с микробами
Метициллин-резистентный Staphylococcus aureus (MRSA) — стойкий возбудитель госпитальных и внебольничных инфекций, который сопротивляется многим нашим лучшим антибиотикам. В этом исследовании поставлен неожиданный вопрос: можно ли перепрофилировать распространённый препарат для снижения давления — цилексетил кандесартан — чтобы ослабить MRSA и повысить эффективность стандартных антибиотиков? Исследователи опробовали воздействие на MRSA с разных сторон — химии, генетики, визуализации и на животных моделях — и показали, как это средство пробивает оборону бактерий и возрождает действие старых препаратов.
Почему устойчивый стафилококк так трудно лечить
MRSA вызывает сотни тысяч тяжёлых инфекций и тысячи смертей ежегодно. Одна из причин трудности лечения — наружная мембрана и клеточная стенка бактерии, которые действуют как умный щит. Жирные молекулы в этом щите могут перестраиваться, делая оболочку более жёсткой, менее проницаемой и более устойчивой к стандартным антибиотикам. Некоторые клетки MRSA также входят в медленнорастущие «персистентные» состояния или прячутся в вязких биоплёнках, где они терпят препараты, которые обычно убивают активные бактерии. Эти особенности делают важным поиск новых способов атаки поверхности бактерий, а не разработку ещё одного традиционного антибиотика с нуля.
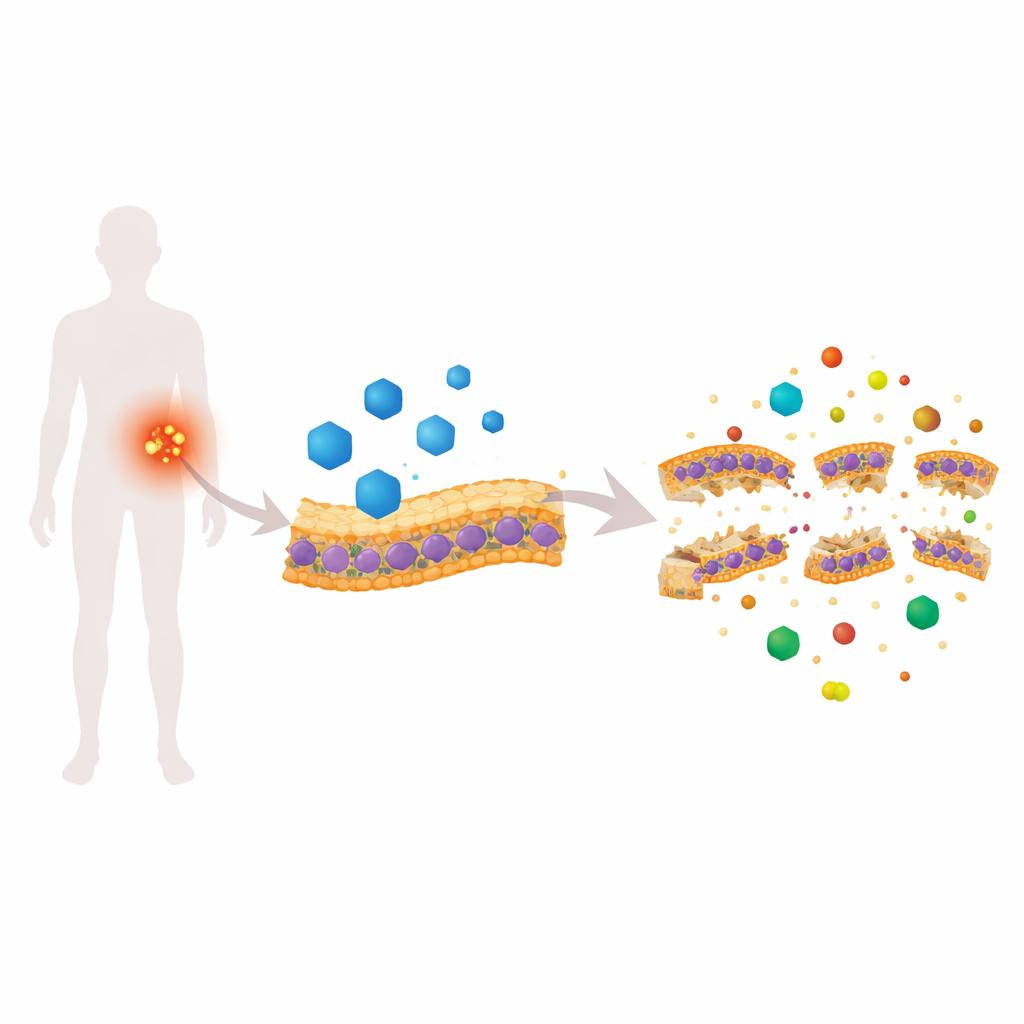
Кардиологическое средство, атакующее бактериальную «кожу»
Цилексетил кандесартана (ЦК) одобрен для лечения высокого кровяного давления, но в скрининге на червях он неожиданно показал сильную активность против MRSA. В лабораторных тестах ЦК убивал активно делящиеся клетки MRSA и более упрямые клетки в стационарной фазе, а также снижал образование и жизнеспособность биоплёнок. Детальные эксперименты с флуоресцентными красителями показали, что ЦК быстро делает мембрану MRSA проницаемой, разрушает электрический градиент через неё и вызывает необычное повышение внутренней щёлочности клетки. Высокоточная визуализация — сканирующая электронная микроскопия, атомно-силовая микроскопия, просвечивающая электронная микроскопия и 3D крио-томография — выявила пузыристую поверхность, истончение мембраны и видимые зазоры, все признаки физического нарушения бактериальной «кожи».
Перенастройка химии и жирового покрова бактерии
Чтобы понять механизмы действия ЦК, команда объединила РНК-секвенирование, профилирование метаболитов и анализ липидов. Они обнаружили, что гены и малые молекулы, вовлечённые в синтез клеточной стенки, образование мембранных липидов и генерацию энергии, в целом снижали активность после воздействия ЦК, даже при дозах, недостаточных для немедленной гибели. Несколько ключевых фосфолипидов, поддерживающих целостность мембраны, уменьшились в количестве. Яркое изменение касалось определённой группы длинных 20-углеродных жирных кислот (обозначаемых как C20:0). Когда исследователи использовали другой соединение, церуленин, для истощения этих жирных кислот, MRSA стал менее чувствителен к ЦК. Возврат C20:0 жирных кислот восстанавливал большую часть эффекта препарата, а отдельные связывающие тесты показали прямое взаимодействие ЦК с липидами, связанными с C20:0, и с родственными поверхностными компонентами. Измерения «текучести» мембраны указывали, что ЦК фактически делает мембрану MRSA более жёсткой, фиксируя липиды в более ригидном состоянии, что в конечном счёте подрывает её функции.
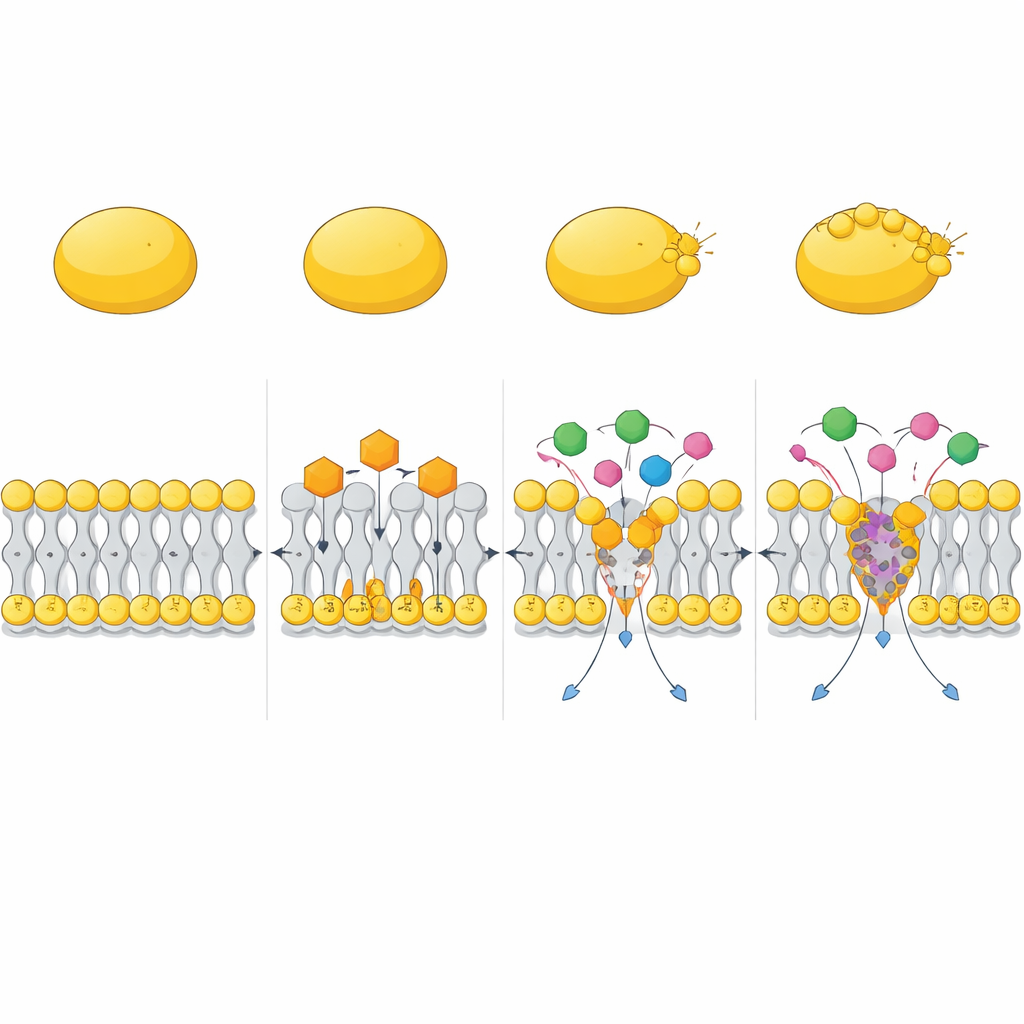
Сотрудничество с существующими антибиотиками
Исследование также оценивало поведение ЦК в сочетании с уже существующими препаратами. В экспериментах «шахматной доски» и тестах на время-убийство ЦК значительно усиливал активность аминогликозидных антибиотиков, таких как гентамицин, а также полимиксина B. Эти комбинации быстро уничтожали как активно растущий MRSA, так и трудноубиваемые персистентные клетки, тогда как отдельные препараты часто оставляли выживших. Компьютерные моделирования предложили одно объяснение: ЦК может образовывать компактные комплексы с полимиксином B, которые внедряются в мембрану и деформируют её мощнее, чем каждая молекула по отдельности, создавая глубокие, далеко идущие искажения липидного слоя. Это облегчает другим антибиотикам преодоление мембранного барьера и более эффективный доступ к их мишеням.
От чашки Петри до живых организмов
Обнадеживающе, антибактериальные и вспомогательные эффекты ЦК проявились не только в пробирке. В маленьких круглых червях и личинках восковой моли, инфицированных MRSA, ЦК улучшал выживаемость. В мышиной модели инфекции бедренной мышцы с вирулентным штаммом MRSA ЦК в одиночку снижал количество бактерий, а его комбинация с гентамицином уменьшала бактериальную нагрузку примерно в тысячу раз по сравнению с нелечеными контрольными животными. Измерения в крови показали, что уровни препарата, сопоставимые с эффективными в лаборатории, можно достигнуть у мышей без очевидного повреждения печени, почек или сердца в течение эксперимента.
Какие перспективы для будущих методов лечения
Проще говоря, эта работа показывает, что давно используемое средство от давления может выполнять роль направленного на мембрану оружия против MRSA. Связываясь с определёнными жирными строительными блоками в бактериальной оболочке, делая мембрану жёстче и проделывая в ней отверстия, цилексетил кандесартан одновременно убивает MRSA и открывает путь для старых антибиотиков вернуться в строй. Хотя необходимы дополнительные исследования безопасности и дозирования — особенно учитывая, что препарат также действует на сосуды человека — результаты указывают на многообещающий короткий путь: вместо изобретения полностью новых антибиотиков можно перенастроить существующие лекарства, чтобы ослабить барьеры бактерий и восстановить эффективность уже имеющихся терапий.
Цитирование: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Ключевые слова: MRSA, антибиотикорезистентность, переназначение лекарств, бактериальная мембрана, цилексетил кандесартана