Clear Sky Science · fr
Le cilexétil de candésartan perturbe la membrane du Staphylococcus aureus résistant à la méthicilline et potentialise l’activité de la gentamicine et de la polymyxine B
Transformer un comprimé pour la tension artérielle en allié anti-germes
Le Staphylococcus aureus résistant à la méthicilline (MRSA) est un germe tenace, rencontré à la fois à l’hôpital et en communauté, qui résiste à bon nombre de nos meilleurs antibiotiques. Cette étude pose une question surprenante : un médicament courant contre l’hypertension, le cilexétil de candésartan, peut‑il être réutilisé pour affaiblir le MRSA et rendre les antibiotiques classiques plus efficaces ? En sondant les cellules de MRSA sous plusieurs angles — chimie, génétique, imagerie et modèles animaux — les chercheurs montrent comment ce comprimé peut percer les défenses bactériennes et raviver l’efficacité d’anciens médicaments.
Pourquoi le staphylocoque résistant est si difficile à traiter
Le MRSA provoque chaque année des centaines de milliers d’infections graves et des milliers de décès. Une des raisons qui rendent son traitement si difficile tient à la présence d’une enveloppe externe et d’une paroi cellulaire qui forment un bouclier sophistiqué. Les molécules lipidiques de ce bouclier peuvent être réarrangées pour devenir plus dures, moins perméables et plus résistantes aux antibiotiques classiques. Certaines cellules de MRSA entrent aussi dans des états de faible croissance dits « persisters » ou se cachent dans des biofilms adhésifs, où elles tolèrent des médicaments qui tueraient normalement des bactéries actives. Ces caractéristiques rendent cruciales la recherche de nouvelles façons d’attaquer la surface bactérienne plutôt que de concevoir encore un antibiotique traditionnel à partir de zéro.
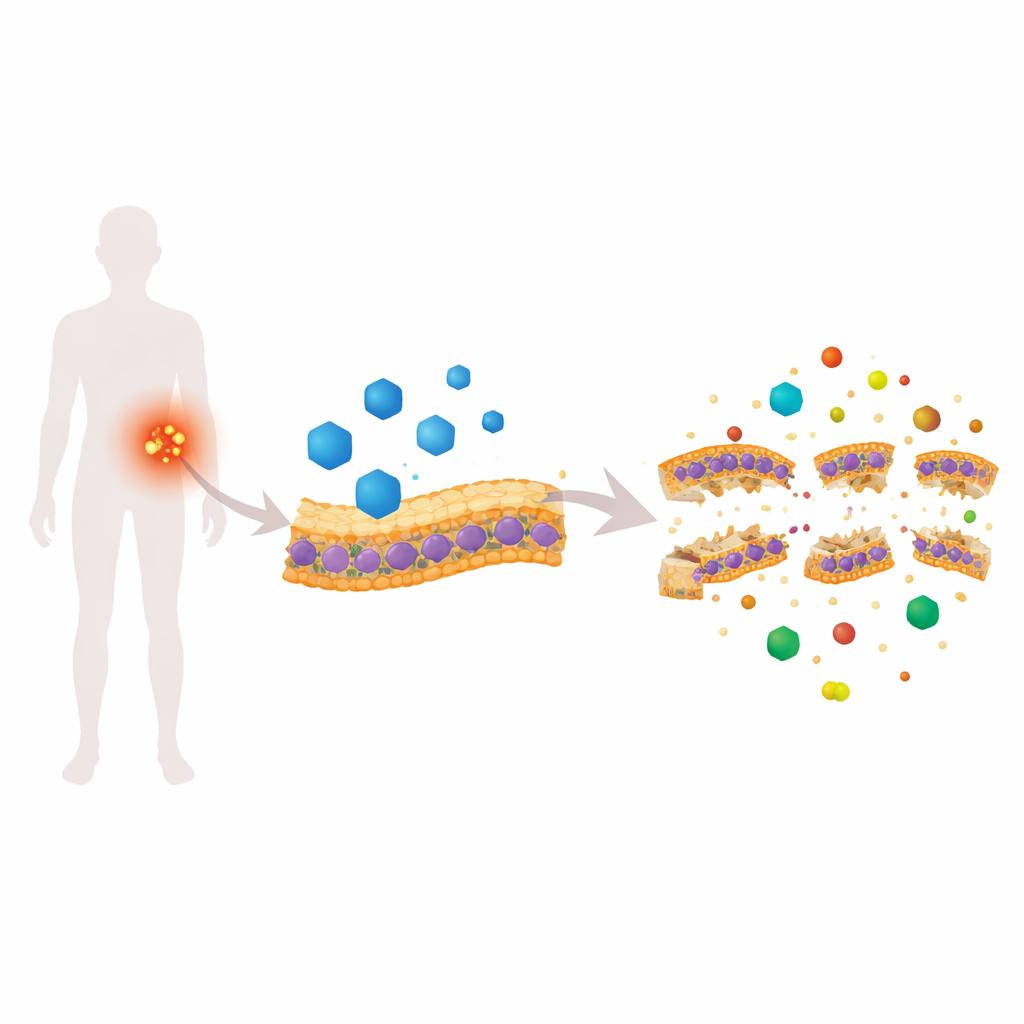
Un médicament cardiaque qui attaque la « peau » bactérienne
Le cilexétil de candésartan (CC) est approuvé pour traiter l’hypertension, mais lors d’un criblage de médicaments chez le ver il a montré de manière inattendue une forte activité contre le MRSA. En laboratoire, le CC a tué les MRSA en division active ainsi que les cellules plus tenaces en phase stationnaire, et il a réduit la formation et la viabilité des biofilms. Des expériences détaillées avec des colorants fluorescents ont révélé que le CC rend rapidement la membrane du MRSA perméable, effondre le gradient électrique à travers elle et rend l’intérieur de la cellule anormalement alcalin. L’imagerie à haute résolution — microscopie électronique à balayage, microscopie à force atomique, microscopie électronique en transmission et cryo-tomographie 3D — a montré des surfaces cloquées, un amincissement de la membrane et des lacunes visibles, autant de signes que la « peau » bactérienne est compromise sur le plan physique.
Reconfigurer la chimie et l’enveloppe lipidique du germe
Pour comprendre ce que fait le CC en profondeur, l’équipe a combiné séquençage d’ARN, profilage des métabolites et analyse des lipides. Ils ont trouvé que les gènes et petites molécules impliqués dans la construction de la paroi cellulaire, la synthèse des lipides membranaires et la production d’énergie étaient globalement atténués après exposition au CC, même à des doses trop faibles pour tuer directement. Plusieurs phospholipides clés qui contribuent à la cohésion membranaire ont diminué en abondance. Une variation frappante concernait un groupe particulier d’acides gras longs de 20 carbones (appelés C20:0). Lorsque les chercheurs ont utilisé un autre composé, la cérulénine, pour épuiser ces acides gras, le MRSA est devenu moins sensible au CC. La réintroduction d’acides gras C20:0 a restauré une grande partie de l’effet du médicament, et des tests de liaison séparés ont montré que le CC interagit directement avec des lipides liés au C20:0 et des composants de surface apparentés. Des mesures de la « fluidité » membranaire ont indiqué que le CC rigidifie en réalité la membrane du MRSA, verrouillant les lipides dans un état plus rigide qui compromet finalement sa fonction.
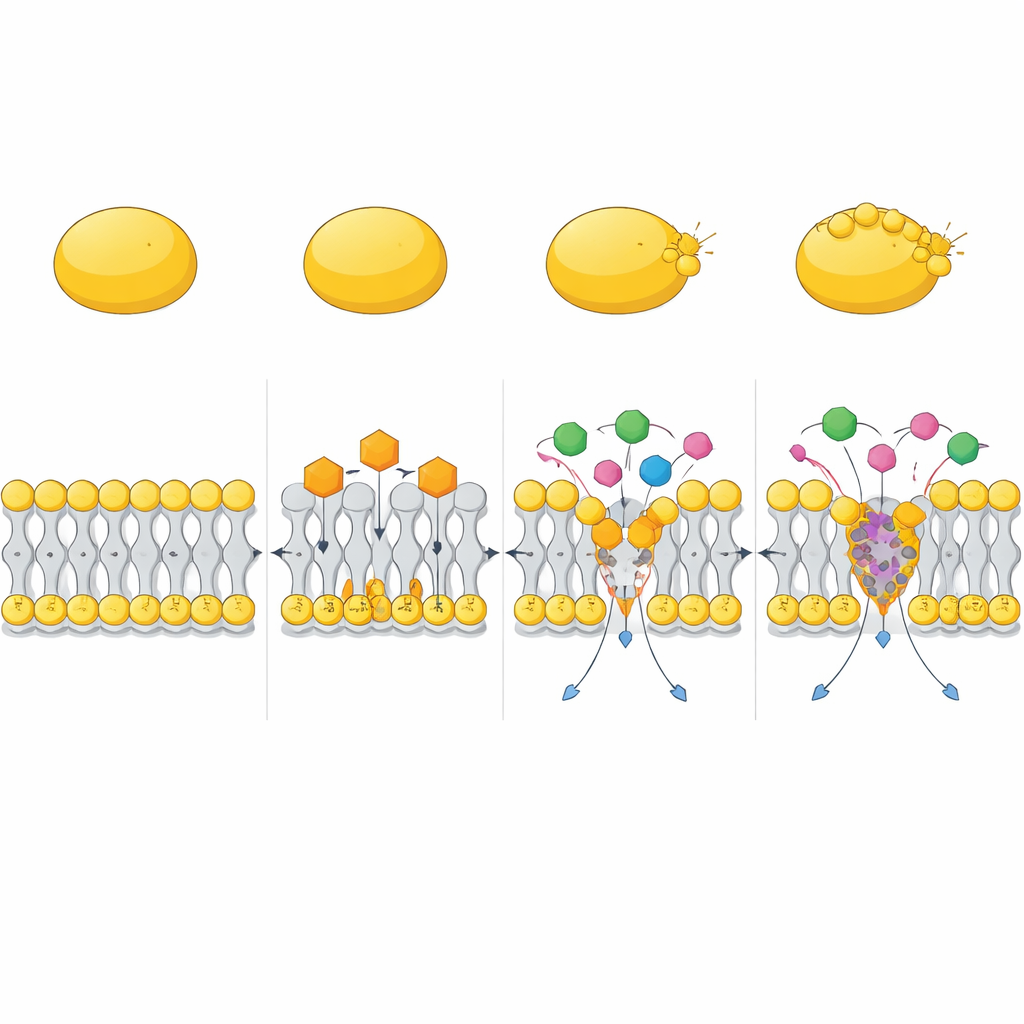
S’associer aux antibiotiques existants
L’étude a aussi testé le comportement du CC en association avec des médicaments existants. Dans des expériences en damier et de cinétique bactéricide, le CC a considérablement renforcé l’activité des antibiotiques aminoglycosides comme la gentamicine, ainsi que de la polymyxine B. Ces combinaisons ont rapidement éliminé à la fois les MRSA en croissance active et les cellules persisters difficiles à tuer, alors que les médicaments pris séparément laissaient souvent des survivants. Des simulations informatiques ont suggéré une raison possible : le CC peut former des complexes compacts avec la polymyxine B qui s’insèrent dans la membrane et la déforment plus puissamment que chaque molécule isolée, créant des déformations profondes et étendues dans la couche lipidique. Cela aide d’autres antibiotiques à traverser la barrière membranaire et à atteindre leurs cibles plus efficacement.
De la boîte de Pétri aux animaux vivants
De façon encourageante, les effets antibactériens et d’appoint du CC se sont étendus au‑delà de l’éprouvette. Chez de petits vers et des larves de cire infectés par le MRSA, le CC a amélioré la survie. Dans un modèle d’infection de la cuisse chez la souris utilisant une souche virulente de MRSA, le CC seul a réduit les comptes bactériens, et son association avec la gentamicine a diminué la charge bactérienne d’environ mille fois par rapport aux témoins non traités. Les mesures sanguines ont montré que des concentrations du médicament similaires à celles efficaces en laboratoire pouvaient être atteintes chez la souris sans dégâts évidents au foie, aux reins ou au cœur au cours de l’expérience.
Ce que cela pourrait signifier pour les traitements futurs
En termes clairs, ce travail révèle qu’un médicament antihypertenseur utilisé de longue date peut faire double emploi comme arme ciblant la membrane contre le MRSA. En se liant à des blocs lipidiques spécifiques de l’enveloppe bactérienne, en rigidifiant la membrane et en y perçant des trous, le cilexétil de candésartan tue le MRSA directement et ouvre la voie pour que de vieux antibiotiques retrouvent leur efficacité. Bien que des études supplémentaires sur la sécurité et les posologies soient nécessaires — d’autant que ce médicament agit aussi sur les vaisseaux sanguins humains — ces résultats suggèrent un raccourci prometteur : plutôt que d’inventer entièrement de nouveaux antibiotiques, nous pourrions réorienter des médicaments existants pour affaiblir les défenses bactériennes et restaurer la puissance des traitements dont nous disposons déjà.
Citation: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Mots-clés: MRSA, résistance aux antibiotiques, repositionnement de médicaments, membrane bactérienne, cilexétil de candésartan