Clear Sky Science · de
Candesartan cilexetil zerstört die Membran von methicillinresistenten Staphylococcus aureus und verstärkt die Wirkung von Gentamicin und Polymyxin B
Eine Blutdrucktablette als Verbündeter gegen Keime
Methicillin-resistenter Staphylococcus aureus (MRSA) ist ein hartnäckiger Krankenhaus- und Gemeinschaftserreger, der vielen unserer besten Antibiotika trotzt. Diese Studie stellt eine überraschende Frage: Kann ein gängiges Blutdruckmedikament, Candesartan cilexetil, umgenutzt werden, um MRSA zu schwächen und herkömmliche Antibiotika wirksamer zu machen? Durch Untersuchungen der MRSA-Zellen aus chemischen, genetischen, bildgebenden und tierexperimentellen Blickwinkeln zeigen die Forschenden, wie dieses Präparat die bakteriellen Abwehrmechanismen angreift und ältere Wirkstoffe wiederbelebt.
Warum sich resistente Staphylokokken so schwer behandeln lassen
MRSA verursacht jährlich Hunderttausende schwerer Infektionen und Tausende von Todesfällen. Ein Grund für die schwierige Behandlung ist, dass die Außenmembran und die Zellwand des Bakteriums als intelligente Schutzschicht fungieren. Die fettartigen Bausteine dieser Hülle können neu angeordnet werden, sodass sie härter, weniger durchlässig und resistenter gegen gängige Antibiotika wird. Manche MRSA-Zellen gehen zudem in langsame „Persister“-Zustände oder verstecken sich in klebrigen Biofilmen, wo sie Medikamente tolerieren, die normalerweise aktive Bakterien töten. Diese Eigenschaften machen es wichtig, neue Wege zu finden, die bakterielle Oberfläche anzugreifen, statt erneut nur klassische Antibiotika zu entwickeln.
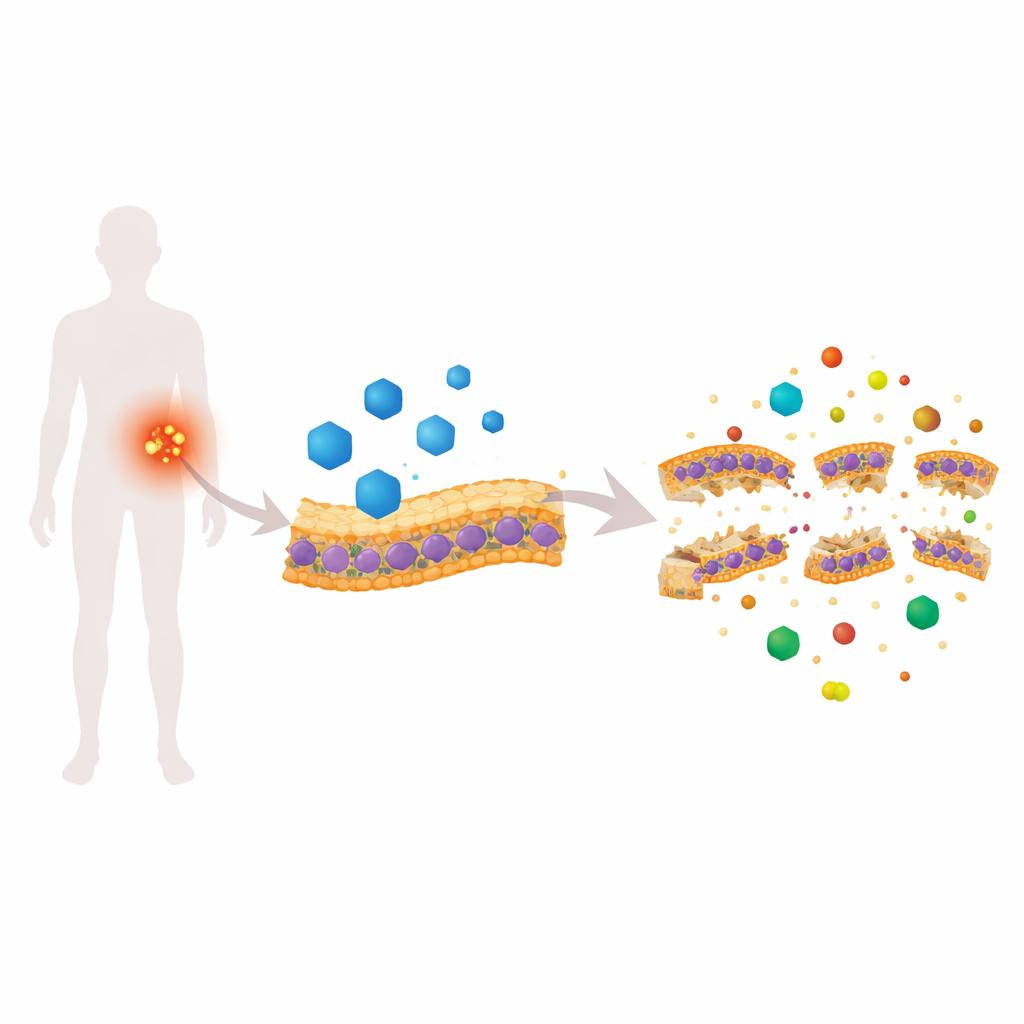
Ein Herzmedikament, das bakterielle Häute angreift
Candesartan cilexetil (CC) ist zur Behandlung von Bluthochdruck zugelassen, zeigte aber in einem Wurm-basierten Wirkstoffscreen unerwartet starke Aktivität gegen MRSA. In Laborversuchen tötete CC aktiv teilende MRSA sowie die hartnäckigeren stationären Zellen und verringerte die Biofilmbildung und -vitalität. Detaillierte Experimente mit fluoreszierenden Farbstoffen zeigten, dass CC die MRSA-Membran schnell durchlässig macht, das elektrische Gradienten über die Membran kollabieren lässt und das Zellinnere ungewöhnlich alkalisch werden lässt. Hochauflösende Bildgebung — Rasterelektronenmikroskopie, Rasterkraftmikroskopie, Transmissions-Elektronenmikroskopie und 3D-Kryo-Tomographie — zeigte aufgeblähte Oberflächen, eine Ausdünnung der Membran und sichtbare Lücken, alles Anzeichen dafür, dass die bakterielle „Haut“ physisch beschädigt ist.
Umschaltung der bakteriellen Chemie und Fettschicht
Um zu verstehen, was CC unter der Oberfläche bewirkt, kombinierten die Forschenden RNA-Sequenzierung, Metabolitprofiling und Lipidanalysen. Sie fanden, dass Gene und kleine Moleküle, die am Aufbau der Zellwand, der Synthese von Membranlipiden und der Energieerzeugung beteiligt sind, nach CC-Exposition breit herunterreguliert wurden — selbst bei Dosen, die nicht unmittelbar töten. Mehrere Schlüsselphospholipide, die die Membran stabilisieren, gingen in der Menge zurück. Eine auffällige Veränderung betraf eine bestimmte Gruppe langer 20-Kohlenstoff-Fettsäuren (genannt C20:0). Als die Forschenden eine andere Verbindung, Cerulenin, einsetzten, um diese Fettsäuren zu vermindern, wurden MRSA-Zellen weniger empfindlich gegenüber CC. Das Wiederzufügen von C20:0-Fettsäuren stellte einen Großteil der Wirkung des Wirkstoffs wieder her, und separate Bindungsassays zeigten, dass CC direkt mit C20:0-gebundenen Lipiden und verwandten Oberflächenkomponenten interagiert. Messungen der Membran„Fluidität“ deuteten darauf hin, dass CC die MRSA-Membran tatsächlich versteift und Lipide in einem starreren Zustand fixiert, was letztlich ihre Funktion untergräbt.
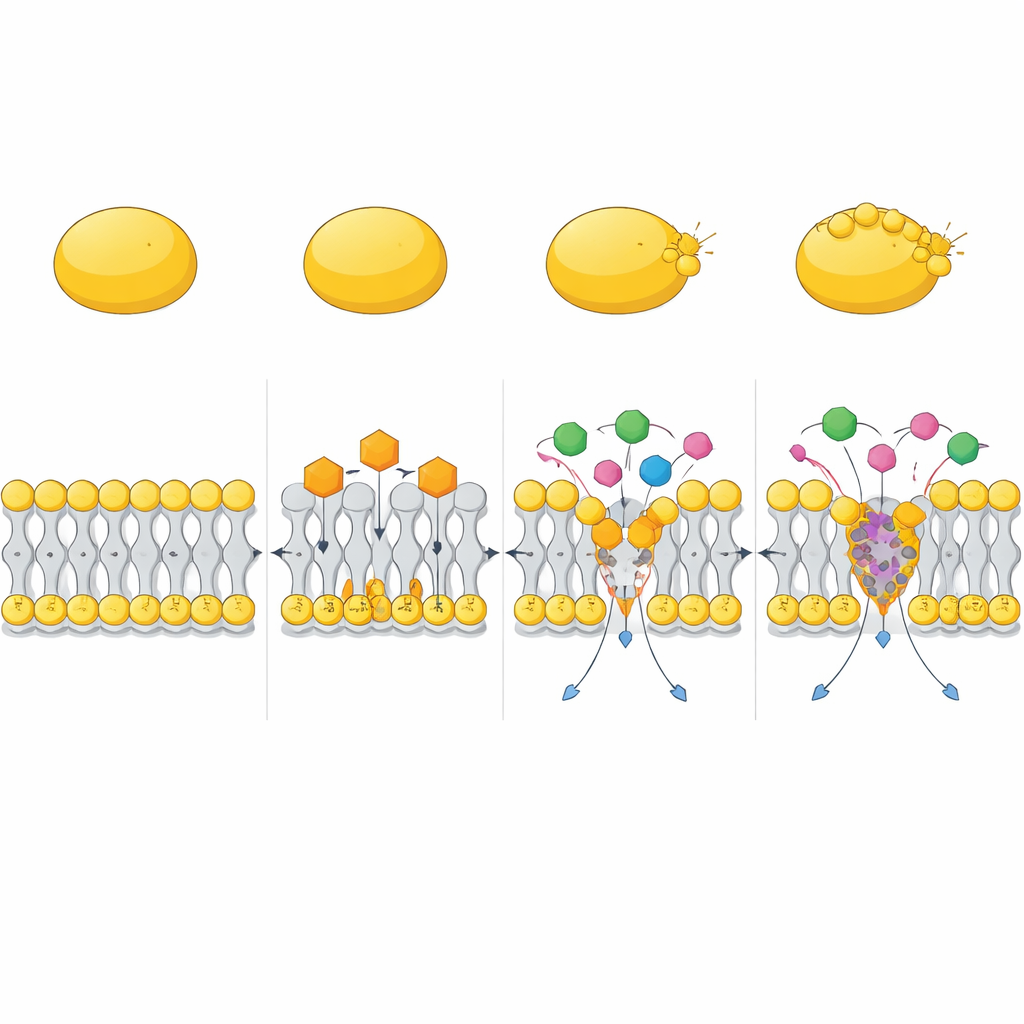
Im Team mit bestehenden Antibiotika
Die Studie untersuchte auch, wie CC zusammen mit vorhandenen Arzneien wirkt. In Checkerboard- und Zeit-Kill-Experimenten verstärkte CC die Aktivität von Aminoglykosid-Antibiotika wie Gentamicin sowie von Polymyxin B dramatisch. Diese Kombinationen beseitigten schnell sowohl aktiv wachsende MRSA als auch schwer zu tötene Persister-Zellen, während die Einzelwirkstoffe oft Überlebende zurückließen. Computersimulationen deuteten auf einen Grund hin: CC kann kompakte Komplexe mit Polymyxin B bilden, die sich in die Membran einfügen und sie eindrucksvoller verformen als die einzelnen Moleküle allein, wodurch tiefe, weitreichende Deformationen in der Lipidschicht entstehen. Das erleichtert anderen Antibiotika das Überwinden der Membranbarriere und das Erreichen ihrer Ziele effizienter.
Vom Petrischale-Experiment zum Lebenden Tier
Ermutigend waren die antibakteriellen und unterstützenden Effekte von CC nicht auf Reagenzgläser beschränkt. In winzigen Würmern und Wachsmottenlarven, die mit MRSA infiziert waren, verbesserte CC das Überleben. In einem Mausmodell mit Oberschenkelinfektion durch einen virulenten MRSA-Stamm reduzierte CC allein die Bakterienzahlen, und die Kombination mit Gentamicin senkte die bakterielle Last im Vergleich zu unbehandelten Kontrollen um etwa das Tausendfache. Blutmessungen zeigten, dass im Labor wirksame Arzneispiegel in Mäusen erreicht werden konnten, ohne über den Versuchszeitraum offensichtliche Schäden an Leber, Niere oder Herzgewebe zu verursachen.
Was das für zukünftige Behandlungen bedeuten könnte
Ganz nüchtern zeigt diese Arbeit, dass ein seit langem eingesetztes Blutdruckmedikament zugleich als membranzielgerichtete Waffe gegen MRSA dienen kann. Indem es sich an spezifische Fettsäure-Bausteine in der bakteriellen Hülle anlagert, die Membran versteift und Löcher hineinbohrt, tötet Candesartan cilexetil MRSA direkt und öffnet zugleich die Tür dafür, dass ältere Antibiotika wieder wirken. Obwohl weitere Sicherheits- und Dosierungsstudien nötig sind — besonders weil dieses Medikament auch auf menschliche Blutgefäße wirkt — deuten die Befunde auf eine vielversprechende Abkürzung hin: Statt völlig neue Antibiotika zu entwickeln, könnten wir bestehende Wirkstoffe umfunktionieren, um bakterielle Abwehrmechanismen zu schwächen und die Wirksamkeit bereits verfügbarer Behandlungen wiederherzustellen.
Zitation: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Schlüsselwörter: MRSA, antibiotikaresistenz, Wirkstoff-Repositionierung, bakterielle Membran, candesartan cilexetil