Clear Sky Science · ar
كانديسارتان سيليكستيل يعطل غشاء المكورات العنقودية المقاومة للميثيسيلين ويقوّي فعالية الجنتاميسين والبوليميكسين B
تحويل دواء خافض للضغط إلى حليف لمكافحة الجراثيم
المكورات العنقودية المقاومة للميثيسيلين (MRSA) هي جرثومة مستعصية في المستشفيات والمجتمع تقاوم العديد من أفضل مضاداتنا الحيوية. يطرح هذا البحث سؤالاً مفاجئاً: هل يمكن إعادة توظيف دواء شائع لخفض ضغط الدم، كانديسارتان سيليكستيل، لإضعاف MRSA وجعل المضادات الحيوية القياسية أكثر فعالية؟ من خلال فحص خلايا MRSA من زوايا متعددة — كيمياء، جينات، تصوير ونماذج حيوانية — يوضح الباحثون كيف يمكن لهذا الدواء أن يثقّب دفاعات البكتيريا ويعيد فعالية أدوية أقدم.
لماذا يصعب علاج المكورات العنقودية المقاومة للمضادات الحيوية
تسبب MRSA مئات الآلاف من الإصابات الحادة وآلاف الوفيات سنوياً. أحد أسباب صعوبة علاجها هو أن غشائها الخارجي وجدار الخلية يعملان كدرع ذكي. يمكن إعادة ترتيب الجزيئات الدهنية في هذا الدرع لتصبح أكثر صلابة وأقل نفاذية وأكثر مقاومة للمضادات الحيوية القياسية. تدخل بعض خلايا MRSA أيضاً في حالات بطيئة النمو تسمى "المثابرون" أو تختبئ في أغشية لزجة (بيوفيلم)، حيث تتحمل الأدوية التي تقتل عادة البكتيريا النشطة. تجعل هذه الخصائص من الضروري إيجاد طرق جديدة لمهاجمة السطح البكتيري بدلاً من تصميم مضاد حيوي تقليدي جديد من الصفر.
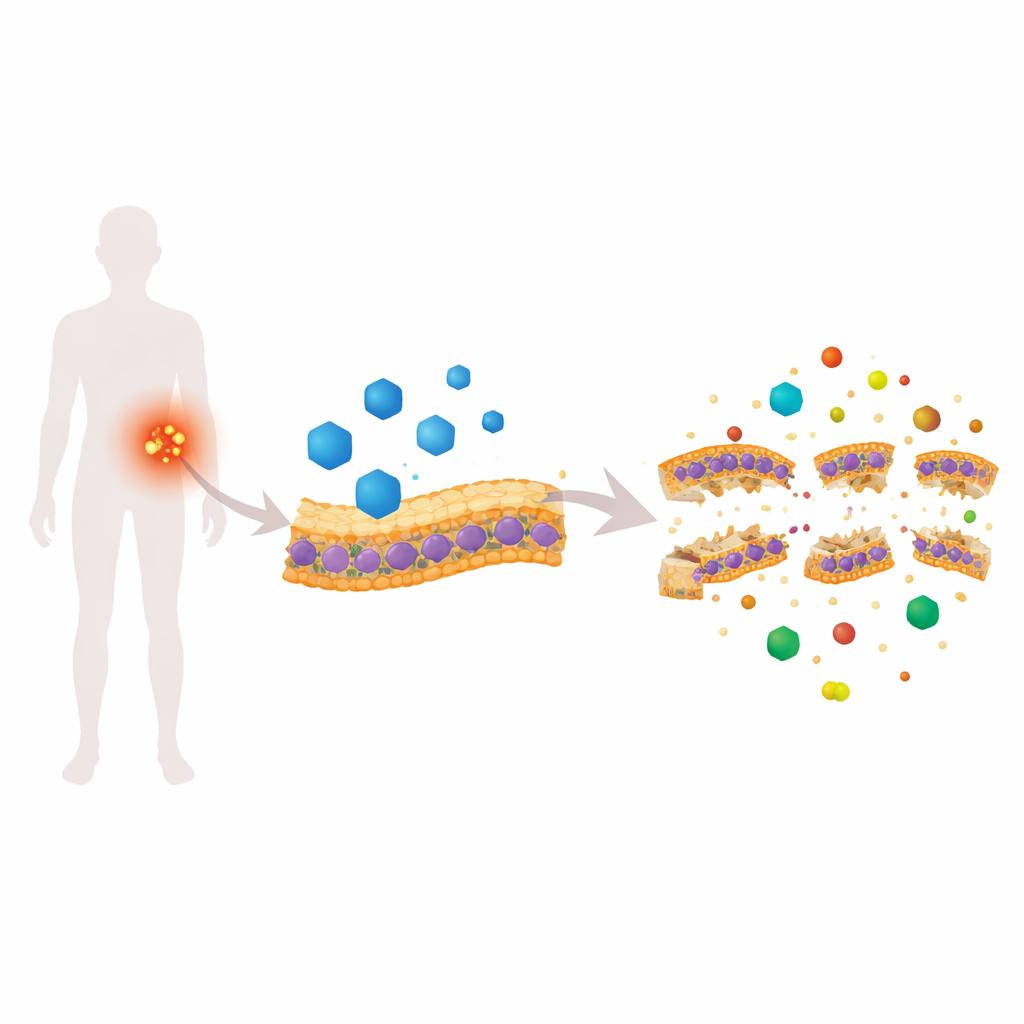
دواء للقلب يهاجم "جلود" البكتيريا
كانديسارتان سيليكستيل (CC) مرخّص لعلاج ارتفاع ضغط الدم، لكن في فحص للأدوية مستخدماً دود الخيط، أظهر بشكل غير متوقع نشاطاً قوياً ضد MRSA. في اختبارات مخبرية، قضى CC على خلايا MRSA المنقسمة بنشاط والخلايا الأكثر عناداً في الطور الساكن، كما قلّل من تكوين البيوفيلم وقابلية العيش فيه. كشفت تجارب مفصلة باستخدام صبغات فلورية أن CC يجعل غشاء MRSA مسرباً بسرعة، ويؤدي إلى انهيار التدرج الكهربائي عبره، ويتسبب في أن يصبح داخل الخلية قلوياً بشكل غير معتاد. أظهر التصوير عالي الدقة — المجهر الإلكتروني الماسح، مجهر القوة الذرية، المجهر الإلكتروني النافذ، والتصوير المجمد المقطعي ثلاثي الأبعاد — أسطحاً مبلّلة، وترققاً في الغشاء، وفجوات مرئية، وهي كلها علامات على أن "جلد" البكتيريا متضرر مادياً.
إعادة توصيل كيمياء الجرثوم وطبقة الدهون
لفهم ما يفعله CC تحت السطح، جمعت الفريق تسلسل الحمض النووي الريبي، وتحليل المستقلبات، وتحليل الدهون. وجدوا أن الجينات والجزيئات الصغيرة المشاركة في بناء جدار الخلية، وصنع دهون الغشاء، وتوليد الطاقة كانت مقللة على نطاق واسع بعد تعرضها لـCC، حتى عند جرعات منخفضة لا تقتل مباشرة. انخفضت وفرة عدة فوسفوليبيدات رئيسية تساعد في المحافظة على تماسك الغشاء. كان تغير لافت يتعلق بمجموعة معينة من الأحماض الدهنية الطويلة بطول 20 ذرة كربون (المسمّاة C20:0). عندما استخدم الباحثون مركباً آخر، السيرولينين، لاستنزاف هذه الأحماض الدهنية، أصبحت MRSA أقل حساسية لـCC. إعادة إضافة أحماض دهنية C20:0 أعادت كثيراً من فعالية الدواء، وأظهرت تجارب ربط منفصلة أن CC يتفاعل مباشرة مع الدهون المرتبطة بـC20:0 ومكونات سطحية ذات صلة. أشارت قياسات "سيولة" الغشاء إلى أن CC فعلياً يقسِّي غشاء MRSA، مقفلاً الدهون في حالة أكثر صلابة تؤدي في النهاية إلى تقويض وظيفته.
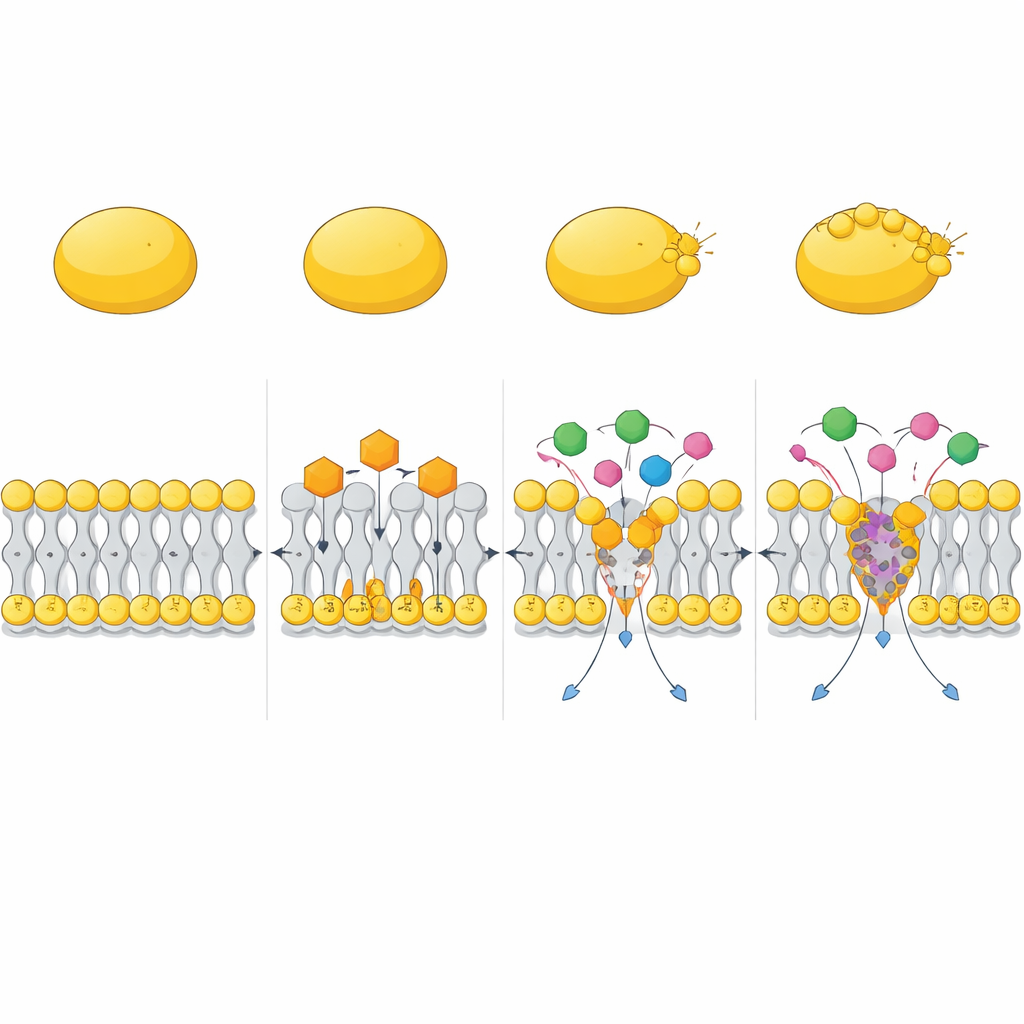
التحالف مع المضادات الحيوية الموجودة
اختبر البحث أيضاً كيف يتصرف CC إلى جانب الأدوية الموجودة. في تجارب شبكة التراكيز وتجارب القتل الزمني، عزز CC بشكل كبير فعالية مضادات أمينوغليكوزيد مثل الجنتاميسين، وكذلك البوليميكسين B. قضت هذه التركيبات بسرعة على كل من MRSA النامية بنشاط وخلايا المثابر الصعبة القتل، في حين غالباً ما كانت الأدوية المفردة تترك ناجين. أشارت المحاكاة الحاسوبية إلى سبب محتمل: يمكن لـCC تكوين مركبات مدمجة مع البوليميكسين B تدخل الغشاء وتشوهه بقوة أكبر من كل جزيء بمفرده، محدثة تشوهات عميقة وواسعة في طبقة الدهون. هذا يساعد مضادات حيوية أخرى على عبور حاجز الغشاء والوصول إلى أهدافها بكفاءة أكبر.
من طبق بتري إلى حيوانات حية
من المشجع أن تأثيرات CC المضادة للبكتيريا والمساعدة امتدت إلى ما هو أبعد من الأنبوب الاختباري. في دودات صغيرة ويرقات عثة الشمع المصابة بـMRSA، حسّن CC البقاء على قيد الحياة. في نموذج عدوى فخذ الفأر باستخدام سلالة MRSA شديدة الفوعة، قلل CC وحده أعداد البكتيريا، وقلّص توليفه مع الجنتاميسين العبء الجرثومي بحوالي ألف ضعف مقارنةً مع الضوابط غير المعالجة. أظهرت قياسات الدم أن مستويات الدواء المماثلة لتلك الفعالة في المختبر يمكن الوصول إليها في الفئران دون تلف واضح في أنسجة الكبد أو الكلية أو القلب خلال فترة التجربة.
ما الذي قد يعنيه هذا لعلاجات المستقبل
بعبارات بسيطة، تكشف هذه الدراسة أن دواءً طويل الاستخدام لخفض ضغط الدم يمكن أن يعمل كسلاح يستهدف الأغشية ضد MRSA. من خلال الارتباط بلبنات دهنية محددة في غلاف البكتيريا، وتصلب الغشاء، وفتح ثقوب فيه، يقضي كانديسارتان سيليكستيل على MRSA مباشرة ويفتح الباب أمام أدوية أقدم لتعمل مجدداً. بينما هناك حاجة لمزيد من دراسات السلامة والجرعات — خاصة لأن هذا الدواء يؤثر أيضاً على الأوعية الدموية البشرية — تشير النتائج إلى طريق مختصر واعد: بدلاً من اختراع مضادات حيوية جديدة تماماً، قد نعيد تهيئة أدوية موجودة لإضعاف دفاعات البكتيريا واستعادة فعالية العلاجات التي لدينا بالفعل.
الاستشهاد: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
الكلمات المفتاحية: MRSA, مقاومة المضادات الحيوية, إعادة توظيف الأدوية, غشاء بكتيري, كانديسارتان سيليكستيل